Proteina
Le proteine sono state definite come macromolecole biologiche presenti in tutte le cellule viventi , ma recenti studi dimostrano che esistono anche centinaia se non migliaia di micro o nano-proteine. Sono formati da una o più catene polipeptidiche . Ognuna di queste catene è composta dalla sequenza di residui di amminoacidi legati tra loro da legami peptidici .
Le proteine svolgono una moltitudine di funzioni all'interno delle cellule viventi e nei tessuti . Sono proteine enzimatiche ( enzimi ) che catalizzano la sintesi chimica e le reazioni di degradazione necessarie al metabolismo della cellula. Altre proteine svolgono un ruolo strutturale all'interno del citoscheletro o dei tessuti ( actina , collagene ), alcune sono motori molecolari che consentono la mobilità ( miosina ), altre sono coinvolte nel condizionamento del DNA ( istoni ), regolazione dell'espressione genica ( fattori di trascrizione ), energia metabolismo ( ATP sintasi ) o la trasmissione di segnali cellulari ( recettori di membrana ).
Le catene proteiche sono sintetizzate nella cellula dai ribosomi , a partire dalle informazioni codificate nei geni , che determinano l'ordine in cui sono legati i 22 amminoacidi, detti proteinogeni , che vengono incorporati direttamente durante la biosintesi dei geni . La sequenza degli amminoacidi è chiamata sequenza polipeptidica. Delle modificazioni post-traduzionali può poi intervenire una volta sola la proteina sintetizzata, che può avere l'effetto di modificarne le proprietà fisiche o chimiche. E 'anche comune per molecole non proteiche, chiamati gruppi prostetici , per legare stabilmente alle proteine e contribuire in modo decisivo alla loro funzioni biologiche: questo è per esempio il caso di eme in emoglobina , senza i quali la proteina non può trasportare ossigeno nel sangue .
Le proteine adottano una struttura tridimensionale che consente loro di svolgere la loro funzione biologica. Questa particolare struttura è determinata soprattutto dalla loro sequenza amminoacidica, le cui diverse proprietà fisico-chimiche portano la catena proteica ad adottare un ripiegamento stabile.
In laboratorio, possono essere separati da altri costituenti cellulari utilizzando varie tecniche come l' ultracentrifugazione , la precipitazione , l' elettroforesi e la cromatografia . L' ingegneria genetica ha introdotto una serie di metodi per facilitare la purificazione delle proteine. La loro struttura può essere studiata mediante immunoistochimica , mutagenesi sito- diretta, cristallografia a raggi X , risonanza magnetica nucleare e spettrometria di massa .
Le proteine sono una componente importante del cibo animale, vengono degradate nel tratto digestivo e gli amminoacidi rilasciati vengono poi riutilizzati dall'organismo.
distinguiamo tra proteine complete e proteine incomplete. Una proteina completa contiene tutti e nove gli amminoacidi essenziali mentre una proteina incompleta che si trova negli alimenti di origine vegetale non li contiene tutti.
Etimologia
Le proteine furono scoperte dal 1835 nei Paesi Bassi dal chimico organico Gerardus Johannes Mulder (1802-1880), sotto il nome di wortelstof . Fu il suo illustre collega svedese, Jöns Jacob Berzelius , a suggerirgli il nome proteina nel 1838 .
Il termine proteina deriva dal greco antico prôtos che significa primo , essenziale . Questo probabilmente si riferisce al fatto che le proteine sono essenziali per la vita e spesso costituiscono la maggioranza (parte 60%) del peso secco delle cellule (animali). Un'altra teoria è che la proteina si riferisce, come l'aggettivo proteiforme, al dio greco Proteus che poteva cambiare forma a piacimento. Le proteine assumono molte forme e svolgono molteplici funzioni. Ma questo non è stato scoperto solo molto più tardi, nel corso del XX ° secolo .
Biochimica
Le proteine sono formate da una o più catene polipeptidiche , che sono biopolimeri lineari, possono essere piuttosto lunghe, composte da una ventina di acidi L -α-ammino diversi. In genere si parla di proteine con più di cinquanta residui nella molecola, e di peptidi fino a poche decine di residui.
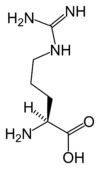
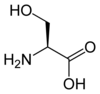
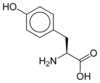
Tutti gli amminoacidi proteinogenici - ad eccezione della prolina - condividono una struttura comune costituita da una funzione acido carbossilico , un'ammina primaria sul carbonio α , e una catena laterale . Quest'ultimo ha una varietà molto ampia di strutture chimiche, ed è l'effetto combinato di tutte queste catene laterali di una catena polipeptidica che determina la struttura tridimensionale e le proprietà chimiche di quest'ultima. La scheda sottostante mostra la struttura chimica dei 22 aminoacidi proteinogenici:
|
Struttura di 22 aminoacidi proteinogenici . La pirrolisina e la selenocisteina (sopra in grigio) sono specifiche di alcune proteine : - la pirrolisina presente solo in alcuni metanogeni arcaici , - la selenocisteina è presente anche tra gli eucarioti ma a priori in decine di enzimi della famiglia delle ossidoriduttasi . Gli altri 20 amminoacidi, detti standard, sono invece universalmente distribuiti in tutti gli esseri viventi conosciuti. |
Gli amminoacidi in una catena polipeptidica sono legati tra loro da legami peptidici che si stabiliscono tra il carbossile -COOH di un primo amminoacido e l' ammina primaria -NH 2 un secondo:
La spina dorsale della proteina è quindi costituita da una catena lineare di amminoacidi a cui le catene laterali sono collegate e legate da legami peptidici. Il legame peptidico presenta due forme di risonanza che gli conferiscono in parte le proprietà di un doppio legame , che limita le rotazioni attorno al proprio asse, in modo che i quattro atomi del gruppo ammidico - (C = O) NH- siano sempre grossolanamente complanari . Gli altri due legami che costituiscono la spina dorsale dell'amminoacido, invece, possono ruotare liberamente. I due angoli diedri corrispondenti a questi due legami interni determinano la geometria locale adottata dalla catena proteica.
L'estremità carbossilica della catena laterale polipeptidica è chiamata estremità C- terminale , mentre il lato amminico è chiamato estremità N- terminale . Le parole proteina, polipeptide e peptide sono piuttosto ambigue e i loro significati possono sovrapporsi. Si parla generalmente di proteina in riferimento alla molecola biologica completa dotata di una conformazione stabile, mentre un peptide designa generalmente una molecola più corta senza una struttura tridimensionale stabile. La linea tra i due è molto imprecisa e si aggira intorno a qualche dozzina di residui di amminoacidi.
taglie
Le proteine sono sempre state ritenute grandi (a scala biomolecolare); c'era un senso dagli anni '80 e sapevamo dall'inizio degli anni '90 che non era così, in seguito alla scoperta di una, poi di alcune altre MicroProteine (a volte chiamate MiP ). Da allora, gli scienziati hanno dimostrato l'esistenza di centinaia e poi migliaia di microproteine e nanoproteine (a volte associando solo pochi amminoacidi, magari autoassemblati), così piccole che i sistemi di analisi genomica classici non riescono a non individuarle. Sembrano avere ruoli chiave all'interno delle cellule all'interno del complesso proteico , interagendo nelle relazioni proteina-proteina. Alcuni controllano così l'attività di proteine più grandi, svolgendo un ruolo di regolatori post-traduzionali, senza interagire direttamente con il DNA o l'RNA. Altri promuovono lo sviluppo muscolare e regolano la contrazione muscolare . Altri ancora contribuiscono alla gestione dei rifiuti intracellulari (RNA vecchio, degradato o difettoso). Nelle piante, potrebbero partecipare alla rilevazione della luce e in altri casi svolgere un ruolo nella segnalazione fito- ormonale . Negli animali, partecipano al funzionamento dell'orologio biologico .
Si trova in particolare nei veleni (di ragni , scorpioni e altri animali velenosi ). Nanoproteine complesse possono essere create in vitro mediante autoassemblaggio di amminoacidi ; potrebbero forse essere usati per il riconoscimento biomolecolare e la catalisi. Sono già stati trovati di interesse commerciale: alcuni insetticidi lo usano. Sono di interesse medico: servono per marcare i tumori cerebrali per consentire interventi chirurgici più precisi.
Struttura
La natura delle proteine è determinata soprattutto dalla loro sequenza amminoacidica, che ne costituisce la struttura primaria . Amminoacidi aventi proprietà chimiche molto diverse, la loro disposizione lungo la catena polipeptidica determina la loro disposizione spaziale. Questo è descritto localmente dalla loro struttura secondaria , stabilizzata da legami idrogeno tra residui amminoacidici vicini, e globalmente dalla loro struttura terziaria , stabilizzata da tutte le interazioni tra i residui - a volte molto distanti sulla sequenza peptidica ma portate a contatto spazialmente dal ripiegamento della proteina - così come tra la proteina stessa e il suo ambiente. Infine, l'assemblaggio di diverse subunità proteiche per formare un complesso funzionale è descritto dalla struttura quaternaria di questo insieme.
Possono inoltre formarsi ulteriori legami covalenti, sia all'interno della stessa catena proteica, sia tra diverse catene peptidiche all'interno di una proteina, in particolare attraverso la formazione di ponti disolfuro tra residui di cisteina .
La maggior parte delle proteine adotta una conformazione tridimensionale unica. La forma naturale di una proteina in vivo è il suo stato nativo , che è la forma che assume per essere biologicamente attiva e funzionale. Molte proteine sono esse stesse biologicamente attive da esse sotto l'effetto della distribuzione spaziale dei residui di amminoacidi che le costituiscono, altre necessitano per fare ciò di essere assistite da proteine chaperone per essere ripiegate secondo il loro stato originario.
Livelli organizzativi
In biochimica , possiamo quindi distinguere quattro livelli di organizzazione per descrivere la struttura delle proteine:
- La struttura primaria corrisponde alla sequenza degli amminoacidi.
- La struttura secondaria descrive la disposizione dei residui di amminoacidi osservabili su scala atomica. Stabilizzate da legami idrogeno , queste disposizioni locali sono ad esempio le α eliche , i fogli , i barili β oi gomiti. Esistono diverse varietà ed è comune che una proteina abbia diversi tipi di strutture secondarie nel suo insieme.
- La struttura terziaria corrisponde alla forma generale della proteina osservabile sulla scala dell'intera molecola. Descrive le interazioni tra i diversi elementi della struttura secondaria. È stabilizzato da tutta una serie di interazioni che spesso portano alla formazione di un nucleo idrofobo , possibilmente con legami salini , legami idrogeno, ponti disolfuro o anche modifiche post-traduzionali . Una struttura terziaria viene spesso definita ripiegamento di una proteina.
- La struttura quaternaria descrive il complesso risultante dall'assemblaggio di più molecole proteiche (più catene polipeptidiche), chiamate in questo caso subunità proteiche per formare un unico complesso proteico. Tutte le proteine non sono necessariamente costituite da più subunità e quindi non sempre hanno una struttura quaternaria.
Le proteine non sono molecole completamente rigide. È probabile che adottino diverse conformazioni correlate mentre svolgono le loro funzioni biologiche. Il passaggio da una di queste conformazioni ad un'altra è chiamato cambiamento conformazionale . Nel caso di un enzima, ad esempio, tali cambiamenti conformazionali possono essere indotti dall'interazione con il substrato a livello del sito attivo . In soluzione, le proteine subiscono anche molti cambiamenti conformazionali dovuti alla vibrazione termica della collisione con altre molecole.
Implicazioni biologiche e determinazione delle strutture terziarie e quaternarie
Esistono tre grandi gruppi di proteine a seconda della loro struttura terziaria o quaternaria: le proteine globulari , le proteine fibrose e le proteine di membrana . Quasi tutte le proteine globulari sono solubili e spesso sono enzimi . Le proteine fibrose svolgono spesso un ruolo strutturale, come il collagene , il principale costituente del tessuto connettivo , o la cheratina , un costituente proteico dei capelli e delle unghie . Le proteine di membrana sono spesso recettori o canali che consentono alle molecole polari o caricate elettricamente di passare attraverso la membrana .
La conoscenza della struttura terziaria, o anche quaternaria, di una proteina può fornire importanti informazioni per comprendere come questa proteina svolge la sua funzione biologica. La cristallografia a raggi X e la spettroscopia NMR sono metodi sperimentali comuni per studiare la struttura delle proteine, che possono l'uno e l'altro fornire informazioni con una risoluzione in scala atomica . I dati NMR forniscono informazioni dalle quali è possibile stimare un sottoinsieme di distanze tra determinate coppie di atomi, che permette di dedurre le possibili conformazioni di questa molecola. L' interferometria a doppia polarizzazione è un metodo analitico quantitativo per misurare la conformazione complessiva della proteina e le sue variazioni conformazionali in funzione della sua interazione con altri stimoli. Il dicroismo circolare fornisce un'altra tecnica di laboratorio per risolvere alcuni elementi della struttura secondaria delle proteine ( α eliche e fogli β particolari). La microscopia crioelettronica fornisce informazioni strutturali a bassa risoluzione su proteine molto grandi, inclusi i virus . La cristallografia elettronica (in) , tecnica fine della precedente, permette in alcuni casi di produrre anche dati ad alta risoluzione, soprattutto per cristalli bidimensionali di proteine di membrana . Le strutture proteiche risolte sono generalmente depositate nel Protein Data Bank (PDB), un database ad accesso aperto che fornisce la struttura di mille proteine per le quali sono disponibili le coordinate cartesiane di ciascun atomo.
Il numero di proteine la cui struttura è stata risolta è molto inferiore al numero di geni la cui sequenza è nota. Inoltre, il sottoinsieme di proteine la cui struttura è stata risolta è sbilanciato a favore di proteine che possono essere facilmente preparate per l'analisi mediante cristallografia a raggi X, uno dei principali metodi per determinare le strutture proteiche. In particolare, le proteine globulari sono comparativamente le più facili da cristallizzare per la cristallografia, mentre le proteine di membrana sono più difficili da cristallizzare e sono sottorappresentate tra le proteine disponibili in PDB. Per porre rimedio a questa situazione, sono stati intrapresi approcci di genomica strutturale al fine di risolvere le strutture rappresentative delle principali classi di ripiegamento proteico . I metodi di previsione della struttura proteica mirano a fornire i mezzi per generare la struttura plausibile di una proteina da strutture che potrebbero essere determinate sperimentalmente.
Sintesi
Gli α-ammino proteinogenici acidi sono assemblati in polipeptidi all'interno delle cellule dai ribosomi dall'informazione genetica trasmessa dall'RNA messaggero dal DNA che comprende i geni . È la sequenza nucleotidica del DNA, trascritta identicamente nell'RNA messaggero, che trasporta l'informazione letta dai ribosomi per produrre proteine secondo la sequenza peptidica specificata dai geni. La corrispondenza tra la sequenza nucleotidica del DNA e dell'RNA messaggero da un lato e la sequenza peptidica delle proteine sintetizzate dall'altro è determinata dal codice genetico , che è sostanzialmente lo stesso per tutti gli esseri viventi conosciuti tranne un numero abbastanza limitato di variazioni.
Codice genetico
Il codice genetico stabilisce la corrispondenza tra una tripletta di basi nucleiche , detta codone , sull'RNA messaggero e un α-amminoacido proteinogenico. Questa corrispondenza è svolta in vivo dagli RNA transfer , che sono RNA comprendenti al massimo un centinaio di nucleotidi e portatori di un amminoacido che esterifica la loro estremità 3'-OH. Ciascuno degli amminoacidi è legato a specifici RNA di trasferimento, anch'essi portatori di codoni specifici, in modo che ciascuno dei 64 possibili codoni possa codificare un solo amminoacido. D'altra parte, ciascuno dei 22 aminoacidi proteinogenici può essere codificato da diversi codoni. Sono gli enzimi che effettuano l'esterificazione degli RNA messaggeri con amminoacidi - amminoacil-tRNA sintetasi - che mantengono il codice genetico: infatti, questi enzimi si legano specificamente sia ad un dato RNA di trasferimento che ad un amminoacido dato, in modo che ciascuno tipo di RNA di trasferimento è esterificato solo con un amminoacido specifico.
Il caso della selenocisteina e della pirrolisina è alquanto diverso in quanto questi particolari amminoacidi non sono codificati direttamente da codoni specifici ma dalla ricodifica traduzionale dei codoni di stop in presenza di particolari sequenze di inserzione chiamate rispettivamente elemento SECIS e elemento PYLIS , che ricodificano i codoni di stop UGA (Opale) e UAG (Ambra) in selenocisteina e pirrolisina, rispettivamente. Inoltre, la selenocisteina non è legata come tale al suo RNA di trasferimento, perché è troppo reattiva per esistere liberamente nella cellula; è la serina che è legata ad un RNA di trasferimento della selenocisteina Sec tRNA dalla serina tRNA ligasi . Il seril - tRNA Sec non può essere utilizzato dai ribosomi in quanto non è riconosciuto dai fattori di allungamento coinvolti nella biosintesi delle proteine , per cui la serina può essere incorporata nelle selenoproteine al posto della selenocisteina. Al contrario, seril-tRNA Sec è un substrato per alcuni enzimi che la sua conversione in sélénocystéinyl - tRNA Sec : conversione diretta dal selenocisteina sintasi in batteri , conversione indiretta tramite l' O -phosphoséryl -ARNt Sec successivamente dalla O - phosphoseryl-tRNA Sec chinasi e O -fosfoseril-tRNA: selenocisteinil-tRNA sintasi in archaea ed eucarioti .
I geni codificati nel DNA vengono prima di tutto trascritti nell'RNA pre-messaggero da enzimi come le RNA polimerasi . La maggior parte degli esseri viventi modifica questo RNA pre-messaggero attraverso una serie di processi chiamati modificazioni post-trascrizionali che portano all'RNA messaggero maturo. Quest'ultimo può quindi essere utilizzato dai ribosomi per fungere da modello durante la biosintesi delle proteine . Nei procarioti , l'RNA messaggero può essere utilizzato non appena sintetizzato o tradotto in proteine dopo aver lasciato il nucleoide . Al contrario, negli eucarioti , l'RNA messaggero è prodotto nel nucleo della cellula mentre le proteine sono sintetizzate nel citoplasma , quindi l'RNA messaggero deve attraversare la membrana nucleare .
Biosintesi
La biosintesi di una proteina da un RNA messaggero è la traduzione di questo mRNA. L'RNA messaggero si lega al ribosoma, che lo legge in sequenza a tre nucleotidi in ogni fase della sintesi. Ogni tripletta di nucleotidi costituisce un codone sull'RNA messaggero, al quale può legarsi l' anticodone di un RNA di trasferimento che fornisce l'amminoacido corrispondente. L' accoppiamento tra il codone e l'anticodone si basa sulla complementarietà delle rispettive sequenze . È questa complementarietà che assicura il riconoscimento tra l'RNA di trasferimento e il codone dell'RNA messaggero. L'amminoacido fornito dall'RNA di trasferimento sul ribosoma stabilisce un legame peptidico con l' estremità C - terminale della catena nascente, che gli consente di estendersi di un residuo amminoacidico. Il ribosoma sposta quindi tre nucleotidi sull'RNA messaggero per affrontare un nuovo codone, che segue esattamente il codone precedente. Questo processo viene ripetuto fino a quando il ribosoma si trova davanti a un codone di stop , nel qual caso la traduzione si interrompe.
La biosintesi di una proteina viene effettuata e il residuo dopo residuo, l' estremità N -Terminal all'estremità C -Terminal . Una volta sintetizzata, la proteina può subire varie modificazioni post-traduzionali come scissione , fosforilazione , acetilazione , amidazione , metilazione , glicosilazione , lipidazione , o anche la formazione di legami disolfuro . La dimensione delle proteine così sintetizzate è molto variabile. Questo formato può essere espressa in numero di aminoacidi residui ammino costituiscono queste proteine, come pure in dalton (simbolo Da), che in biologia molecolare corrispondono alla unità di massa atomica . Poiché le proteine sono spesso molecole piuttosto grandi, la loro massa è spesso espressa in kilodalton (simbolo kDa). Ad esempio, le proteine del lievito hanno una lunghezza media di 466 residui amminoacidici, per una massa di 53 kDa . Le proteine più grandi conosciute sono le titine dei sarcomeri che formano le miofibrille dei muscoli scheletrici striati : la titina di topo contiene circa 35.213 residui di amminoacidi costituiti da 551.739 atomi con una massa di oltre 3.900 kDa e una lunghezza di l dell'ordine di 1 µm .
Sintesi chimica
Le piccole proteine possono anche essere sintetizzate in vitro mediante una varietà di metodi noti di sintesi peptidica , che si basano su tecniche di sintesi organica come la legatura chimica (in) per produrre efficacemente peptidi. La sintesi chimica permette di introdurre amminoacidi innaturali nella catena polipeptidica, ad esempio posizionando sonde fluorescenti sulla catena laterale di alcuni di essi. Questi metodi sono utili in laboratorio in biochimica e biologia cellulare ma non sono generalmente impiegati per applicazioni commerciali. La sintesi chimica non è efficiente nel sintetizzare peptidi di più di circa 300 residui di amminoacidi e le proteine così prodotte potrebbero non assumere facilmente la loro struttura terziaria nativa. Molti metodi di sintesi proteica chimica procedono dalla fine C -Terminal alla fine N -Terminal , vale a dire nella direzione opposta alla biosintesi di proteine da ribosomi .
Funzioni
Tra tutti i costituenti della cellula, le proteine sono gli elementi più attivi. A parte alcuni RNA , la maggior parte delle altre molecole biologiche non sono abbastanza reattive chimicamente e sono le proteine ad agire su di esse. Le proteine costituiscono circa la metà della sostanza secca di una cellula di E. coli , mentre l' RNA e il DNA costituiscono rispettivamente un quinto e il 3%. Tutte le proteine espresse in una cellula ne costituiscono il proteoma .
La caratteristica principale delle proteine che consente loro di svolgere le loro funzioni biologiche è la loro capacità di legarsi ad altre molecole in modo molto specifico e molto stretto. La regione di una proteina che si lega a un'altra molecola è il suo sito di legame, che spesso forma una depressione, una cavità o una "tasca" sulla superficie della molecola. È la struttura terziaria della proteina e la natura chimica delle catene laterali dei residui di amminoacidi del sito di legame che determina la specificità di questa interazione. I siti di legame possono portare a legami particolarmente specifici e stretti: così, l' inibitore della ribonucleasi si lega all'angiogenina umana con una costante di dissociazione sub-femtomolare ( <10 −15 mol L −1 ) ma non si lega affatto alla Ranpirnasi , omologa di anfibio di questa proteina (costante maggiore di 1 mol L -1 ). Una leggera modifica chimica può alterare radicalmente la capacità di una molecola di interagire con una data proteina. Così, l' aminoacil-tRNA sintetasi specifica per la valina si lega a quest'ultima senza interagire con l' isoleucina , che però è strutturalmente molto vicina ad essa.
Le proteine possono legarsi ad altre proteine oa piccole molecole come substrati . Quando si legano specificamente ad altre proteine identiche a se stesse, possono polimerizzare per formare fibrille . Questo è comune per le proteine strutturali, formate da monomeri globulari che si autoassemblano per formare fibre rigide. Delle interazioni proteina-proteina regolano anche la loro attività enzimatica , l'andamento del ciclo cellulare e l'assemblaggio di grandi complessi proteici realizzando condividendo reazioni strettamente correlate una comune funzione biologica. Le proteine possono anche legarsi alla superficie delle membrane cellulari e spesso addirittura diventarne parte integrante. La capacità di alcune proteine di cambiare conformazione quando si legano a specifiche molecole consente la costruzione di reti di segnalazione cellulare estremamente complesse. In generale, lo studio delle interazioni tra specifiche proteine è un elemento chiave per la nostra comprensione del funzionamento delle cellule e della loro capacità di scambiare informazioni.
Enzimi
La parte più visibile delle proteine nella cellula è quella dell'enzima , cioè della biomolecola che catalizza le reazioni chimiche . Gli enzimi sono generalmente molto specifici e accelerano solo una o poche reazioni chimiche. La stragrande maggioranza delle reazioni chimiche nel metabolismo sono svolte da enzimi. Oltre al metabolismo, questi ultimi sono coinvolti nella espressione genica , la replicazione del DNA , DNA riparazione , la trascrizione di DNA in RNA e traduzione di RNA messaggero in proteine. Alcuni enzimi lavorano su altre proteine per legare o scindere determinati gruppi funzionali e residui di altre biomolecole in esse contenute, in un processo chiamato modificazione post-traduzionale . Gli enzimi catalizzano oltre 5.000 diverse reazioni chimiche. Come tutti i catalizzatori, non modificano gli equilibri chimici ma accelerano le reazioni, talvolta in proporzioni considerevoli; quindi, l' orotidina-5'-fosfato decarbossilasi catalizza in millisecondi una reazione che altrimenti richiederebbe diversi milioni di anni.
Le molecole che si legano agli enzimi e sono chimicamente alterate da essi sono chiamate substrati . Sebbene gli enzimi a volte siano costituiti da diverse centinaia di residui di amminoacidi, solo alcuni di essi entrano in contatto con il/i substrato/i dell'enzima e un numero molto piccolo - di solito tre o quattro - è direttamente coinvolto nella catalisi. Il sito attivo è la regione di un enzima coinvolto nella reazione chimica catalizzata da questa proteina: raggruppa i residui che si legano al substrato o contribuiscono al suo posizionamento, nonché i residui che catalizzano direttamente la reazione.
Segnalazione cellulare e legame con il ligando
Molte proteine sono coinvolte nei meccanismi di segnalazione cellulare e di trasduzione del segnale . Alcune proteine come l' insulina appartengono all'ambiente extracellulare e trasmettono un segnale dalla cellula dove vengono sintetizzate ad altre cellule talvolta localizzate in tessuti distanti. Altre sono proteine di membrana che agiscono come recettori la cui funzione principale è quella di legarsi a molecole che trasportano segnali e indurre una risposta biochimica nella cellula bersaglio. Molti recettori di membrana hanno un sito di legame esposto all'esterno della cellula e un effettore di campo (en) a contatto con il mezzo intracellulare. Questo dominio effettore può svolgere un'attività enzimatica o può subire cambiamenti conformazionali agendo su altre proteine intracellulari.
Gli anticorpi sono componenti proteici del sistema immunitario la cui funzione primaria è quella di legarsi ad antigeni o xenobiotici per contrassegnarli per l'eliminazione dall'organismo. Gli anticorpi possono essere secreti nel mezzo extracellulare o ancorati nella membrana plasmatica di linfociti B specializzati chiamati plasmacellule . Laddove gli enzimi sono molto specifici per i loro substrati al fine di accelerare reazioni chimiche molto precise, gli anticorpi non hanno questo vincolo; d'altra parte, la loro affinità per il loro obiettivo è estremamente alta.
Molte proteine trasportatrici di ligandi si legano specificamente a piccole molecole e le trasportano alle loro destinazioni attraverso le cellule ei tessuti degli organismi multicellulari . Queste proteine devono avere un'elevata affinità per il loro ligando quando la sua concentrazione è elevata, ma devono anche essere in grado di rilasciarlo quando la sua concentrazione è bassa nei tessuti bersaglio. L'esempio canonico della proteina che trasporta il ligando è l' emoglobina , che trasporta l' ossigeno dai polmoni ad altri organi e tessuti in tutti i vertebrati e ha controparti correlate in tutti i regni viventi. Le lectine sono proteine che si legano in modo reversibile a determinati carboidrati con specificità molto elevata. Svolgono un ruolo nei fenomeni di riconoscimento biologico che coinvolgono cellule e proteine.
Le proteine transmembrana possono anche svolgere il ruolo di ligando trasportatore, le proteine possono alterare la permeabilità della membrana cellulare alle piccole molecole polari e agli ioni . La membrana stessa ha un nucleo idrofobo attraverso il quale le molecole polari o caricate elettricamente non possono diffondersi. Le proteine di membrana possono così contenere uno o più canali attraverso la membrana cellulare e permettere a queste molecole ea questi ioni di attraversarla. Molti canali ionici sono molto specifici per lo ione che circolano. Pertanto, i canali del potassio e i canali del sodio sono spesso specifici per uno dei due ioni potassio e sodio ad esclusione dell'altro.
proteine strutturali
Le proteine strutturali conferiscono rigidità e rigidità ai costituenti biologici che, senza di esse, sarebbero fluidi. La maggior parte delle proteine strutturali sono fibrose. È il caso ad esempio del collagene e dell'elastina, costituenti essenziali dei tessuti connettivi come la cartilagine , e della cheratina presente in strutture dure o filamentose come capelli , unghie , piume , zoccoli e nell'esoscheletro di alcuni animali . Alcune proteine globulari possono anche svolgere un ruolo strutturale, ad esempio actina e tubulina i cui monomeri sono globulari e solubili ma polimerizzano per formare lunghi filamenti rigidi costituenti il citoscheletro , che permette alla cellula di mantenere la sua forma e dimensione.
Le proteine motorie sono proteine strutturali specifiche in grado di generare forze meccaniche. Questi sono, per esempio , la miosina , chinesina e dineina . Queste proteine sono essenziali per la motilità degli organismi unicellulari così come per lo sperma degli organismi pluricellulari . Aiutano anche a generare le forze che agiscono nella contrazione muscolare e svolgono un ruolo essenziale nel trasporto intracellulare.
Tuttavia, le mannoproteine sembrano avere ruoli chiave all'interno delle cellule, in particolare controllando la porosità della parete cellulare.
Riepilogo delle funzioni svolte dalle proteine
Le proteine svolgono quindi un'ampia varietà di funzioni all'interno della cellula e del corpo:
- le proteine strutturali che consentono alla cellula di mantenere la sua organizzazione nello spazio, e che sono i costituenti del citoscheletro ;
- le proteine di trasporto , che provvedono al trasferimento di diverse molecole dentro e fuori le cellule;
- le proteine regolatrici , che modulano l'attività di altre proteine o che controllano l'espressione genica ;
- le proteine di segnalazione che catturano i segnali esterni e ne assicurano la trasmissione nella cellula o nell'organismo; ne esistono di diversi tipi, ad esempio le proteine ormonali , che aiutano a coordinare le attività di un organismo agendo come segnali tra le cellule;
- le proteine recettrici , che rilevano molecole messaggere e altri segnali affinché la cellula agisca di conseguenza:
- le proteine sensoriali rilevano i segnali ambientali e rispondono trasmettendo segnali nella cellula (es. luce).
- i recettori ormonali rilevano gli ormoni e inviano segnali alla cellula per agire di conseguenza (es. l' insulina è un ormone che, quando ricevuto, indica alla cellula di assorbire e utilizzare il glucosio );
- le proteine motorie , che consentono alle cellule o agli organismi, oa determinati elementi (ciglia) di muoversi o deformarsi (per es., l' actina e la miosina permettono al muscolo di contrarsi );
- le proteine di difesa che proteggono la cellula dagli agenti infettivi (es. l' anticorpo );
- le proteine di riserva che permettono la prenotazione di acido dell'ordine ammino biosynthesize altre proteine (ad esempio la. ovalbumina , la proteina principale di bianco d'uovo fornisce l'immagazzinaggio per lo sviluppo di embrioni di pollo );
- gli enzimi che modificano la velocità di quasi tutte le reazioni chimiche nella cellula senza essere trasformati nella reazione.
Metodi di studio
La struttura e le funzioni delle proteine possono essere studiate in vivo , in vitro e in silico . Gli studi in vivo consentono di esplorare il ruolo fisiologico di una proteina all'interno di una cellula vivente o anche all'interno di un organismo nel suo insieme. Gli studi in vitro di proteine purificate in ambienti controllati sono utili per comprendere come funziona una proteina in vivo : ad esempio, lo studio della cinetica di un enzima permette di analizzare il meccanismo chimico della sua attività catalitica e la sua relativa affinità rispetto a diversi substrati . Gli studi in silico utilizzano algoritmi informatici per modellare le proteine.
Purificazione delle proteine
Per poter essere analizzata in vitro , una proteina deve prima essere stata purificata dagli altri costituenti chimici della cellula. Questo di solito inizia con la lisi della cellula, durante la quale la membrana plasmatica viene rotta per rilasciare il suo contenuto in una soluzione per dare un lisato. Questa miscela può essere purificata mediante ultracentrifugazione , che consente di separare i suoi costituenti in frazioni contenenti rispettivamente proteine solubili, lipidi e proteine di membrana , organelli cellulari e acidi nucleici . La precipitazione delle proteine per rilascio permette di concentrarle da questo lisato. È quindi possibile utilizzare diversi tipi di cromatografia per isolare le proteine che si desidera studiare in base alle loro proprietà fisico-chimiche come la loro massa molare , la loro carica elettrica o anche la loro affinità di legame. Il grado di purificazione può essere seguito utilizzando diversi tipi di elettroforesi su gel se sono noti la massa molecolare e il punto isoelettrico delle proteine studiate, mediante spettroscopia se la proteina ha caratteristiche spettroscopiche identificabili, o mediante saggio enzimatico (in ) se la proteina svolge attività enzimatica . Inoltre, le proteine possono essere isolate in base alla loro carica elettrica mediante focalizzazione isoelettrica .
Le proteine naturali alla fine richiedono una serie di passaggi di purificazione prima di poter essere studiate in laboratorio. Per semplificare questo processo, l'ingegneria genetica viene spesso utilizzata per modificare le proteine dotandole di caratteristiche che le rendano più facili da purificare senza alterarne la struttura o l'attività. Aggiunge così "etichette" riconoscibili sulla proteina sotto forma di sequenze di amminoacidi individuate, spesso un numero di residui di istidina - polyhistidine-tag o His-tag - all'estremità C- terminale o all'estremità N- terminale di la catena polipeptidica . Pertanto, quando il lisato viene posto in una colonna cromatografica contenente nichel , i residui di istidina complessano con il nichel e rimangono legati alla colonna mentre i costituenti non marcati la attraversano senza essere fermati. Sono stati sviluppati diversi tipi di etichette per consentire ai ricercatori di purificare particolari proteine da miscele complesse.
Localizzazione cellulare
Lo studio in vivo delle proteine spesso implica sapere con precisione dove vengono sintetizzate e dove si trovano nelle cellule. Sebbene la maggior parte delle proteine intracellulari sono prodotte nel citoplasma e più membrana o proteine secrete nel mezzo extracellulare sono prodotti nel reticolo endoplasmatico , è raro che si capisce esattamente come le proteine bersaglio i certe strutture cellulari o certe strutture cellulari. Organelli . L' ingegneria genetica fornisce strumenti utili per farsi un'idea della localizzazione di determinate proteine, ad esempio legando la proteina ad una proteina studiata permettendo lo spot, cioè effettuando una fusione proteica tra la proteina studiata e una proteina usata come un marcatore, come la proteina fluorescente verde . La localizzazione intracellulare della proteina di fusione risultante può essere facilmente ed efficientemente visualizzata al microscopio .
Altri metodi di localizzazione intracellulare di proteine prevedono l'uso di marcatori noti per alcuni compartimenti cellulari come il reticolo endoplasmatico , l'apparato di Golgi , i lisosomi , i mitocondri , i cloroplasti , la membrana plasmatica , ecc. È ad esempio possibile localizzare proteine marcate con un'etichetta fluorescente o mirate con anticorpi contro questi marcatori. Le tecniche di immunofluorescenza consentono quindi di localizzare proteine specifiche. I pigmenti fluorescenti sono anche usati per etichettare i compartimenti cellulari per uno scopo simile.
L' immunoistochimica utilizza generalmente un anticorpo mirato a una o più proteine diverse che sono coniugate ad enzimi che emettono segnali luminescenti o cromogeni che possono essere confrontati con vari campioni, il che permette di dedurre informazioni sulla localizzazione delle proteine studiate. È anche possibile utilizzare tecniche di co-frazionamento in un gradiente di saccarosio (o altra sostanza) mediante centrifugazione isopicnica.
La microscopia immunoelettronica combina l'uso della microscopia elettronica convenzionale con l'uso di un anticorpo diretto contro la proteina studiata, questo anticorpo essendo precedentemente coniugato a un materiale ad alta densità elettronica come l' oro . Ciò consente di individuare i dettagli ultrastrutturali e la proteina oggetto di studio.
proteomica
L'insieme delle proteine di una cellula o di un tipo di cellula ne costituisce il proteoma , e la disciplina scientifica che lo studia è la proteomica . Questi due termini sono stati coniati per analogia con genoma e genomica . Se il proteoma è derivato dal genoma, tuttavia, non è possibile prevedere esattamente quale sarà il proteoma di una cellula dalla semplice conoscenza del suo genoma. Infatti, l' espressione di un gene varia da una cellula all'altra all'interno dello stesso organismo in funzione del differenziamento cellulare , o addirittura nella stessa cellula in funzione del ciclo cellulare . Inoltre, lo stesso gene può dare più proteine (ad esempio poliproteine virali ), e spesso sono necessarie modifiche post-traduzionali per rendere attiva una proteina.
Tra le tecniche sperimentali utilizzate in proteomica, si segnalano l' elettroforesi bidimensionale , che consente la separazione di un gran numero di proteine, la spettrometria di massa , che consente l'identificazione rapida e ad alto rendimento delle proteine nonché il sequenziamento dei peptidi (il più delle volte dopo gel digestion (en) ), chip proteici (en) , che consentono di rilevare le concentrazioni relative di un gran numero di proteine presenti in una cellula, e il doppio approccio ibrido che consente anche l'esplorazione delle interazioni proteina-proteina . L'insieme delle interazioni proteina-proteina in una cellula è chiamato interactome . L'approccio per determinare la struttura delle proteine tra tutte le loro possibili conformazioni è la genomica strutturale .
Bioinformatica
Ora sono disponibili una varietà di metodi informatici per analizzare la struttura, la funzione e l'evoluzione delle proteine. Lo sviluppo di tali strumenti è stato reso necessario dalla grande quantità di dati genomici e proteomici disponibili per un numero molto elevato di esseri viventi, a partire dal genoma umano . È impossibile studiare sperimentalmente tutte le proteine, per cui solo un piccolo numero di esse viene studiato in laboratorio mentre gli strumenti computazionali consentono di estrapolare i risultati così ottenuti ad altre proteine ad esse simili. Tali proteine omologhe sono identificate in modo efficiente mediante tecniche di allineamento di sequenza . Gli strumenti di profilazione della sequenza peptidica consentono di individuare i siti scissi dagli enzimi di restrizione , leggere i frame nelle sequenze nucleotidiche e prevedere le strutture secondarie . È anche possibile costruire alberi filogenetici e sviluppare ipotesi sull'evoluzione utilizzando software come ClustalW (in) per risalire agli antenati degli organismi moderni e ai loro geni. Gli strumenti di bioinformatica sono diventati essenziali per lo studio dei geni e delle proteine espresse da questi geni.
Previsione e simulazione della struttura
Oltre alla genomica strutturale, la previsione della struttura proteica mira a sviluppare mezzi per costruire in modo efficiente modelli plausibili che descrivano la struttura delle proteine che non potrebbero essere risolti sperimentalmente. Il modo più efficiente di predire la struttura, chiamato modellizzazione dell'omologia , si basa sull'esistenza di strutture modello note la cui sequenza è simile a quella della proteina oggetto di studio. L'obiettivo della genomica strutturale è fornire dati sufficienti sulle strutture risolte per consentire di delucidare quelle che rimangono da risolvere. Sebbene rimanga difficile modellare le strutture con precisione quando ci sono solo modelli strutturali distanti a cui fare riferimento, si ritiene che il nocciolo del problema risieda nell'allineamento delle sequenze perché si possono trovare modelli molto esatti. è conosciuto. Molte previsioni di strutture sono state utili al campo emergente dell'ingegneria delle proteine (in) , che includeva lo sviluppo di nuove modalità di ripiegamento . Un problema più complesso da risolvere mediante calcolo è la previsione delle interazioni intermolecolari, come la previsione dell'ancoraggio di molecole e delle interazioni proteina-proteina .
Il ripiegamento e il legame delle proteine possono essere simulati utilizzando tecniche come la meccanica molecolare , la dinamica molecolare e il metodo Monte Carlo , che beneficiano di un numero sempre maggiore di architetture informatiche di calcolo parallelo e distribuito , come il progetto Folding@home o la modellazione molecolare su un processore grafico . Il ripiegamento di piccoli domini proteici α-elica , come il cappuccio villinico e la proteina accessoria dell'HIV, è stato simulato con successo in silico e metodi ibridi che combinano dinamiche molecolari standard con elementi di meccanica quantistica hanno permesso l'esplorazione degli stati elettronici di rodopsina .
Proprietà
fenotipo
Il piano per produrre le proteine dipende quindi prima di tutto dal gene . Tuttavia, le sequenze dei geni non sono strettamente identiche da un individuo all'altro. Inoltre, nel caso di esseri viventi diploidi , ci sono due copie di ciascun gene. E queste due copie non sono necessariamente identiche. Un gene esiste quindi in diverse versioni da un individuo all'altro e talvolta nello stesso individuo. Queste diverse versioni sono chiamate alleli . L'insieme degli alleli di un individuo costituisce il genotipo .
Poiché i geni esistono in più versioni, anche le proteine esisteranno in versioni diverse. Queste diverse versioni di proteine causeranno differenze da un individuo all'altro, tale individuo avrà gli occhi azzurri ma come gli altri avranno gli occhi neri, ecc . Queste caratteristiche, visibili o meno, specifiche di ogni individuo sono chiamate fenotipo . Nello stesso individuo, un gruppo di proteine con una sequenza simile e una funzione identica si dice isoforma . Le isoforme possono essere il risultato dello splicing alternativo dello stesso gene, l'espressione di più alleli di un gene o la presenza di più geni omologhi nel genoma.
Evoluzione
Durante l' evoluzione , l'accumulo di mutazioni ha causato la divergenza dei geni all'interno e tra le specie . Da ciò deriva la diversità delle proteine ad esse associate. Tuttavia, è possibile definire famiglie di proteine, a loro volta corrispondenti a famiglie di geni. Quindi, in una specie geni molto simili, e quindi proteine, possono coesistere formando una famiglia. È probabile che due specie strettamente correlate abbiano rappresentanti della stessa famiglia di proteine.
Si parla di omologia tra proteine quando proteine diverse hanno un'origine comune, un gene ancestrale comune.
Il confronto delle sequenze di proteine permette di dimostrare il grado di “correlazione” tra proteine diverse, si parla qui di similarità di sequenza. La funzione delle proteine può divergere al diminuire della somiglianza, dando luogo a famiglie di proteine di origine comune ma con funzioni diverse.
L'analisi delle sequenze e delle strutture proteiche ha mostrato che molte si organizzano in domini , cioè parti che acquisiscono struttura e svolgono una funzione specifica. L'esistenza di proteine con più domini può essere il risultato della ricombinazione in un unico gene di più geni originariamente individuali, e viceversa proteine composte da un singolo dominio possono essere il risultato della separazione in più geni di un gene originariamente codificante un multi -proteina di dominio.
cibo umano
Durante la digestione , dallo stomaco, le proteine di origine vegetale, batterica, fungina o animale vengono scomposte ( idrolizzate ) dalle proteasi ; scomposto in polipeptidi e quindi in amminoacidi utili all'organismo , compresi gli amminoacidi essenziali (che l'organismo non è in grado di sintetizzare). Il pepsinogeno viene convertito in pepsina a contatto con l' acido cloridrico dello stomaco. La pepsina è l'unico enzima proteolitico che digerisce il collagene , la principale proteina del tessuto connettivo .
La digestione delle proteine avviene principalmente nel duodeno . Vengono assorbiti principalmente quando arrivano nel digiuno e solo l'1% delle proteine ingerite si trova nelle feci . Nelle cellule epiteliali dell'intestino rimangono alcuni amminoacidi , utilizzati per la biosintesi di nuove proteine, comprese le proteine intestinali che vengono costantemente digerite, riciclate e assorbite dall'intestino tenue .
La digeribilità delle proteine varia notevolmente a seconda della loro natura e della preparazione dell'alimento.
Quantità consigliate
L' ANSES raccomanda un apporto dietetico raccomandato (RDI) di 0,83 g · kg -1 · d -1 , per un massimo di 2,2 g · kg -1 · d -1 negli adulti in buona salute, 62 g al giorno per un uomo di 75 chilogrammi . Da notare che gli ANC sono superiori ai fabbisogni medi che sono 0,66 g · kg -1 · d -1 secondo questo stesso rapporto, che darebbero 49,5 g al giorno per il caso precedente.
I fabbisogni proteici medi sono stati definiti dalla FAO, che raccomanda 49 g di proteine per gli uomini adulti e 41 g per le donne (47 in gravidanza, 58,5 in allattamento).
Proteine animali, fungine, vegetali
Secondo l' American Heart Association , non è necessario consumare proteine animali per avere abbastanza proteine nella dieta: le proteine vegetali possono fornire abbastanza aminoacidi essenziali e non, a patto che le fonti di proteine alimentari siano varie e che il contenuto calorico l'assunzione è sufficiente per soddisfare il fabbisogno energetico. Non è necessario unirli nello stesso pasto. L' American Dietetic Association ricorda inoltre che le proteine vegetali possono soddisfare il fabbisogno proteico se la dieta della pianta è varia e soddisfa il fabbisogno energetico. Inoltre, “un assortimento di alimenti vegetali consumati nel corso di una giornata può fornire tutti gli amminoacidi essenziali e garantire una sufficiente ritenzione e utilizzo di azoto negli adulti sani, in modo che la combinazione proteica durante lo stesso pasto non sia necessaria. "
- Proteine animali : sono sempre accompagnate da lipidi saturi , il cui consumo è spesso eccessivo, e talvolta da additivi alimentari (come i nitriti dei salumi , sospettati di essere cancerogeni). Si ritiene che anche le proteine animali o prodotti associati come le ammine eterocicliche siano un fattore di rischio per alcuni tumori ( colon , vescica ). Dal 2015 l'OMS e l' IARC hanno classificato la carne rossa (maiale, bovina, ovina, equina e caprina) come probabile cancerogena e la carne lavorata come cancerogena accertata (34.000 decessi/anno in tutto il mondo, secondo uno studio del Global Burden of Disease Progetto ; secondo l'OMS: mangiare 50 grammi di carne lavorata al giorno aumenta del 18% il rischio di cancro del colon-retto (una carne si dice lavorata se ha subito salatura, maturazione, fermentazione, affumicatura o altri processi volti a migliorarne la sapore o la sua conservazione). Per mancanza di dati, il Gruppo di lavoro IARC non è stato in grado di classificare la carne cruda rispetto al rischio di cancro, ma ricorda che presenta un rischio infettivo avere inquinanti bioconcentrati attraverso la catena alimentare
- Proteine vegetali : gli effetti positivi sono associati alle piante ricche di proteine. I legumi sono ricchi di proteine, ma anche di fibre , minerali e portano una sensazione di sazietà per un basso indice glicemico. Il consumo di fagioli contribuisce ad abbassare i livelli di colesterolo e il rischio di incidenti cardiovascolari e alcuni tipi di cancro ( colon-rettale , prostata e pancreas ). Sono ovviamente un'alternativa per vegani o vegetariani. Noci, verdure, fagioli, quinoa e cereali contengono elevate quantità di proteine ma anche energia.
- Proteine fungine : i funghi commestibili sono spesso ricchi di proteine e, come le piante, sono fonti di fibre alimentari e minerali. D'altra parte, raccolte in natura o coltivate su substrati inquinati, tendono ad accumulare una grande quantità di metalli pesanti , metalloidi e persino radionuclidi .
Qualità delle proteine
Tutti gli amminoacidi necessari devono essere forniti dal cibo, pena la carenza, il che implica fonti proteiche diversificate.
La raccomandazione di combinare proteine animali e vegetali in ogni pasto è stata invalidata dal 1994 a seguito di un articolo di Vernon Young e Peter Pellett che è diventato un riferimento sul metabolismo proteico nell'uomo, confermando che la combinazione di proteine nel pasto è totalmente inutile. Le persone che non desiderano mangiare proteine animali non corrono il rischio di uno squilibrio aminoacidico delle proteine vegetali nella loro dieta. Molte proteine vegetali contengono poco meno di uno o più aminoacidi essenziali ( lisina soprattutto e in misura minore metionina e treonina ), senza che il consumo esclusivo di fonti di proteine vegetali impedisca di avere una dieta equilibrata in aminoacidi essenziali.
Le conclusioni dell'articolo di Young e Pellet sono da considerare solo nel caso molto generale in cui i cereali non sono la fonte esclusiva di cibo, che si preoccupano di specificare, inoltre, dove spiegano in altri articoli. Così in alcune regioni svantaggiate le razioni alimentari possono includere solo cereali, il che provoca seri problemi di salute ai bambini piccoli, ad esempio nelle famiglie povere dello stato del Madhya Pradesh in India (grano e riso).
Inoltre, le aziende sementiere stanno cercando di ottenere o hanno già ottenuto varietà di cereali con un contenuto di aminoacidi modificato ( OGM ), ad esempio il mais arricchito in lisina.
Le autorità sanitarie francesi (AFSSA/ ANSES ) si rifiutano ancora di dirimere questa questione.
Integratori alimentari
Gli integratori alimentari proteici esistono per gli atleti che desiderano sviluppare il proprio volume muscolare e per le persone con carenze proteiche. Le proteine utilizzate sono spesso proteine ottenute da erba medica (erba medica sotto forma di estratto di foglie (EFL) ) , fave , piselli o siero di latte (sotto il nome di "siero di latte"), e aminoacidi ramificati designati con il nome di "BCAA" .
Cibi ricchi di proteine
- I funghi hanno un contenuto proteico difficile da misurare con precisione (contenuti in precedenza sopravvalutati dal 70 al 200% a volte) ma spesso relativamente elevato (dal 15 al 35% del peso secco del fungo), molto superiore ai cereali come frumento e mais, di interesse alimentare. Questi livelli sono paragonabili a quelli dei legumi come piselli e lenticchie.
Gli amminoacidi essenziali rappresentano spesso una quota significativa di queste proteine ( es. 61,8 e 63,3% dei livelli di amminoacidi totali rispettivamente in Tricholoma portentosum e Tricholoma terreum (in cui la leucina , l' isoleucina e il triptofano sono gli amminoacidi limitanti) I punteggi degli aminoacidi corretti (PDCAAS) delle proteine di questi due funghi sono bassi rispetto a quelli di caseina, albume d'uovo e soia, ma superiori a quelli di molte proteine vegetali.Il contenuto di grassi era basso (5,7% per Tricholoma porterosum e 6,6 % per Tricholoma terreum ) in entrambe le specie, con acidi oleico e linoleico che rappresentano oltre il 75% degli acidi grassi
totali.Alcuni come il fungo de Paris (3,09 g di proteine per 100 g ) sono stati a lungo coltivati ed essiccati, ma individualmente ( come altri alimenti) possono essere carenti di alcuni amminoacidi ( es. amminoacidi contenenti zolfo, metionina e cistina nel caso dei funghi ostrica ad esempio) ma sono ricchi di lisina e leucina che mancano ad esempio nei cereali. Si stanno ancora scoprendo virtù ( es: una di queste proteine sembra inibire nei topi le allergie alimentari ) e difetti ( es: un'altra proteina fungina si è dimostrata cardiotossica ).
- Gli alimenti di origine animale sono generalmente più proteici di quelli di origine vegetale, ed in particolare le uova (ricche di albumina) o i formaggi (caseina, ecc.), come il parmigiano, ad esempio, che contiene 39,4 g/100 g, più della carne e pesce. Oltre ad alcune carni ( es: petto di pollo cotto con un contenuto medio di 29,2 g/100 g) come il manzo che ne contiene 26 g/100 g, anche pesci come il tonno alalunga o le sardine contengono circa 30 g/100 g. Le uova sono anche una fonte di proteine (24 g/100 g per quattro uova).
- Certe piante o semi sono molto ricchi di proteine: olio di semi ( mandorle , pistacchi , lino , ecc ) e legumi ( ceci , fagioli , lenticchie , ecc ). Così 100 g di prodotto crudo contengono una quota proteica di: 58 g per la spirulina , 38 g per i semi di soia , 30 g per i semi di zucca , 25 g per i fagioli neri , 24 g per le lenticchie , 21 g per il seitan (glutine) e la frutta secca , 20 g per mandorle e semolino , 15 g per avena , 15 g per riso selvatico, 14 g per quinoa .
- I lieviti , i batteri e i cianobatteri raramente vengono coltivati per essere mangiati direttamente, ma il lievito o la Spirulina (58 g di proteine per 100 g di spirulina) sono molto ricchi di proteine.
Note e riferimenti
- Scoperte di proteine
- Gregory A. Petsko e Dagmar Ringe ( trad . dall'inglese), Struttura e funzione delle proteine , Bruxelles, De Boek Universitynovembre 2008, 190 pag. ( ISBN 978-2-8041-5888-0 , leggi online )
- (in) Alex Gutteridge e Janet M. Thornton , " Capire il kit di strumenti catalitici della natura " , Trends in Biochemical Sciences , vol. 30, n . 11,novembre 2005, pag. 622-629 ( PMID 16214343 , DOI 10.1016 / j.tibs.2005.09.06 , leggi online )
- (in) Harvey Lodish, Arnold Berk, Paul Matsudaira, Chris A. Kaiser, Monty Krieger, Matthew P. Scott, Lawrence Zipursky e James Darnell, biologia cellulare molecolare , New York, WH Freeman & Company 5 ° edizione,agosto 2003, 973 pag. ( ISBN 978-0-7167-4366-8 )
- Garcia Martin S (2015) Nanoproteine dinamiche: autoassemblaggio di peptidi su nanoparticelle d'oro monostrato protette
- Mitch Leslie (2019) Impatto fuori misura ; | Scienza 18 ottobre 2019: Vol. 366, Numero 6463, pp. 296-299 | DOI: 10.1126 / science.366.6463.296 ( riassunto )
- Staudt, AC, & Wenkel, S. (2011). Regolazione della funzione proteica da parte delle "microproteine" . Rapporti EMBO, 12 (1), 35-42.
- (Wang et al (2009)
- zhang et al, 2009)
- (in) Zhaohui Xu, Arthur L. Horwich e Paul B. Sigler , " La struttura cristallina dell'asimmetrico GroEL-GroES- (ADP) 7complesso chaperonin ” , Nature , vol. 388, n . 6644,21 agosto 1997, pag. 741-750 ( PMID 9285585 , DOI 10.1038 / 41944 , leggi online )
- (in) Lisa J Harris, Eileen Skaletsky e Alexander McPherson , " Struttura cristallografica di un anticorpo monoclonale IgG1 intatto " , Journal of Molecular Biology , vol. 275, n . 5,6 febbraio 1998, pag. 861-872 ( PMID 9480774 , DOI 10.1006 / jmbi.1997.1508 , leggi online )
- (in) W. Bolton e MF Perutz , " Sintesi di Fourier tridimensionale della deossiemoglobina di cavallo a 2,8 Risoluzione " , Nature , vol. 228, n ° 5271,7 novembre 1970, pag. 551-552 ( PMID 5472471 , DOI 10.1038 / 228551a0 , Bibcode 1970Natur.228..551B , leggi online )
- (in) Edward N. Baker, Thomas L. Blundell, John F. Cutfield, Susan M. Cutfield, Eleanor J. Dodson, Guy G. Dodson, Dorothy Crowfoot Hodgkin Mr. Roderick E. Hubbard, Neil W. Isaacs, Colin D. Reynolds, Kiwako Sakabe, Norioshi Sakabe e Numminate M. Vijayan , " La struttura dei cristalli di insulina di maiale 2Zn a una risoluzione di 1,5 " , Philosophical Transactions B , vol. 319, n . 11956 luglio 1988, pag. 369-456 ( PMID 2905485 , DOI 10.1098 / rstb.1988.0058 , Bibcode 1988RSPTB.319..369B , leggi online )
- (it) Michael B. Berry e George N. Phillips Jr. , " Strutture cristalline di Bacillus stearothermophilus adenilato chinasi con Ap 5 A legato , Mg 2+ Ap 5 A e Mn 2+ Ap 5 Arivelano una posizione palpebrale intermedia e sei coordinate geometriche ottaedriche per Mg 2+ e Mn 2+ legati " , Proteins: Structure, Function, and Bioinformatics , vol. 32, n . 3,15 agosto 1998, pag. 276-288 ( PMID 9715904 , leggi online )
- (in) Harindarpal S. Gill e David Eisenberg , " La struttura cristallina della fosfinotricina nel sito attivo della glutammina sintetasi illumina il meccanismo dell'inibizione enzimatica " , Biochimica , vol. 40, n ° 7,20 febbraio 2001, pag. 1903-1912 ( PMID 11329256 , DOI 10.1021/bi002438h , leggi online )
- (in) Wojciech R. Rypniewski Hazel Holden e Ivan Rayment , " Conseguenze strutturali della metilazione riduttiva dei residui di lisina nel lisozima dell'albume d'uovo di gallina: un'analisi a raggi X con risoluzione 1,8-Å " , Biochimica , vol. 32, n ° 37,21 settembre 1993, pag. 9851-9858 ( PMID 8373783 , DOI 10.1021/bi00088a041 , leggi online )
- (in) Tamir Gonen Yifan Cheng, Piotr Sliz, Yoko Hiroaki Yoshinori Fujiyoshi, Stephen C. Harrison e Thomas Walz , " Interazioni lipide-proteina in cristalli bidimensionali a doppio strato AQP0 " , Nature , vol. 438, n ° 7068,1 ° dicembre 2005, pag. 633-638 ( PMID 16319884 , PMCID 1350984 , DOI 10.1038/nature04321 , leggi online )
- (in) Daron M. Standley, Akira R. Kinjo, Kengo Kinoshita e Haruki Nakamura , " Banche dati sulla struttura delle proteine con nuovi servizi web per la biologia strutturale e la ricerca biomedica " , Briefings in Bioinformatics , vol. 9, n ° 4,luglio 2008, pag. 276-285 ( PMID 18430752 , DOI 10.1093/bib/bbn015 , leggi online )
- (in) Peter Walian, Timothy A Cross K e Bing Jap , " Genomica strutturale delle proteine di membrana " , Genome Biology , vol. 5, n ° 4,2004, pag. 215 ( PMID 15059248 , PMCID 395774 , DOI 10.1186 / gb-2004-5-4-215 , leggi online )
- (in) Roy D. Sleator , " Previsione delle funzioni proteiche " , Metodi in biologia molecolare , vol. 815,2012, pag. 15-24 ( PMID 22130980 , DOI 10.1007 / 978-1-61779-424-7_2 , leggi online )
- Forchhammer K, Bock A, “ Selenocisteina sintasi da Escherichia coli. Analisi della sequenza di reazione ”, J. Biol. chimica , vol. 266, n . 10,1991, pag. 6324-8 ( PMID 2007585 )
- (in) Yuhei Araiso, Sotiria Palioura, Ryuichiro Ishitani, R. Lynn Sherrer, Patrick O'Donoghue, Jing Yuan, Hiroyuki Oshikane, Naoshi Domae Julian DeFranco, Dieter Söll e Osamu Nureki , " Approfondimenti strutturali sugli archaeal RNA-dipendenti ed eucaristici formazione di selenocisteina ” , Ricerca sugli acidi nucleici , vol. 36, n . 4,marzo 2008, pag. 1187-1199 ( PMID 18158303 , PMCID 2275076 , DOI 10.1093/nar / gkm1122 , leggi online )
- (in) Sotiria Palioura R. Lynn Sherrer, Thomas A. Steitz Dieter Söll e Miljan Simonovic , " Il complesso umano SepSecS-tRNA Sec rivela il meccanismo dell'educazione alla selenocisteina " , Science , vol. 325, n . 5938,17 luglio 2009, pag. 321-325 ( PMID 19608919 , PMCID 2857584 , DOI 10.1126 / science.1173755 , Bibcode 2009Sci ... 325..321P , leggi online )
- (in) Alice B. Fulton e William B. Isaacs , " Titina, una proteina sarcomerica enorme ed elastica con un probabile ruolo nella morfogenesi " , BioEssays , vol. 13, n . 4,aprile 1991, pag. 157-161 ( PMID 1859393 , DOI 10.1002 / bies.950130403 , leggi online )
- (in) " Titin (CE 2.7.11.1) (Connectin) Mus musculus (Mouse) " su ProtParam su ExPASy (accede 9 maggio 2015 )
- (in) Thomas Bruckdorfer Oleg Marder e Fernando Albericio , " Dalla produzione di peptidi in quantità di milligrammi per la ricerca alle quantità multitonali per i farmaci del futuro " , Current Pharmaceutical Biotechnology , vol. 5, n ° 1,febbraio 2004, pag. 29-43 ( PMID 14965208 , DOI 10.2174 / 1389201043489620 , leggi online )
- (in) Dirk Schwarzer e Philip A Cole , " Semisintesi proteica e legatura proteica espressa: inseguire la coda di una proteina " , Current Opinion in Chemical Biology , vol. 9, n . 6,dicembre 2005, pag. 561-569 ( PMID 16226484 , DOI 10.1016 / j.cbpa.2005.09.018 , leggi online )
- (in) Stephen BH Kent , " sintesi chimica totale delle proteine " , Chemical Society Reviews , vol. 38, n . 2febbraio 2009, pag. 338-351 ( PMID 19169452 , DOI 10.1039/B700141J , leggi online )
- (in) R. Sankaranarayanan e D. Moras , " La fedeltà della traduzione del codice genetico " , Acta Biochimica Polonica , vol. 48, n . 22001, pag. 323-335 ( PMID 11732604 , leggi online )
- (in) John A. Copland, Melinda Sheffield-Moore, Nina Koldzic-Zivanovic, Sean Gentry, George Lamprou, Fotini Tzortzatou-Stathopoulou Vassilis Zoumpourlis, Randall J. Urban e Spiros A. Vlahopoulos , " Recettori degli steroidi sessuali nella differenziazione scheletrica e neoplasia epiteliale: è possibile un intervento tessuto-specifico? ” , BioEssays , vol. 31, n . 6,giugno 2009, pag. 629-641 ( PMID 19382224 , DOI 10.1002 / bies.200800138 , leggi online )
- (in) Stanislav Samarin e Asma Nusrat , " Regolazione del complesso giunzionale apicale epiteliale da parte della famiglia Rho GTPases " , Frontiers in Bioscience , vol. 14,gennaio 2009, pag. 1129-1142 ( PMID 19273120 , DOI 10.2741/3298 , leggi online )
- (in) Ida Schomburg Antje Chang, Sandra Placzek Carola Söhngen, Michael Rother, Maren Lang, Cornelia Munaretto Susanne Ulas, Michael Stelzer, Andreas Grote, Maurice Scheer e Dietmar Schomburg , " BRENDA nel 2013: reazioni integrate, dati cinetici, funzione enzimatica dati, classificazione delle malattie migliorata: nuove opzioni e contenuti in BRENDA ” , Nucleic Acids Research , vol. 41, n o D1,Gennaio 2013, D764-D772 ( PMID 23203881 , DOI 10.1093/nar/gks1049 , leggi online )
- (in) A. e R. Radzicka Wolfenden , " Un abile enzima " , Science , vol. 267, n . 5194,6 gennaio 1995, pag. 90-93 ( PMID 7809611 , DOI 10.1126 / science.7809611 , leggi online )
- (in) Brian P. Callahan e Brian G. Miller , " OMP decarboxylase-An enigma Persists " , Bioorganic Chemistry , vol. 35, n . 6, dicembre 2007, pag. 465-469 ( PMID 17889251 , DOI 10.1016 / j.bioorg.2007.07.004 , leggi online )
- (in) Harold Rudiger, Hans-Christian Siebert, Dolores Solis, l'iniziale di Gesù Jimenez-Barbero, Antonio Romero, Claus-Wilhelm von der Lieth, Teresa Diaz-Maurino e Hans-Joachim Gabius , " Chimica medicinale basata sul codice dello zucchero: Fondamenti di lectinologia e strategie sperimentali con le lectine come bersagli ” , Current Medicinal Chemistry , vol. 7, n ° 4,aprile 2000, pag. 389-416 ( PMID 10702616 , DOI 10.2174 / 0929867003375164 , leggi online )
- Da Nobel, JG, Klis, FM, Priem, J., Munnik, T., & Van Den Ende, H. (1990) Le mannoproteine solubili in glucanasi limitano la porosità della parete cellulare in Saccharomyces cerevisiae . Lievito, 6 (6), 491-499.
- Zlotnik, HINDA, Fernandez, MP, Bowers, BLAIR, & Cabib, ENRICO (1984). Le mannoproteine di Saccharomyces cerevisiae formano uno strato esterno della parete cellulare che determina la porosità della parete . Giornale di batteriologia, 159 (3), 1018-1026.
- Caridi A (2006) Funzioni enologiche delle mannoproteine parietali di lievito. Antonie Van Leeuwenhoek, 89 (3-4), 417-422 ( riassunto )
- Harvey Lodish , Arnold Berk , Paul Matsudaira , Chris A. Kaiser , Monty Krieger , Matthew P. Scott , S. Laurence Zipursky e James Darnell ( trad. Pierre L. Masson e Chrystelle Sanlaville), Biologia molecolare della cellula ["Molecular Biologia cellulare ”], Bruxelles, Università De Boeck,2005, 3 e ed. , 1096 pag. [ dettaglio edizione ] ( ISBN 2-8041-4802-5 )
- (in) Julie Hey, Anton Posch, Andrew Cohen, Liu Ning e Adrianna Harbers , " Fractionation of Complex Protein Mixtures by Liquid-Phase Isoelectric Focusing " , Methods in Molecular Biology , vol. 424,2008, pag. 225-239 ( PMID 18369866 , DOI 10.1007 / 978-1-60327-064-9_19 , leggi online )
- (in) K. Terpe , " Panoramica sulle fusioni di proteine tag: dai fondamenti molecolari e biochimici ai sistemi di scambio " , Microbiologia applicata e biotecnologia , vol. 60, n . 5,gennaio 2003, pag. 523-533 ( PMID 12536251 , DOI 10.1007 / s00253-002-1158-6 , leggi online )
- (in) Olesya V. Stepanenko, Vladislav V. Verkhusha Irina Kuznetsova Mr. Vladimir N. Uversky e KK Turoverov , " Proteine fluorescenti come biomarcatori e biosensori: lanciare luci colorate sui processi molecolari e cellulari " , Current Protein & Peptide Science , vol . 9, n ° 4,agosto 2008, pag. 338-369 ( PMID 18691124 , PMCID 2904242 , DOI 10.2174 / 138920308785132668 , leggi online )
- (in) Rafael Yuste , " La microscopia a fluorescenza oggi " , Nature Methods , vol. 2, n . 12,dicembre 2005, pag. 902-904 ( PMID 16299474 , DOI 10.1038 / nmeth1205-902 , leggi online )
- (in) William Margolin , " Proteina fluorescente verde come reporter per la localizzazione macromolecolare nelle cellule batteriche " , Metodi , vol. 20, n ° 1,gennaio 2000, pag. 62-72 ( PMID 10610805 , DOI 10.1006 / meth.1999.0906 , leggi online )
- (in) Terry M. Mayhew e John M. Lucocq , " Sviluppi nella biologia cellulare per la microscopia immunoelettronica quantitativa basata su sezioni sottili: una revisione " , Istochimica e biologia cellulare , vol. 130, n . 2agosto 2008, pag. 299-313 ( PMID 18553098 , PMCID 2491712 , DOI 10.1007 / s00418-008-0451-6 , leggi online )
- (in) Angelika Görg, Walter Weiss e Michael J Dunn , " La tecnologia attuale dell'elettroforesi bidimensionale per la proteomica " , Proteomica , vol. 4, n . 12,dicembre 2004, pag. 3665-3685 ( PMID 15543535 , DOI 10.1002 / pmic.200401031 , leggi online )
- (in) P. e S. Conrotto Souchelnytskyi , " Approcci proteomici nelle scienze biologiche e mediche: principi e applicazioni " , Sperimentale Oncologia , vol. 30, n . 3,settembre 2008, pag. 171-180 ( PMID 18806738 )
- (in) T. J. Joos e Bachmann , " Microarray proteici: potenziali e limitazioni " , Frontiers in Bioscience , Vol. 14,gennaio 2009, pag. 4376-4385 ( PMID 19273356 , DOI 10.2741 / 3534 )
- (in) Manfred Koegl e Peter Uetz , " Migliorare i sistemi di screening dei due ibridi di lievito " , Briefings in Functional Genomics , vol. 6, n ° 4,dicembre 2007( PMID 18218650 , DOI 10.1093/bfgp / elm035 , bfg.oxfordjournals.org/content/6/4/302.full.pdf+html)
- (in) Dariusz e Krzysztof Ginalski Plewczyński , " L'interattoma: predire le interazioni proteina-proteina nelle cellule " , Lettere di biologia cellulare e molecolare , vol. 14, n ° 1,marzo 2009, pag. 1-22 ( PMID 18839074 , DOI 10.2478 / s11658-008-0024-7 , leggi online )
- (in) Chao Zhang e Sung-Hou Kim , " Panoramica della genomica strutturale: dalla struttura alla funzione " , Current Opinion in Chemical Biology , vol. 7, n ° 1, febbraio 2003, pag. 28-32 ( PMID 12547423 , DOI 10.1016 / S1367-5931 (02) 00015-7 , leggi online )
- (in) Yang Zhang , " Progressi e sfide nella previsione della struttura proteica " , Current Opinion in Structural Biology , vol. 18, n . 3, giugno 2008, pag. 342-348 ( PMID 18436442 , PMCID 2680823 , DOI 10.1016 / j.sbi.2008.02.004 , leggi online )
- (in) Zhexin Xiang , " Advances in Protein Structure Modeling Homology " , Current Protein & Peptide Science , vol. 7, n . 3, giugno 2006, pag. 217-227 ( PMID 16787261 , PMCID 1839925 , DOI 10.2174 / 138920306777452312 # sthash.hup2vFsH.dpuf , leggi online )
- (in) Yang Zhang e Jeffrey Skolnick , " Il problema di previsione della struttura proteica potrebbe essere risolto utilizzando l'attuale libreria PDB " , Atti della National Academy of Sciences degli Stati Uniti d'America , vol. 102, n . 4, 25 gennaio 2005, pag. 1029-1034 ( PMID 15653774 , PMCID 545829 , DOI 10.1073/pnas.0407152101 , leggi online )
- (in) Brian Kuhlman, Gautam Dantas, Gregory C. Ireton, Gabriele Varani, Barry L. Stoddard e David Baker , " Design of a Novel Globular Protein Fold with Atomic-Level Accuracy " , Science , vol. 302, n ° 5649, 21 novembre 2003, pag. 1364-1368 ( PMID 14631033 , DOI 10.1126 / science.1089427 , leggi online )
- (in) David W. Ritchie , " Progressi recenti e direzioni future nel docking proteina-proteina " , Current Protein & Peptide Science , vol. 9, n ° 1, febbraio 2008, pag. 1-15 ( PMID 18336319 , DOI 10.2174 / 138920308783565741 , leggi online )
- (in) T. Herges e W. Wenzel , " In Silico Folding of a Three Helix Protein e caratterizzazione del suo paesaggio di energia libera in un campo di forza di tutti gli atomi " , Physical dreamed Letters , vol. 94, n . 1, 14 gennaio 2005, pag. 018101 ( PMID 15698135 , DOI 10.1103 / PhysRevLett.94.018101 , Bibcode 2005PhRvL..94a8101H , leggi online )
- (in) Michael Hoffmann, Marius Wanko Paul Strodel, Peter H. König, Thomas Frauenheim Klaus Schulten, Walter Thiel, Emad Tajkhorshid e Marcus Elstner , " Color Tuning in rhodopsins: The Mechanism for the Spectral Shift entre Bacteriorhodopsin and Sensory Rhodopsin II " , Journal of American Chemical Society , vol. 128, n . 33, 23 agosto 2006, pag. 10808-10818 ( PMID 16910676 , DOI 10.1021/ ja062082i , leggi online )
- Le proteine
- " Guida all'alimentazione familiare " (consultato il 26 novembre 2014 )
- (en-US) American Heart Association , " Dieta vegetariana, vegana e salute del cuore " , Go Red For Women® ,26 marzo 2014( letto online , consultato il 29 luglio 2017 )
- (in) " Posizione dell'American Dietetic Association: Vegetarian Diets " , Journal of American Dietetic Association ,luglio 2009, pag. 1267–1268 ( leggi online )
- Studio sulla salute avventista-1 - Risultati sul cancro: alcuni punti salienti
- OMS comunicato stampa cancerogenicità del consumo di carne rossa e carni lavorate ottobre 2015]
- Modulo Dry Bean sul sito Web del passaporto sanitario
- Il consumo di legumi diversi dalla soia riduce i livelli di colesterolo: una meta-analisi di studi randomizzati controllati
- Consumo di legumi e rischio di malattia coronarica negli uomini e nelle donne statunitensi: studio di follow-up epidemiologico NHANES I
- V. R. Young e PL Pellett , “ Le proteine vegetali in relazione alla nutrizione delle proteine umane e degli aminoacidi ”, The American Journal of Clinical Nutrition , vol. 59, n . 5 Supplemento,maggio 1994, pag. 1203S – 1212S ( ISSN 0002-9165 , PMID 8172124 , lettura online , accesso 29 luglio 2017 )
- (in) VR Young e PL Pellett , " Le proteine del grano in relazione al fabbisogno proteico e alla disponibilità di aminoacidi " , The American Journal of Clinical Nutrition , vol. 41, n . 5,1 ° maggio 1985, pag. 1077–1090 ( ISSN 0002-9165 e 1938-3207 , DOI 10.1093/ajcn/41.5.1077 , lettura online , accesso 4 febbraio 2020 )
- Sophie Landrin, " In India la religione si autoinvita nel piatto degli scolari " , su Le Monde ,4 febbraio 2020(consultato il 4 febbraio 2020 )
- " I campi di applicazione della transgenesi " , sulla pedagogia gnis (consultato il 5 febbraio 2020 )
- " STATI UNITI - Un mais arricchito in lisina " , su inf'OGM ,novembre 2005(consultato il 5 febbraio 2020 )
- Rapporto AFSSA/ANSES, pagg. 232 e 233
- Il contenuto proteico dei funghi è difficile da misurare proprio perché la loro chitina e altri composti azotati interferiscono con l'analisi dell'azoto totale (es. metodo di Kjeldahl ) precedentemente utilizzato. Fonte: Danell E. e Eaker D. (1992), Aminoacido e contenuto proteico totale del fungo commestibile Cantharellus cibarius (Fries) , Journal of the Science of Food and Agriculture , 60 (3), 333-337.
- Dıez VA e Alvarez A. (2001), Studi compositivi e nutrizionali su due funghi commestibili selvatici del nord-ovest della Spagna , Chimica degli alimenti , 75 (4), 417-422 ( riassunto )
- Chang ST e Buswell JA (1996), gli integratori alimentari funghi , World Journal of Microbiology e delle biotecnologie , 12 (5), 473-476 ( abstract ).
- Peter CK Cheung (2009), Valore nutrizionale e benefici per la salute dei funghi, funghi come alimenti funzionali , (71-109).
- (en) VA Dı́ez e A. Alvarez, Studi compositivi e nutrizionali su due funghi commestibili selvatici del nord-ovest della Spagna . In Chimica Alimentare . Fascia 75, n . 4, dicembre 2001, S. 417-422, DOI : 10.1016 / S0308-8146 (01) 00229-1
- Chang ST e Miles PG (1991), Recenti tendenze nella produzione mondiale di funghi commestibili , The Mushroom Journal , 503, 15-18.
- Shah H., Khalil IA e Jabeen S. (1997), Composizione nutrizionale e qualità proteica del fungo Pleurotus , Sarhad Journal of Agriculture (Pakistan) ( Riassunto Agris/FAO ).
- Hsieh, KY, Hsu, CI, Lin, JY, Tsai, CC e Lin, RH (2003), La somministrazione orale di una proteina derivata da funghi commestibili inibisce lo sviluppo di reazioni allergiche al cibo nei topi , Allergia clinica e sperimentale , 33 (11), 1595-1602 ( riassunto )
- Lin, JY, Lin, YJ, Chen, CC, Wu, HL, Shi, GY e Jeng, TW (1974), Proteina cardiotossica da funghi commestibili , Nature , 252 (5480), 235 ( riassunto ).
- " Tabella Ciqual di composizione nutrizionale degli alimenti " , su ciqual.anses.fr (consultato il 10 settembre 2018 )
- Albert-François Creff e Daniel Layani, Manuale di dietetica nella pratica medica attuale , Parigi, Masson,2004, 301 pag. ( ISBN 978-2-294-01346-1 , leggi in linea ) , p. 4
Vedi anche
Bibliografia
- Gregory Petsko, Dagmar Ringe (trad. Chrystelle Sanlaville, Dominique Charmot-Bensimon), Struttura e funzione delle proteine , De Boeck, Bruxelles, 2009. ( ISBN 978-2-8041-5888-0 ) .
- Lubert Stryer, Jeremy Mark Berg, John L. Tymoczko (trad. Serge Weinman), Biochimica , Flammarion, "Medicine-Sciences", Paris, 2008, 6 ° ed. ( ISBN 978-2-257-00003-3 ) .
- Carl-Ivar Brändén, John Tooze (trad. Bernard Lubochinsky, pref. Joël Janin), Introduzione alla struttura delle proteine , Università De Boeck, Bruxelles, 1996. ( ISBN 978-2-8041-2109-9 ) .
Articoli Correlati
- Combinazione di proteine (cibo - esempio: riso/lenticchie)
- Proteine ricombinanti
- Sottofamiglia di proteine
- Aggregazione proteica
- acquaporina
- Proteine Rieske
- Trasportatore di aminoacidi lisosomiali
- proteine fibrose
- Proteina globulare
- Viciline
- fattori di trascrizione
- proteine Cdx
- Proteine da impalcatura
- proteina tau
- tioproteina
- Selenoproteina
- mannoproteine
- Microproteina
link esterno
- ( fr ) Progetto Predictor Un software di calcolo condiviso che utilizza la piattaforma BOINC per studiare il ripiegamento delle proteine.
- (it) Server MRS Un server di banca dati biologica, dove l'identificazione di una voce nella banca PDB permette di visualizzare la struttura a video, in modalità dinamica (si veda ad esempio cosa una ricerca nella banca produce PDB delle voci corrispondenti alla tripsina).
- ( fr ) Proteins @ home Un progetto su larga scala per studiare il ripiegamento delle proteine, a cui puoi partecipare con il tuo computer.