Istone
Istone H2A / H2B / H3 / H4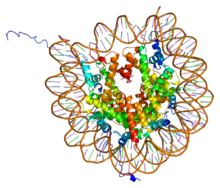 Rappresentazione del complesso formato da una particella nucleosomica (h3, h4, h2a, h2b) e un frammento di DNA lungo 146 paia di basi ( PDB 1AOI ).
Rappresentazione del complesso formato da una particella nucleosomica (h3, h4, h2a, h2b) e un frammento di DNA lungo 146 paia di basi ( PDB 1AOI ).
| Pfam | PF00125 |
|---|---|
| Clan Pfam | CL0012 |
| InterPro | IPR007125 |
| SCOP | 1 ora |
| SUPERFAMIGLIA | 1 ora |
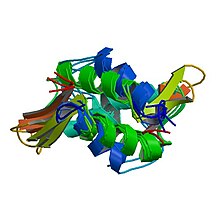 Struttura dell'istone HIST1H1B (en) ( PDB 1GHC )
Struttura dell'istone HIST1H1B (en) ( PDB 1GHC )
| Pfam | PF00538 |
|---|---|
| InterPro | IPR005818 |
| INTELIGENTE | SM00526 |
| SCOP | 1hst |
| SUPERFAMIGLIA | 1hst |
Gli istoni sono proteine situate nel nucleo delle cellule eucariote e negli archaea . Sono i principali costituenti proteici dei cromosomi . Sono infatti strettamente associati al DNA di cui consentono la compattazione, questa azione formando strutture chiamate nucleosomi : il DNA è avvolto attorno agli istoni come filo attorno ad una bobina. Gli istoni sono molto ricchi di aminoacidi basici ( lisina e arginina ), la cui carica positiva a pH fisiologico consente una forte interazione con i gruppi fosfato del DNA portatori di cariche negative.
Struttura
Gli istoni sono piccole proteine basiche con una massa molecolare compresa tra 13 e 15 kDa. Sono caratterizzati da un dominio C-terminale globulare, il dominio della piega istonica . Questo dominio, molto conservato dagli archei agli eucarioti superiori, è costituito da tre eliche α separate da due brevi anelli. Consente la dimerizzazione degli istoni in un cosiddetto modello di stretta di mano , che funge da base per l'assemblaggio del nucleosoma .
Il dominio della piega istonica si trova in molte proteine diverse dagli istoni e definisce la famiglia di proteine note come simili agli istoni .
L'N-terminale degli istoni non è strutturato e sporge all'esterno del DNA nel nucleosoma assemblato. Queste estremità sono accessibili agli enzimi modificanti .
Diversi tipi di istoni
Gli istoni comprendono cinque classi di proteine, raggruppate in due categorie in base al loro ruolo nella formazione del nucleosoma:
- gli istoni delle classi H2A , H2B, H3 e H4 costituiscono gli istoni “core”, così chiamati perché formano la particella core del nucleosoma: due istoni di ciascuna classe si associano in un ottamero attorno al quale il doppio filamento di DNA circa 150 coppie di basi;
- gli istoni della classe H1 sono i cosiddetti istoni “leganti”: un istone di questa classe lega il DNA nel punto in cui entra ed esce dalla particella centrale, e quindi “sigilla” il nucleosoma.
Ogni classe comprende diversi sottotipi (eccetto la classe H4) distinti in base al loro profilo di espressione:
- sottotipi la cui espressione è accoppiata alla replicazione del DNA;
- sottotipi la cui espressione è indipendente dalla replicazione del DNA;
- sottotipi espressi specificamente in determinati tessuti o in determinati stadi di sviluppo.
Nelle cellule cicliche, i sottotipi la cui espressione è accoppiata alla replicazione predominano nella cromatina, motivo per cui sono chiamati istoni convenzionali o canonici . Al contrario, gli altri sottotipi sono indicati come "varianti istoniche" ; generalmente rappresentano meno del 10% degli istoni totali nelle cellule cicliche, ma questa proporzione può raggiungere il 50% nelle cellule differenziate.
I geni che codificano gli istoni convenzionali sono solitamente presenti nel genoma in più copie organizzate in cluster - per esempio negli esseri umani, tre cluster sui cromosomi 1 e 6; nei topi, tre cluster sui cromosomi 3, 11 e 13. Presentano caratteristiche atipiche per i geni eucariotici, come l'assenza di introni e la terminazione della trascrizione segnalata da una struttura stelo-loop invece che da un segnale di poliadenilazione . Al contrario, i geni che codificano le varianti istoniche sono presenti solo in una o due copie e sono distribuiti isolatamente in tutto il genoma; Hanno tutti almeno un introne e un segnale di poliadenilazione.
Istone e condensazione del DNA
Ci sono circa cinquantaquattro coppie di basi tra due nucleosomi, questo valore varia a seconda della specie (ad esempio, ce ne sono centosessantacinque per il lievito ). Il livello successivo di compattazione del DNA coinvolge altre cosiddette proteine " non istoniche " . "
Il grado di condensazione del DNA attorno ai nucleosomi istonici e alle proteine non istoniche è variabile lungo i cromosomi , nella cromatina . È a basso contenuto di eucromatina cosiddetta "aperta" ed è accessibile al macchinario della RNA polimerasi . È ricco di eterocromatina , che si dice sia "chiusa" e "inaccessibile" al meccanismo di trascrizione .
Questo grado di condensazione è regolato da modifiche delle estremità N-terminali degli istoni, come fosforilazioni , acetilazioni , metilazioni , ubiquitinazioni , sumoilazioni , ecc. tutte queste modificazioni sono catalizzate da enzimi specifici. Le modificazioni covalenti degli istoni agirebbero o direttamente modificando la compattazione dell'avvolgimento del DNA attorno ai nucleosomi, oppure indirettamente costituendo "segni" che permettessero il reclutamento di proteine in grado di modificare la struttura della cromatina . Il modello delle modifiche covalenti degli istoni che agiscono come un codice (il "codice istonico") è stato proposto da Strahl e Allis nel 2000 sulla rivista Nature . Tuttavia, questo codice sembra essere lungi dall'essere universale e piuttosto relativamente specifico a seconda dei geni e delle cellule considerate.
Codice istonico
Il codice dell'istone stabilisce un collegamento diretto tra la modifica di alcuni residui della coda dell'istone che crea legami per gli effettori delle proteine e lo stato trascrizionale delle cromatine .
Una modifica dell'istone può influenzarne un'altra in modo sinergico o antagonistico; è un meccanismo che genera e stabilizza specifiche impronte digitali.
L' acetilazione (aggiunta del gruppo acetile) viene effettuata su enzimi specifici attraverso residui di lisina denominati istone acetil transferasi (HAT).
Generalmente diminuisce l'interazione inter-nucleosomica e tra le code degli istoni e il frammento di DNA che costituisce il collegamento tra i nucleosomi. Questo porta al rilassamento della cromatina, facendola passare allo stato eucromatinale, e quindi consente una migliore accessibilità ad altri fattori. L'acetilazione è associata all'attivazione della trascrizione ed è facilmente reversibile attraverso l'azione delle istone deacetilasi (HDAC).
La metilazione , a sua volta, può essere eseguita sia su lisina che su arginina e può consistere nell'aggiunta di uno, due o tre gruppi metilici.
A seconda dei residui metilati e del numero di gruppi aggiunti, è associato all'attivazione o alla repressione della trascrizione. A lungo considerata statica, la metilazione dell'istone si è dimostrata una modifica reversibile coinvolta in un processo dinamico, sebbene più stabile dell'acetilazione e della fosforilazione. È stato identificato un numero crescente di istoni demetilasi.
In generale, questi due tipi di modifiche sono antagoniste e la deacetilazione delle lisine deve precedere la loro metilazione. Questo antagonismo porta alla creazione di un certo equilibrio dinamico tra i territori dell'eterocromatina (generalmente non esprimibile e metilata su alcuni amminoacidi chiave) ed eucromatina (generalmente esprimibile e acetilata). Ad esempio, la lisina 9 dell'istone H3 è nota per essere associata alla repressione della cromatina circostante quando metilata. Questa metilazione è riconosciuta da una proteina, HP1, che quindi si lega all'H3 metilato. A sua volta, HP1 attrae la proteina Suv39, una metiltransferasi istone, che può metilare la lisina 9 dell'istone H3 del nucleosoma adiacente e così via. Possiamo quindi vedere come, passo dopo passo, gli istoni H3 verranno metilati e la cromatina sarà condensata. Tuttavia, questa invasione di eterocromatina verrà interrotta se l'H3 lisina 9 incontrata è già acetilata. Viene così stabilito un equilibrio competitivo tra i domini della cromatina espressa e repressa.
I cambiamenti nelle code degli istoni agiscono come "tag" epigenetici che risultano nel reclutamento di diverse classi di proteine, poiché le lisine acetilate o metilate sono riconosciute da domini proteici differenti. Inoltre, il reclutamento di alcuni fattori a livello di cromatina richiede la previa esistenza di modificazioni di istoni e proteine già legate. Il codice istonico viene quindi interpretato nel contesto di altri fattori associati alla cromatina ed è la combinazione dell'interazione tra gli istoni modificati e altri fattori che determina se una proteina viene reclutata per la cromatina.
Varianti istoniche
In diverse specie eucariotiche, sono state scoperte varianti istoniche, chiamate anche istoni non canonici.
Queste varianti hanno una sequenza che differisce da quella degli istoni convenzionali solo su pochi residui (caso delle cosiddette varianti omeomorfe ), o su porzioni maggiori della proteina (caso di varianti eteromorfe ).
Le varianti istoniche svolgono un ruolo importante in diversi aspetti della biologia come la riparazione del DNA, l'organizzazione centromerica, l' inattivazione del cromosoma sessuale X e la condensazione specifica delle cellule dei gameti maschili.
Istoni e temperatura
Nel granchio ( Arabidopsis thaliana ) è sufficiente un solo istone (H2A.Z) per rendere questo taxon sensibile a variazioni di temperatura inferiori a 1 ° C. Questo istone modifica l'avvolgimento del DNA su se stesso e controlla quindi l'accesso al DNA di alcune molecole che inibiscono o attivano diverse dozzine di geni. Questo effetto “bio-termostato” sembra frequente in natura, perché si rileva anche nel lievito .
Nello sperma
Gli istoni sono sostituiti da protamine , proteine ricche di arginina e cisteina .
La ricchezza in cisteina permette la formazione di un ponte disolfuro . Questa struttura protegge il DNA durante eventuali movimenti legati alla fecondazione .
Note e riferimenti
- Annabelle Gérard, Sophie Polo e Geneviève Almouzni , " Code Name: istoni ", Pour la science , n o 46,Marzo 2005( ISSN 0153-4092 , leggi in linea )
- Arents e Moudrianakis 1995
- Sullivan et al. 2002
- Fan e Roberts 2006
- Brush et al. 1985
- Wells e Kedes 1985
- Marzluff et al. 2002
- Kamakaka e Biggins 2005
- Strahl e Allis 2000
- Klose e Zhang 2007
- Redon et al. 2002
- Billon e Cote 2011
- Foltz et al. 2009
- Fernandez-Capetillo et al. 2003
- Okada et al. 2005
- Govin et al. 2004
- Kumar e Wigge 2010
- Perrier 2010
Vedi anche
Bibliografia
- (it) Gina Arents e Evangelos N. Moudrianakis , " La piega istonica: un motivo architettonico onnipresente utilizzato nella compattazione del DNA e nella dimerizzazione delle proteine " , Proc. Natl. Acad. Sci. USA , vol. 92, n o 24,Novembre 1995, p. 11170–11174 ( PMID 7479959 , leggi online [PDF] )
- (it) David Brush , Jerry B. Dodgson , Ok-Ryun Choi , Priscilla Stevens e James Douglas Engel , "I geni istonici di varianti di sostituzione contengono sequenze intermedie " , Mol. Cellula. Biol. , vol. 5, n o 6,1985, p. 1307–1317 ( PMID 2863747 , leggi in linea )
- (it) Li Fan e Victoria Roberts , " Complesso dell'istone linker H5 con il nucleosoma e le sue implicazioni per l'imballaggio della cromatina " , Proc. Natl. Acad. Sci. USA , vol. 103, n o 22,2006, p. 8384–8389 ( PMID 16717183 , DOI 10.1073 / pnas.0508951103 , leggi in linea )
- (it) Oscar Fernandez-Capetillo , Shantha K. Mahadevaiah , Arkady Celeste , Peter J. Romanienko , R. Daniel Camerini-Otero , William M. Bonner , Katia Manova , Paul Burgoyne e André Nussenzweig , " H2AX è richiesto per il rimodellamento della cromatina e inattivazione dei cromosomi sessuali nella meiosi dei topi maschi " , Dev. Cell , vol. 4, n o 4,2003, p. 497–508 ( PMID 12689589 )
- (it) Daniel Foltz , Lars Jansen , Aaron Bailey , John Yates , Emily Bassett , Stacey Wood , Ben Black e Don Cleveland , "L' assemblaggio centromero-specifico dei nucleosomi CENP-A è mediato da HJURP " , Cell , vol. 137, n ° 3,2009, p. 472–484 ( PMID 19410544 , DOI 10.1016 / j.cell.2009.02.039 , leggi online )
- (en) Jérôme Govin , Cécile Caron , Cécile Lestrat , Sophie Rousseaux e Saadi Khochbin , " Il ruolo degli istoni nel rimodellamento della cromatina durante la spermiogenesi dei mammiferi " , Eur. J. Biochem. , vol. 271, n o 17,2004, p. 3459–3469 ( PMID 15317581 , DOI 10.1111 / j.1432-1033.2004.04266.x , leggi online )
- ( fr ) Rohinton Kamakaka e Sue Biggins , " Varianti istoniche: devianti? " , Genes Dev. , vol. 19, n o 3,Febbraio 2005, p. 295–310 ( PMID 15687254 , DOI 10.1101 / gad.1272805 , leggi in linea )
- (en) Robert Klose e Yi Zhang , " Regolazione della metilazione degli istoni mediante demetiliminazione e demetilazione " , Nat. Rev. Mol. Cell Biol. , vol. 8, n o 4,2007, p. 307–318 ( PMID 17342184 , DOI 10.1038 / nrm2143 )
- (en) S. Vinod Kumar e Philip A. Wigge , " I nucleosomi contenenti H2A.Z mediano la risposta termosensoriale in Arabidopsis " , Cell , vol. 140, n o 1,2010, p. 136-147 ( PMID 20079334 , DOI 10.1016 / j.cell.2009.11.006 )
- (en) William Marzluff , Preetam Gongidi , Keith Woods , Jianping Jin e Lois Maltais , " I geni dell'istone dipendenti dalla replicazione umana e murina " , Genomics , vol. 80, n o 5,2002, p. 487–498 ( PMID 12408966 )
- (en) Takashi Okada , Makoto Endo , Mohan Singh e Prem Bhalla , " Analisi della famiglia del gene H3 dell'istone in Arabidopsis e identificazione della variante AtMGH3 specifica del gamete maschile " , Plant J. , vol. 44, n o 4,2005, p. 557-568 ( PMID 16262706 , DOI 10.1111 / j.1365-313X.2005.02554.x )
- Jean-Jacques Perrier , " Un termometro proteico nelle piante ", Per la scienza ,2010( leggi online )
- (it) Christophe Redon , Duane Pilch , Emmy Rogakou , Olga Sedelnikova , Kenneth Newrock e William Bonner , " Histone H2A varianti H2AX e H2AZ " , Curr. Opin. Scopa. Dev. , vol. 12, n o 22002, p. 162–169 ( PMID 11893489 )
- (it) Pierre Billon e Jacques Côté , " Deposizione precisa dell'istone H2A.Z nella cromatina per l'espressione e il mantenimento del genoma " , Biochim Biophys Acta. ,ottobre 2011( PMID 22027408 , leggi in linea )
- (it) Brian D. Strahl e C. David Allis , " Il linguaggio delle modificazioni istoniche covalenti " , Nature , vol. 403, n o 6765,2000, p. 41–45 ( PMID 10638745 , DOI 10.1038 / 47412 )
- (it) Steven Sullivan , Daniel Sink , Kenneth Trout , Izabela Makalowska , Patrick Taylor , Andreas Baxevanis e David Landsman , " The Histone Database " , Nucleic Acids Res. , vol. 30, n o 1,gennaio 2002, p. 341–342 ( PMID 11752331 , leggi in linea )
- (it) Dan Wells e Larry Kedes , " Struttura di un cDNA di istoni umani: prove che i geni degli istoni espressi in modo basale hanno sequenze intermedie e codificano mRNA poliadenilati " , Proc. Natl. Acad. Sci. USA , vol. 82, n o 9,1985, p. 2834–2838 ( PMID 2859593 , leggi online [PDF] )