Elio
| Elio | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Elio liquido superfluido ( T ≤ 2 K ). | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Posizione nella tavola periodica | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Simbolo | Hey | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nome | Elio | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Numero atomico | 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gruppo | 18 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Periodo | 1 e periodo | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bloccare | Blocca s | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Famiglia di elementi | gas nobile | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Configurazione elettronica | 1 s 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elettroni per livello di energia | 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietà atomiche dell'elemento | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Massa atomica | 4.002602 ± 0.000002 u | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Raggio atomico (calc) | 128 pm ( 31 pm ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| raggio covalente | 28 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Raggio di Van der Waals | 140 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Stato di ossidazione | 0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ossido | sconosciuto | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energie di ionizzazione | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 re : 24.587387 eV | 2 e : 54.417760 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isotopi più stabili | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietà fisiche semplici del corpo | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Stato ordinario | Gas | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
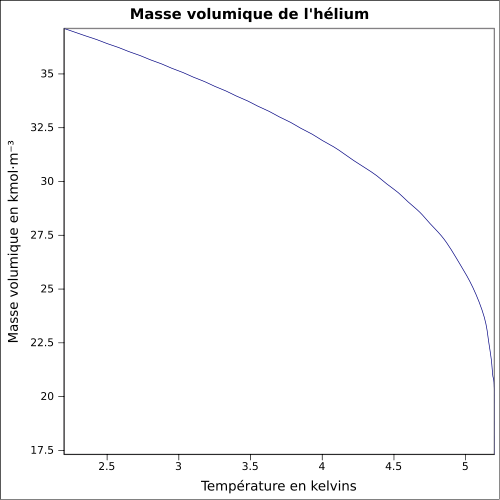
| Massa volumica |
0,1786 g · L -1 ( 0 °C , 1 atm ); 0,125 kg · L -1 (liquido, -268,93 °C ) equazione:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sistema di cristallo | Esagonale compatto | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Colore | Incolore | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto di fusione | 0,95 K ( 26 atm ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto di ebollizione | -268,93 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energia di fusione | 5,23 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energia di vaporizzazione | 0,08 kJ · mol -1 ( 1 atm , -268,93 °C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Temperatura critica | -267,96 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pressione critica | 2,26 atm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volume molare | 22,414 × 10 -3 m 3 · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pressione del vapore |
equazione:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Velocità del suono | 972 m · s -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Calore massiccio | Cp 20,79 J · mol -1 · K -1
equazione:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conduttività termica | 152,0 mW · m -1 · K -1 ( 26,85 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Varie | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100.028.334 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o EC | 231-168-5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Precauzioni | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 avvertimento H280 e P410 + P403 H280 : Contiene gas sotto pressione; può esplodere se riscaldato P410 + P403 : Proteggere dai raggi solari. Conservare in un'area ben ventilata. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 A, A : Temperatura critica del gas compresso = -267,9 ° C Divulgazione all'1,0% secondo i criteri di classificazione |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Trasporto | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
1046 : ELIO COMPRESSO Classe: 2.2 Etichetta: 2.2 :Gasnon infiammabili, non tossici (corrisponde ai gruppi designati da una A o una O maiuscola);  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Unità di SI e STP se non diversamente indicato. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
L' elio è l' elemento chimico di numero atomico 2 del simbolo He. È un gas nobile (o gas raro), praticamente inerte , il primo della famiglia dei gas nobili nella tavola periodica degli elementi . Il suo punto di ebollizione è il più basso tra i corpi conosciuti, ed esiste in forma solida solo se sottoposto a una pressione maggiore di 25 atmosfere .
L'elio ha due isotopi stabili: l' elio 4 ( 4 He), il più abbondante, e l' elio 3 ( 3 He). Questi due isotopi, a differenza di quelli della maggior parte degli elementi chimici, differiscono notevolmente nelle loro proprietà perché il rapporto delle loro masse atomiche è importante. D'altra parte, gli effetti quantistici, sensibili alle basse energie, conferiscono loro proprietà molto diverse. Questo articolo tratta principalmente dell'elio 4 ( 4 He). L'articolo Helium 3 raccoglie le proprietà specifiche dell'isotopo 3 He.
La parola di elio è stato costruito dal greco Helios ( Ἥλιος / helios , "il sole " ), tale elemento essendo stata osservata per la prima volta nella spettro solare su18 agosto 1868, durante un'eclissi solare totale , dall'astronomo Jules Janssen .
L'elio è, dopo l' idrogeno , l'elemento più abbondante nell'Universo . La maggior parte di questo elio è stato prodotto durante la nucleosintesi primordiale, ma altri processi lo producono, in particolare la radioattività α ( vedi sottosezione Abbondanza naturale ). Sulla Terra , secondo una stima del Bureau of Land Management degli Stati Uniti nel 2006, le risorse di elio ammontano a 52 miliardi di metri cubi.
L'elio ha vari usi in forte crescita, mentre la produzione industriale è diminuita per motivi economici: la sua scarsità sta diventando preoccupante. Tuttavia, nel 2016, da un punto di vista economico, il mercato dell'elio è calmo e recentemente è passato da carenza a surplus.
Sono noti otto isotopi dell'elio. L' elio 3 (due protoni e un neutrone) e l' elio-4 (due protoni e due neutroni) sono stabili, altri sono estremamente instabili, virtualmente certi di esistere solo durante il loro addestramento. Nell'atmosfera terrestre c'è solo un atomo di elio-3 per ogni milione di atomi di elio-4 . A differenza della maggior parte degli elementi, l'abbondanza isotopica dell'elio varia ampiamente a seconda della sua origine, a causa di diversi processi di formazione. L'isotopo più abbondante, l' elio 4 , è prodotto sulla Terra dalla radioattività α di elementi pesanti: le particelle α ivi prodotte sono nuclei di elio 4 completamente ionizzati. L' elio-4 è un nucleo per l'insolita stabilità perché i suoi nucleoni sono disposti in strati completi .
In tutto l'Universo, la maggior parte dell'elio presente si è formato (in quantità enormi, circa il 25% di tutta la materia) durante la nucleosintesi primordiale . Quasi tutto il resto dell'elio prodotto nell'Universo è (o è stato) durante la nucleosintesi stellare.
L' elio-3 è presente sulla Terra solo in tracce; la maggior parte risalgono alla formazione della Terra, anche se un po' cade ancora su di essa, intrappolata nella polvere interstellare . Tracce sono ancora prodotte anche dalla radioattività of del trizio . Le rocce nella crosta terrestre hanno rapporti isotopici che variano fino a un fattore 10 e questi rapporti possono essere utilizzati per determinare l'origine delle rocce e la composizione del mantello terrestre. L' elio-3 è più abbondante nelle stelle, ma è prodotto durante la fusione nucleare , le stelle non rilasciano pochissimo (come il deuterio e il litio , o il boro ) in quanto appare solo in una catena intermedia che porta all'elio 4 : esso viene "consumato" come viene prodotto nelle stelle. Di conseguenza, nel mezzo interstellare , il rapporto isotopico è circa 100 volte superiore a quello terrestre. I materiali extraplanetari, come la regolite della Luna o gli asteroidi, hanno tracce di elio 3 dal vento solare . La superficie della Luna contiene una concentrazione dell'ordine di 10 -8 . Diversi autori, a partire da Gerald Kulcinski nel 1986, hanno proposto di esplorare la luna, estrarre l' elio-3 dalla regolite e utilizzarlo per generare energia attraverso la fusione nucleare.
L' elio-4 può essere raffreddato a circa 1 K mediante evaporazione. L' elio-3 , che ha un punto di ebollizione più basso, può essere raffreddato a 0,2 K con lo stesso metodo. Miscele di parti uguali di elio 3 e 4 si separano, al di sotto di 0,8 K , perché non sono più miscibili , a causa delle loro differenze (l'atomo di elio 4 è un bosone mentre l'atomo di elio 3 è un fermione , seguono due diverse statistiche quantistiche) . I frigoriferi a diluizione utilizzano questa proprietà per ottenere alcuni millikelvin.
Altri isotopi dell'elio possono essere prodotti da reazioni nucleari , che sono instabili e decadono rapidamente in altri nuclei. L'isotopo con l' emivita più breve è l' elio 2 (2 protoni, senza neutroni: il diprotone , che decade in due protoni in 3 × 10 −27 s ). L' elio 5 e l' elio 7 decadono per emissione di un neutrone con un'emivita di 7,6 × 10 -23 s e 2,9 × 10 -21 s , rispettivamente. L' elio 6 e l' elio 8 si disintegrano per radioattività con un'emivita di 0,8 s e 0,119 s , rispettivamente. Gli isotopi 6 e 8 hanno una struttura libera in cui i neutroni orbitano lontano dal cuore, si chiama alone nucleare .
Il corpo unico dell'elio
L'elio è un gas incolore, inodore e non tossico. È praticamente chimicamente inerte , monoatomico in ogni circostanza. In un ampio intervallo di temperature e pressioni si comporta sperimentalmente come un gas ideale, il che lo rende una sostanza privilegiata per la sperimentazione di teorie fisico-chimiche. I due isotopi stabili dell'elio sono gli unici composti chimici che non hanno un punto triplo .
Gas
La conduttività termica dell'elio gassoso è maggiore di quella di tutti i gas eccetto l'idrogeno e il suo calore specifico è eccezionalmente elevato. Il suo coefficiente Joule-Thomson è negativo a temperatura ambiente, il che significa che, a differenza della maggior parte dei gas, si riscalda quando può rilassarsi liberamente. La temperatura di inversione Joule-Thomson è di circa 40 K o -233,15 ° C ad una pressione di 1 atm . Una volta raffreddato al di sotto di questa temperatura, l'elio può essere liquefatto raffreddandosi a causa della sua espansione.
L'elio è anche il gas meno solubile in acqua di tutti i gas conosciuti. A causa delle piccole dimensioni dei suoi atomi, la sua velocità di diffusione attraverso i solidi è tre volte quella dell'aria e circa il 65% quella dell'idrogeno.
L'indice di rifrazione dell'elio è più vicino all'unità di quello di qualsiasi altro gas. La velocità del suono nell'elio è maggiore di quella di qualsiasi altro gas eccetto l'idrogeno.
A differenza del plasma , il gas è un ottimo isolante elettrico.
Plasma
La maggior parte dell'elio extraterrestre si trova allo stato plasmatico , le cui proprietà differiscono notevolmente da quelle dell'elio atomico. Nel plasma, gli elettroni dell'elio non sono legati al nucleo, il che porta ad una conduttività elettrica molto elevata, anche quando la ionizzazione è parziale. Le particelle cariche sono molto sensibili ai campi elettrici e magnetici. Ad esempio, nel vento solare , l'elio e l'idrogeno ionizzati interagiscono con la magnetosfera terrestre , dando origine ai fenomeni delle correnti di Birkeland e dell'aurora polare .
Come altri gas nobili, l'elio ha livelli energetici metastabili che gli consentono di rimanere eccitato in una scarica elettrica la cui tensione è inferiore al suo potenziale di ionizzazione. Questo ne consente l'utilizzo in lampade a scarica .
Liquido
A differenza di altri elementi, l'elio rimane liquido fino allo zero assoluto , a pressioni inferiori a 25 atm . Questa è una diretta conseguenza della meccanica quantistica: più precisamente l'energia degli atomi nello stato fondamentale del sistema è troppo alta per consentire la solidificazione (vedi sottocapitolo #Solido ).
Al di sotto del punto di ebollizione a 4.22 K e sopra l' elemento lambda a 2.176 8 K , l' elio-4 esiste come un normale liquido incolore chiamato elio io . Come altri liquidi criogenici , bolle quando viene riscaldato e si contrae quando la sua temperatura si abbassa. L' elio I ha un indice di rifrazione prossimo a quello del gas: 1.026; il che rende la sua superficie così difficile da vedere che spesso usiamo galleggianti in polistirene espanso per vedere il suo livello. Questo liquido incolore ha una viscosità molto bassa e una densità di 0,125 = 1/8 , che è solo un quarto del valore previsto dalla fisica classica . Per spiegare questa proprietà bisogna ricorrere alla meccanica quantistica e quindi l'elio liquido nelle sue varie forme è detto fluido quantistico , a significare che gli effetti della meccanica quantistica, normalmente sensibile solo alla scala microscopica, si manifestano alla scala macroscopica perché l' elio l'atomo 4 è un bosone . Questo viene interpretato come una conseguenza del fatto che il punto di ebollizione è così vicino allo zero assoluto che i movimenti termici casuali non possono più mascherare le proprietà atomiche.
Superfluido
L'elio liquido al di sotto del punto lambda inizia a mostrare caratteristiche piuttosto insolite, in uno stato chiamato elio II .
Al passaggio da elio I a elio II al punto lambda, l'elio si espande. Man mano che la temperatura scende, l' elio II continua ad espandersi, fino a circa 1 K , dove ricomincia a contrarsi come la maggior parte dei corpi.
L' elio II può fluire attraverso capillari da 10 -7 a 10 -8 m senza misurare la viscosità . Tuttavia, quando misuriamo la viscosità tra due dischi che ruotano l'uno rispetto all'altro, troviamo una viscosità paragonabile a quella dell'elio gassoso. La teoria attuale spiega questo fatto utilizzando un modello a due fluidi di László Tisza (in) per l' elio II . In questo modello, l'elio liquido, al di sotto del punto lambda, è costituito da una miscela di atomi di elio allo stato fondamentale e atomi allo stato eccitato, che si comportano più come un normale fluido.
Un'illustrazione di questa teoria è data dall'effetto fontana . In questo esperimento, un tubo verticale, avente un piccolo ugello alla sua estremità superiore, è immerso nella sua estremità inferiore in un bagno di elio II . Vi è bloccato da un disco sinterizzato , attraverso il quale può circolare solo il fluido senza viscosità. Se riscaldiamo il tubo, accendendolo ad esempio, trasformeremo la parte superfluida in fluido ordinario. Per ristabilire l'equilibrio dei due fluidi con il bagno, il superfluido penetrerà attraverso il tappo sinterizzato, e per conservarne il volume, parte del contenuto del tubo verrà espulso attraverso l'ugello superiore, formando un getto che può interrompere cessando di riscaldarsi.
La conducibilità termica di elio II è superiore a quella di qualsiasi altro organismo noto. Ciò impedisce all'elio II di bollire, poiché qualsiasi apporto di calore viaggia immediatamente in superficie, dove evapora semplicemente in gas. Questa conduttività è un milione di volte maggiore di quella dell'elio I e diverse centinaia di volte quella del rame. Ciò è dovuto al fatto che la conduzione del calore avviene per mezzo di un eccezionale meccanismo quantistico. La maggior parte dei materiali che sono buoni conduttori di calore hanno una banda di valenza di elettroni liberi che vengono utilizzati per condurre il calore. L' Helio II non ha questo nastro ma conduce bene il calore. Il flusso di calore obbedisce a equazioni simili alle equazioni d'onda per la propagazione del suono nell'aria. Quando viene introdotto calore, viaggia a 20 m s −1 a 1,8 K in elio II . Queste onde sono chiamate secondo suono .
A differenza dei liquidi ordinari, l' elio II striscia lungo le superfici, anche, apparentemente, contro la gravità . Sfuggerà da un contenitore non chiuso strisciando ai lati, a meno che non incontri un luogo meno freddo dove evapora. Qualunque sia la superficie, si muove in una pellicola di circa 30 nm . Questo film si chiama Il film di Rollin , in memoria del fisico che per primo lo caratterizzò, Bernard V. Rollin. A causa di questo effetto e della capacità dell'elio II di passare rapidamente attraverso piccole aperture, è difficile confinare l'elio liquido. A meno che la nave non sia costruita in modo intelligente, l' elio II salirà sulle pareti e passerà attraverso le valvole fino a raggiungere una regione più calda dove evaporerà. Le onde che si propagano lungo un film di Rollins obbediscono alle stesse equazioni delle onde in acque poco profonde, ma la forza di ripristino qui è la forza di van der Waals invece della gravità. Queste onde sono conosciute come il terzo suono .
Solido
L'elio si solidifica solo sotto l'effetto di forti pressioni. Il solido risultante praticamente invisibile e incolore è altamente comprimibile; la compressione di laboratorio può ridurne il volume di oltre il 30%. Con un modulo di elasticità cubico dell'ordine di 5 × 10 7 Pa , è cinquanta volte più comprimibile dell'acqua. In condizioni di pressione normale, ea differenza di altri elementi, l'elio non solidifica e rimane liquido fino allo zero assoluto . L' elio solido richiede una pressione minima di circa 26 atm . È spesso abbastanza difficile distinguere l' elio solido dall'elio liquido, poiché i loro indici di rifrazione sono quasi identici. Il solido ha un alto calore latente (calore di fusione) e una struttura cristallina esagonale, come quella dell'acqua.
Proprietà chimiche
Come tutti i gas nobili , l'elio ha il suo strato di valenza completo che implica una reattività chimica molto bassa. Poiché non ha substrati in grado di reagire, è (insieme al neon ) il meno reattivo di tutti i corpi semplici .
L'elio può però formare composti instabili ( eccimeri ) con tungsteno, iodio, fluoro, zolfo e fosforo in fase plasmatica , per scarica o altro. He Ne , Hg He 10 , W He 2 e gli ioni molecolari He 2 + , He 2 ++ , HeH + , He D + sono stati creati in questo modo. Questa tecnica ha permesso anche la produzione della molecola neutra He 2 , che ha un numero maggiore di sistemi a bande, e HgHe, la cui coesione sembra dipendere solo dalle forze di polarizzazione . Teoricamente sono possibili anche altri componenti come il fluoroidruro di elio (HHe F ). Nel 2013, l'eliide di litio LiHe si è formata allo stato gassoso mediante ablazione laser a temperatura molto bassa (da 1 a 5 K ).
I primi provata composti stabili elio sono complessi fullerene endohedral , come He @ C 60 , in cui un atomo di elio viene intrappolato in una gabbia di C 60 fullerene . Da allora è stato dimostrato che a pressioni molto elevate (maggiori di 113 GPa ) è possibile formare un composto stabile di elio e sodio, Na 2 He . Tali molecole potrebbero essere trovate anche in pianeti giganti ad alta pressione come Giove e Saturno .
Dall'interno della Terra emerge (nelle lave e nei gas vulcanici ) l'elio ricco di elio 3 , che si ritiene sia primordiale (cioè acquisito durante la formazione della Terra , quasi 4,6 miliardi di anni fa ). Se fosse allo stato gassoso o disciolto nei minerali del mantello inferiore, avrebbe avuto tutto il tempo per degassarsi quasi completamente, data la sua volatilità e le temperature all'interno della Terra. Deve quindi essere immagazzinato come minerale stabile nelle condizioni del mantello inferiore , ma non se ne conoscono. Il calcolo del 2018 dell'entalpia libera di mille ipotetici ma plausibili composti di elio prevedeva un (e solo uno) composto di entalpia libera abbastanza piccolo da intrappolare l'elio nel mantello invece di lasciarlo libero, biossido di ferro ed elio FeO 2 He.
Proprietà biologiche
L'elio, neutro in condizioni standard, non è tossico, non svolge alcun ruolo biologico e si trova in tracce nel sangue umano. Se viene inalato abbastanza da spostare l' ossigeno necessario per la normale respirazione , l' asfissia diventa possibile.
Inalazione
| File audio | |
| Testo letto con elio | |
| Se necessario, al termine dell'udienza utilizzare il tasto pagina precedente del browser . (it) L'elio è un elemento chimico monoatomico incolore, inodore, insapore, inerte, che è a capo della serie dei gas nobili nella tavola periodica e il cui numero atomico è 2. I suoi punti di ebollizione e fusione sono i più bassi tra gli elementi e esiste solo come gas tranne che in condizioni estreme . | |
| Difficoltà nell'utilizzo di questi media? | |
|---|---|
La voce di un individuo che ha inalato elio cambia temporaneamente tono verso armoniche alte - essendo l'elio tre volte meno denso dell'aria, la velocità del suono diventa così maggiore - e poiché la frequenza fondamentale d' una cavità piena di gas è proporzionale alla velocità del suono, l'inalazione di elio corrisponderà ad un aumento delle frequenze di risonanza dell'apparato fonatorio che modulano la frequenza fondamentale data dalle corde vocali . Un effetto opposto, abbassando il timbro, si può ottenere inalando un gas più denso, come l'esafluoruro di zolfo .
L'inalazione di elio puro a basse dosi è normalmente sicura in quanto gas inerte . Tuttavia, l'uso dell'elio venduto in commercio, come quello usato per gonfiare i palloncini, può essere pericoloso a causa dei numerosi contaminanti che può contenere, tracce di altri gas o aerosol di olio lubrificante.
L'inalazione di elio in eccesso può essere pericolosa, poiché l'elio è semplicemente un asfissiante , che sostituisce l'ossigeno necessario per la normale respirazione. La respirazione di elio puro provoca il soffocamento in pochi minuti. L'inalazione di elio direttamente da bombole in pressione è estremamente pericolosa, a causa dell'elevata portata, che può produrre barotraumi che lacerano il tessuto polmonare e possono essere fatali. Tuttavia, questo incidente è piuttosto raro, dal momento che ci sono stati solo due morti tra il 2000 e il 2004 negli Stati Uniti.
Ad alta pressione (oltre 20 atm o 2 MPa ), una miscela di elio e diossigeno ( heliox ) può portare alla sindrome nervosa da alta pressione , una sorta di effetto contro-anestetico. Aggiungendo un po' di azoto alla miscela, il problema può essere evitato. Tuttavia, nelle immersioni subacquee, la sindrome nervosa da alta pressione può essere contrastata solo con l'aggiunta di idrogeno , l'aggiunta di azoto è altamente narcotica non appena la pressione totale raggiunge i 5 bar.
Uso terapeutico
L'elio viene somministrato in miscele contenenti un minimo del 20% di ossigeno a pazienti con ostruzione delle vie aeree superiori o inferiori. La bassa viscosità dell'elio permette quindi di ridurre il lavoro respiratorio.
sicurezza
Le misure di sicurezza per l'elio criogenico sono simili a quelle richieste per l'azoto liquido ; la sua temperatura estremamente bassa può causare ustioni da freddo.
L'inalazione di una grande quantità in un'unica ripresa produce una leggera asfissia , che porta a una breve ma pericolosa perdita di coscienza . Ci sono anche alcuni casi di embolia cerebrale o gravi problemi polmonari nelle persone che inalano elio pressurizzato.
Inoltre, la velocità di espansione tra la fase liquida e la fase gassosa è tale da poter provocare esplosioni in caso di rapida vaporizzazione, se non è installato un limitatore di pressione.
Anche i serbatoi di elio gassoso a 5 - 10 K devono essere trattati come se contenessero elio liquido, a causa della grande e rapida espansione termica che si verifica quando viene introdotto elio al di sotto dei 10 K. a temperatura ambiente.
Usi
Nonostante il suo prezzo elevato, l'elio viene utilizzato per molti usi che richiedono alcune delle sue proprietà uniche, come il basso punto di ebollizione , la bassa densità , la bassa solubilità , l'elevata conduttività termica o il suo carattere chimicamente e biologicamente inerte . Si trova in commercio in forma liquida o gassosa. In forma liquida si possono trovare piccoli serbatoi detti dewar , che possono contenere fino a 1000 l di elio, oppure in grandi serbatoi ISO con capacità nominali fino a 40.000 l . Sotto forma gassosa, piccole quantità di elio vengono fornite in bombole ad alta pressione contenenti fino a 8,5 m 3 standard, mentre grandi quantità vengono consegnate in autocisterne pressurizzate che possono avere capacità fino a 5.000 m 3 standard.
Industriale
A causa della sua inerzia, della sua elevata conducibilità termica , della sua trasparenza ai neutroni e poiché non forma isotopi radioattivi nei reattori, l'elio viene utilizzato come fluido termovettore in alcuni reattori nucleari raffreddati a gas.
L'elio viene utilizzato come atmosfera protettiva durante la crescita del silicio monocristallino per la fabbricazione di circuiti integrati e fibre ottiche , per la produzione di titanio e zirconio e in gascromatografia , perché inerte.
Per la sua inerzia chimica, le sue proprietà termodinamiche e caloriche ideali , la sua alta velocità del suono e un grande coefficiente di Laplace , è utile anche in gallerie del vento supersoniche o per installazioni che studiano fenomeni transitori.
Queste stesse proprietà ne consentono l'utilizzo in dischi rigidi sigillati per aumentarne la capacità. Poiché nessuna tenuta è perfetta, questi dischi hanno un rilevatore che segnala l'eventuale perdita di elio pericolosa per il disco nel tempo.
L'elio miscelato con un gas più pesante, come lo xeno, è utile per la refrigerazione termoacustica , a causa dell'elevato rapporto di capacità termiche e del basso numero di Prandtl . L'inerzia chimica dell'elio ha vantaggi ambientali rispetto ad altri sistemi di refrigerazione, che contribuiscono al buco dell'ozono o al riscaldamento globale .
Poiché si diffonde attraverso i solidi tre volte più velocemente dell'aria, l'elio viene utilizzato per rilevare le perdite nelle apparecchiature per vuoto ultra alto o nei serbatoi ad alta pressione.
Viene utilizzato anche con i prodotti alimentari (additivo alimentare autorizzato dall'Unione Europea con il riferimento E939 ) per consentire il controllo della chiusura ermetica della confezione (vedi elenco additivi alimentari ).
Scienziati
L'uso dell'elio riduce gli effetti della distorsione dovuta alle variazioni di temperatura nello spazio tra le lenti di alcuni telescopi o occhiali , grazie al suo indice di rifrazione eccezionalmente basso. Questo metodo è particolarmente utilizzato per i telescopi solari, soggetti a notevoli variazioni di temperatura, ma per i quali un involucro che sopporta la differenza di pressione tra atmosfera e vuoto sarebbe troppo pesante.
L'età delle rocce e dei minerali che contengono uranio e torio può essere stimata misurando il loro contenuto di elio mediante un processo chiamato datazione dell'elio .
L'elio liquido viene anche utilizzato per raffreddare alcuni metalli alle temperature estremamente basse richieste per la superconduttività , ad esempio per i magneti superconduttori utilizzati in particolare per i rilevatori di risonanza magnetica . Il LHC al CERN utilizza 120 t di elio liquido per mantenere la temperatura dei magneti a 1,9 K . Più in generale, l'elio a bassa temperatura viene utilizzato nella criogenia .
Commerciale e tempo libero
A causa della sua bassa solubilità nel tessuto nervoso , le miscele di elio come trimix , heliox ed elio vengono utilizzate per immersioni profonde per ridurre gli effetti della narcosi da azoto . A profondità superiori a 150 m , piccole quantità di idrogeno vengono aggiunte alla miscela elio-ossigeno per contrastare la sindrome nervosa da alta pressione .
A queste profondità, la bassa densità di elio riduce notevolmente lo sforzo respiratorio.
I laser He-Ne hanno varie applicazioni, in particolare lettori di codici a barre .
Dirigibili, palloni e razzi
Poiché l'elio è più leggero dell'aria, può essere utilizzato per gonfiare dirigibili e palloncini liberi o legati. Sebbene l'idrogeno abbia circa il 7% in più di capacità portante, l'elio ha il vantaggio di essere incombustibile (e persino ritardante di fiamma).
L'esplorazione dell'atmosfera, in particolare per la meteorologia, viene effettuata con palloni, il più delle volte gonfiati con elio.
Nella tecnologia dei razzi, l'elio viene utilizzato come mezzo di spostamento per gestire il carburante e l' ossidante nei serbatoi a microgravità mediante pressurizzazione e per garantire la miscela di idrogeno e ossigeno che alimenta gli ugelli di propulsione. Viene anche utilizzato per eliminare queste sostanze dalle apparecchiature di terra prima del lancio e per preraffreddare l'idrogeno liquido dai veicoli spaziali . Ad esempio, il razzo Saturn V ha consumato circa 370.000 m 3 di elio per decollare.
Risorse e purificazione dell'elio
Abbondanza naturale
L'elio è il secondo elemento più abbondante nell'Universo conosciuto dopo l' idrogeno e costituisce il 23% della sua massa barionica . La stragrande maggioranza dell'elio si è formata per nucleosintesi primordiale , a pochi minuti dal Big Bang . Ecco perché la misurazione della sua abbondanza aiuta a fissare alcuni parametri dei modelli cosmologici. Durante la maggior parte dell'esistenza delle stelle , è formato dalla fusione nucleare dell'idrogeno. Alla fine della loro vita, le stelle utilizzano l'elio come materia prima per la creazione di elementi più pesanti, mediante processi molto più rapidi, addirittura esplosivi. In definitiva, l'elio nell'Universo arriva solo da una piccolissima parte delle stelle.
Nell'atmosfera terrestre, la concentrazione di elio è 5,2 × 10 -6 in volume. Questa bassa concentrazione è abbastanza costante nel tempo, a causa di un equilibrio tra la continua produzione di elio nelle rocce e la fuga nello spazio da parte di vari meccanismi . Nella terrestre eterosfera , parte atmosfera, elio e altri gas leggeri sono i componenti più abbondanti.
Quasi tutto l'elio sulla Terra proviene dalla radioattività α . Si trova principalmente nei composti di uranio e torio , tra cui pechblenda , carnotite e monazite , perché emettono particelle α , che sono nuclei di elio ionizzato He 2+ , che neutralizzano immediatamente con gli elettroni. Si stima che ogni anno nella litosfera vengano prodotte 3.000 t di elio . Nella crosta terrestre, la concentrazione di elio è 8 × 10 -6 in volume. Nell'acqua di mare, è solo 4 × 10 -12 . Ci sono anche piccole quantità nell'acqua minerale , nei gas vulcanici e nel ferro meteorico . Poiché l'elio è intrappolato come il gas naturale da strati di roccia impermeabili, le più alte concentrazioni di elio si trovano nei giacimenti di gas naturale, da cui viene estratta la maggior parte dell'elio commerciale. La sua concentrazione di volume relativa al gas naturale varia da poche parti per milione a una concentrazione del 7% individuata nella contea di San Juan, New Mexico .
Nel 2016, una società denominata "Helium" ha dichiarato di aver individuato tre possibili giacimenti massicci di questo elemento in Tanzania , abbastanza grandi - secondo essa - da rifornire il mondo per diversi decenni, e per questo cerca 40 milioni di dollari investimento per provare a perforare in Tanzania nel 2017. Alcuni esperti ritengono tuttavia che lo sfruttamento di questo giacimento non sarebbe redditizio per molto tempo, perché secondo loro il mercato mondiale è recentemente entrato in un periodo di sovrapproduzione a causa di un uso più economico e in mercato più grande negli Stati Uniti , Qatar e Russia .
Estrazione e purificazione
Per un uso su larga scala, l'elio viene estratto per distillazione frazionata dal gas naturale, che può contenere fino al 7%. Poiché l'elio ha un punto di ebollizione più basso di qualsiasi altro corpo, la bassa temperatura e l'alta pressione vengono utilizzate per liquefare quasi tutti gli altri gas (principalmente diazoto e metano ). L'elio grezzo risultante viene quindi purificato mediante esposizione a temperature sempre più basse, che fanno precipitare praticamente tutto l'azoto e gli altri gas rimanenti dalla miscela di gas. Infine, il carbone attivo viene utilizzato per una fase di purificazione finale, per ottenere così elio con una qualità del 99,995%. La principale impurità nell'elio di grado A è il neon . Per completare la purificazione, la maggior parte dell'elio prodotto viene liquefatto, mediante un processo criogenico. Liquefazione è necessaria per applicazioni che utilizzano elio liquido ed inoltre permette fornitori di elio per ridurre il costo del trasporto a distanza, i serbatoi di elio liquido più grandi hanno una capacità di almeno cinque volte maggiore rispetto a quelli più grandi. Rimorchi trasportano bombole di gas elio sotto pressione a .
Nel 2005 sono stati estratti dal gas naturale, o prelevati dalle riserve, circa 160 milioni di metri cubi di elio, di cui circa l'83% dagli Stati Uniti , l'11% dall'Algeria e il resto principalmente da Russia e Polonia . Negli Stati Uniti, la maggior parte dell'elio viene estratta dal gas naturale di Hugoton e dai giacimenti vicini in Kansas, Oklahoma e Texas.
Un altro metodo per produrre e purificare l'elio è la diffusione del gas naturale grezzo attraverso membrane semipermeabili o altre barriere.
È possibile sintetizzare l'elio bombardando litio o boro con protoni ad alta energia, ma questo non è un metodo di produzione economicamente sostenibile.
Storia
Scoperta
La prima indicazione di elio si osserva su 18 agosto 1868Come una striscia gialla brillante alla lunghezza d' onda di 587,49 nm nello spettro della cromosfera del sole . Questa linea è stata rilevata dall'astronomo francese Jules Janssen durante un'eclissi totale a Guntur (India) . In un primo momento, si pensa che questa linea sia quella del sodio . Il20 ottobredello stesso anno, l'astronomo inglese Norman Lockyer osservò una riga gialla nello spettro solare, che chiamò riga di Fraunhofer D 3 , per la sua vicinanza alle note righe D 1 e D 2 del sodio. Conclude che è causato da un elemento del Sole sconosciuto sulla Terra. Lockyer e il chimico inglese Edward Frankland chiamano questo elemento dopo la parola greca per Sole, ἥλιος ( helios ).
Nel 1882 Luigi Palmieri riuscì per la prima volta a dimostrare la presenza di elio sulla Terra, mediante l'analisi spettrale della lava del Vesuvio .
Il 26 marzo 1895Il chimico britannico Sir William Ramsay isola l'elio sulla Terra trattando la kleveite (una varietà di pechblenda , contenente almeno il 10% di terre rare ) con acidi minerali. Ramsay era alla ricerca di argon , ma, dopo aver separato l'azoto e l'ossigeno dal gas liberato dall'acido solforico , notò nello spettroscopio una riga gialla brillante che coincideva con la riga D3 osservata nello spettro solare.
Questi campioni sono identificati come elio da Lockyer e dal fisico britannico William Crookes . Indipendentemente da ciò, è stato isolato dalla cleveite lo stesso anno dai chimici Per Theodor Cleve e Abraham Langlet (in) a Uppsala , che accumulano abbastanza gas per essere in grado di determinarne con precisione il peso atomico .
L'elio era stato anche isolato dal geochimico americano William Francis Hillebrand , pochi anni prima della scoperta di Ramsay, notando insolite righe spettrali durante l'esame di un campione di uaninite. Ma Hillebrand attribuisce queste righe al diazoto. La sua lettera di congratulazioni a Ramsay presenta un interessante caso di scoperta e quasi scoperta nella scienza.
Nel 1907, Ernest Rutherford e Thomas Royds hanno dimostrato che le particelle α sono nuclei di elio, permettendo alle particelle di entrare attraverso una sottile finestra di vetro di un tubo dove sono evacuate, creando quindi una scarica nel tubo per studiare lo spettro del nuovo gas in esso. Nel 1908, l'elio fu liquefatto per la prima volta dal fisico olandese Heike Kamerlingh Onnes , raffreddando il gas al di sotto di 1 K . Cerca di solidificarlo abbassando ulteriormente la temperatura, ma non ci riesce, poiché l'elio non ha un punto triplo . È uno studente di Onnes, Willem Hendrik Keesom , che riesce a solidificare sotto pressione 1 cm 3 di elio nel 1926.
Nel 1938, il fisico sovietico Pyotr Leonidovich Kapitsa scoprì che l' elio-4 non aveva quasi viscosità a temperature vicine allo zero assoluto, un fenomeno ora chiamato superfluidità. Nel 1972, lo stesso fenomeno fu osservato nell'elio 3 , ma a una temperatura molto più vicina allo zero assoluto, dai fisici americani Douglas D. Osheroff , David M. Lee e Robert C. Richardson . Il fenomeno nell'elio 3 viene interpretato come la formazione di coppie di atomi, che sono fermioni , a formare bosoni , per analogia con le coppie di elettroni di Cooper alla base della superconduttività .
Produzione e usi
Dopo una trivellazione petrolifera nel 1903 a Dexter , Kansas , il getto di gas prodotto era incombustibile. Erasmus Haworth (in) , il geologo dello Stato del Kansas, ha raccolto alcuni campioni del gas prodotto e portato all'Università del Kansas , Lawrence . Con l'aiuto dei chimici Hamilton Cady (en) e David McFarland, è stato determinato che il gas, in volume, 72% nitroso, 15% metano (una percentuale combustibile solo con più ossigeno) gas e 12% non identificabile. Ulteriori analisi mostrano Cady e McFarland che l'1,84% del campione di gas è elio. Ciò dimostra che, nonostante la sua scarsità globale sulla Terra, l'elio è concentrato in grandi quantità sotto le Grandi Pianure americane e disponibile per la produzione come sottoprodotto dello sfruttamento del gas naturale. Le maggiori riserve di elio si trovano nel campo di Hugoton e nei campi limitrofi nel sud-ovest del Kansas con estensioni al Texas e all'Oklahoma.
Ciò ha permesso agli Stati Uniti di diventare il principale produttore mondiale di elio. Su suggerimento di Sir Richard Threlfall (in) , la Marina degli Stati Uniti sovvenziona tre piccoli impianti sperimentali di produzione di elio durante la prima guerra mondiale . L'obiettivo è fornire ai palloni di sbarramento vincolati questo gas non infiammabile, più leggero dell'aria. Questo programma produce un totale di 5.700 m 3 di elio al 92%, sebbene in precedenza fossero stati prodotti meno di 100 L in totale. Parte di questo gas viene utilizzato per il primo dirigibile al mondo riempito di elio, la US Navy C-7, inaugurato nel suo viaggio inaugurale da Hampton Roads in Virginia a Bolling Field a Washington il1 ° dicembre 1921.
Sebbene il processo di liquefazione del gas a bassa temperatura non sia stato sviluppato abbastanza presto per svolgere un ruolo significativo durante la prima guerra mondiale, la produzione continuerà. L'elio viene utilizzato principalmente per gonfiare i palloncini . Questo utilizzo aumenterà la domanda durante la seconda guerra mondiale , così come la domanda di saldatura ad arco .
Lo spettrometro di massa ad elio è anche vitale per il progetto della bomba atomica di Manhattan .
Il governo degli Stati Uniti ha creato nel 1925 una riserva nazionale di elio ad Amarillo , in Texas , con l'obiettivo di fornire aerostati, personale militare in tempo di guerra e civili in tempo di pace. A causa dell'embargo militare degli Stati Uniti contro la Germania, la fornitura di elio fu limitata e l' Hindenburg dovette essere gonfiato con l'idrogeno, con le conseguenze catastrofiche che ne conseguirono quando si incendiò. Il consumo di elio dopo la seconda guerra mondiale è diminuito, ma la riserva è stata aumentata negli anni '50 per garantire la fornitura di elio liquido per il lancio di razzi durante la corsa allo spazio e la guerra fredda . Nel 1965, il consumo di elio negli Stati Uniti supera di otto volte il massimo raggiunto in tempo di guerra.
A seguito degli emendamenti alla legge sull'elio del 1960 (legge pubblica 86-777 ), l'Ufficio delle miniere degli Stati Uniti ha istituito cinque fabbriche private per estrarre l'elio dal gas naturale. Per questo programma di conservazione dell'elio , il Bureau sta costruendo un oleodotto di 684 km da Bushton, Kansas , a Cliffside, vicino ad Amarillo, un campo parzialmente esaurito. La miscela elio-azoto così fornita viene iniettata e conservata fino al momento del bisogno, quando viene estratta e purificata.
Nel 1995 fu raccolto un miliardo di metri cubi di gas ma la riserva ha 1,4 miliardi di dollari di debito, cosa che porta il Congresso degli Stati Uniti , nel 1996, a cessare gradualmente la sua attività. Il conseguente Helium Privatization Act del 1996 (legge pubblica 104-273) ordina al Dipartimento degli Interni degli Stati Uniti di iniziare a svuotare la riserva nel 2005.
L'elio prodotto tra il 1930 e il 1945 era puro al 98,3% circa (~ 2% di azoto), ideale per gli aerostati. Nel 1945 fu prodotta una piccola quantità di elio al 99,9% da utilizzare nella saldatura ad arco. Già nel 1949 erano disponibili quantità commerciali di elio di grado A al 99,995%.
Per diversi anni, gli Stati Uniti hanno prodotto oltre il 90% dell'elio disponibile in commercio nel mondo, con impianti di estrazione in Canada, Polonia, Russia e altre nazioni che producono il resto. A questo ritmo, secondo uno studio (agosto 2010), le riserve degli Stati Uniti si esauriranno prima del 2040 (quasi un terzo del fabbisogno mondiale viene fornito dagli Stati Uniti la cui capacità produttiva mondiale è di circa 142 milioni di metri cubi (nel 2010) mentre i consumi ammontano a 180 milioni di metri cubi e quell'elio sembra "essenziale per la maggior parte delle sue applicazioni" ).
A metà degli anni '90 , una nuova fabbrica iniziò a produrre ad Arzew , in Algeria . Con 1,7 × 10 7 m 3 all'anno, può coprire tutta la domanda europea, ovvero circa il 16% della produzione mondiale. Nel frattempo, il consumo negli Stati Uniti ha superato le 15.000 t nel 2000. Nel 2004-2006 sono stati costruiti altri due impianti, uno a Ras Laffan ( Qatar ) che produce 9,2 tonnellate di elio liquido al giorno, ovvero 1,88 × 10 7 m 3 all'anno, e l'altro a Skikda (Algeria). L'Algeria divenne rapidamente il secondo produttore di elio. Durante questo periodo, il consumo di elio ei costi di produzione sono aumentati. Tra il 2002 e il 2007, i prezzi dell'elio sono raddoppiati e solo nel 2008 i principali fornitori hanno aumentato i loro prezzi di circa il 50% . Ciò è legato alla bassissima produzione e consumo di elio, che ne rende difficile l'eguaglianza, in quanto pochi produttori desiderano investire in questa “ nicchia di mercato ”.
Robert Richardson ( Premio Nobel per la Fisica ) nel 2010 ha avvertito la comunità internazionale del rischio di carenza, sostenendo un aumento dei prezzi, per riflettere la scarsità di questo elemento e sprecarlo di meno .
La società 45-8 Energy, con sede a Metz , ha depositato nell'ottobre 2019 un permesso di esplorazione esclusivo per l'elio nel sud-ovest del dipartimento della Nièvre , in Francia. La risposta della Prefettura è attesa per settembre 2020.
Note e riferimenti
- (fr) Questo articolo è parzialmente o interamente tratto dall'articolo di Wikipedia in inglese intitolato " Helium " ( vedi l'elenco degli autori ) .
- Statistiche di Bose-Einstein e statistiche di Fermi-Dirac .
- Guarda una clip su Youtube di ucilowtemp .
- (en) David R. Lide, CRC Handbook of Chemistry and Physics , CRC Press Inc,2009, 90 ° ed. , 2804 pag. , Copertina rigida ( ISBN 978-1-420-09084-0 )
- (in) Beatriz Cordero Verónica Gómez, Ana E. Platero-Prats, Marc Revés Jorge Echeverría, Eduard Cremades, Flavia e Santiago Barragan Alvarez , " Radi covalenti rivisitati " , Dalton Transactions ,2008, pag. 2832 - 2838 ( DOI 10.1039/b801115j )
- "Ionization Energies of Atoms and Atomic Ions", in CRC Handbook of Chemistry and Physics, 91a edizione (versione Internet 2011), WM Haynes, ed., CRC Press / Taylor e Francis, Boca Raton, FL., P. 10-203
- (en) Robert H. Perry e Donald W. Green , Perry's Chemical Engineers' Handbook , USA, McGraw-Hill,1997, 7 ° ed. , 2400 pag. ( ISBN 0-07-049841-5 ) , pag. 2-50
- "Elio" nella banca dati sulle sostanze pericolose , accesso 1 maggio 2010
- Database Chemical Abstracts interrogato tramite SciFinder Web 15 dicembre 2009 ( risultati della ricerca )
- Sigma-Aldrich foglio del composto elio ≥99.995% , consultato il 17 agosto, 2018.
- " Elio " nel database dei prodotti chimici Reptox del CSST (organizzazione del Quebec responsabile per la sicurezza e la salute sul lavoro), accesso 25 aprile 2009
- Paul Depovere, La tavola periodica degli elementi. La meraviglia fondamentale dell'Universo , De Boeck Supérieur ,2002, pag. 103.
-
(en) Eric Hand, “ Enormi campi di elio trovati nella zona di rift della Tanzania ” , Science , vol. 353, n ° 6295,8 luglio 2016, pag. 109-110 ( DOI 10.1126/science.353.6295.109 , letto online
 , consultato l'11 luglio 2016 ).
, consultato l'11 luglio 2016 ).
- Audrey Chauvet, "Le riserve mondiali di elio si stanno sgonfiando " , su www.20minutes.fr ,30 agosto 2010(consultato il 22 giugno 2019 ) .
- (en) John Emsley , Nature's building blocks: an AZ guide to the elements , Oxford New York, Oxford University Press ,2001, 538 pag. ( ISBN 978-0-19-850340-8 e 978-0-198-50341-5 , OCLC 248877093 , leggi online ) , p. 175–179.
-
(in) Achim Weiss, " Elementi del passato: Big Bang Nucleosintesi e osservazione " , Max Planck Institute for Gravitational Physics (consultato il 23 giugno 2009 ) ;.
(it) A. Coc et al. , " Nucleosintesi aggiornata del Big Bang confrontata alle osservazioni WMAP e all'abbondanza di elementi leggeri " , The Astrophysical Journal , vol. 600,2004, pag. 544 ( DOI 10.1086/380121 ). -
(in) Don L. Anderson, GR Foulger Anders Meibom, " Helium Fundamentals " , MantlePlumes.orgMantlePlumes.org,
2006(consultato il 20 luglio 2008 ) .
Solo
astratto. Oggetto proposto in vendita. - (in) Aaron Novick , " Half-Life of Tritium " , Physical Review , vol. 72, 1947, pag. 972 ( DOI 10.1103/PhysRev.72.972.2 , leggi online )Accesso riservato agli abbonati PROLA.
- (in) GN Zastenker e E. Salerno, F. Buehler, P. Bochsler, M. Bassi, YN Agafonov, NA Eismont, VV Khrapchenkov, H. Busemann , " Composizione isotopica e abbondanza di elio neutro interstellare basato su misurazioni dirette " , Astrofisica , vol. 45, n . 2aprile 2002, pag. 131-142 ( DOI 10.1023/A: 1016057812964 , leggi online ) Solo astratto . Oggetto proposto in vendita.
- (in) " Lunar Mining of Helium-3 " , Fusion Technology Institute dell'Università del Wisconsin-Madison, 2007(consultato il 9 luglio 2008 ) .
- (it) EN Slyuta AM Abdrakhimov EM Galimov, " La stima delle riserve probabili di elio-3 nella regolite lunare in Lunar and Planetary Science XXXVIII " [PDF] ,2007(consultato il 23 giugno 2009 ) .
- (in) Eric R. Hedman , " Un'ora affascinante con Gerald Kulcinski " , The Space Review ,16 gennaio 2006( leggi in linea ).
- (in) Peter Häussinger1 Reinhard Glatthaar2 Wilhelm Rhode3 Helmut Kick4 Christian Benkmann5 Josef Weber6 Hans-Jörg Wunschel7 Viktor Stenke8 Edith Leicht9 Hermann Stenger10, Gas nobili , Wiley-VCH Verlag GmbH & Co , et al. " Enciclopedia della chimica industriale di Ullmann ",15 marzo 2001( presentazione on line ).
- (en) LW Brandt, (Clifford A. Hampel, ed.) The Encyclopedia of the Chemical Elements , Reinhold Book Corporation , New York, 1968, cap. "Elio" , p. 256-268 .
- (in) Ray F. Weiss , " Solubilità di elio e neon in acqua e acqua di mare " , J. Chem. ing. Dati , vol. 16, n . 21971, pag. 235-241 ( DOI 10.1021/je60049a019 )Prima pagina.
- (in) Jack A. Stone e Alois Stejskal , " Uso dell'elio come standard di rifrazione " , Metrologia , vol. 41,2004, pag. 189–197 ( DOI 10.1088 / 0026-1394 / 41/3/012 ) Astratto .
- (in) L'Enciclopedia degli elementi chimici , op. cit. , pag. 261 .
- (in) F. Buhler e WI Axford, HJA Chivers, K. Martin , " Isotopi dell'elio nell'aurora dell'anno " , J. Geophys. Ris. , vol. 81, n . 1,1976, pag. 111-115 ( DOI 10.1029/ JA081i001p00111 ) Astratto .
- (en) L'Enciclopedia degli elementi chimici , op. cit. pag. 262 .
- (in) PC Hohenberg e PC Martin , " Teoria microscopica dell'elio superfluido " , Annals of Physics , vol. 281, n osso 1-2,ottobre 2000, pag. 636–705 ( DOI 10.1006 / aphy.2000.6019 ) Astratto . Articolo disponibile per gli abbonati a ScienceDirect.
- (a) L'Enciclopedia degli elementi chimici , op. cit. , pag. 263 .
- (in) HA Fairbank e CT Lane , " Rollin Film Rates in Liquid Helium " , Physical Review , vol. 76, n . 8,ottobre 1949, pag. 1209–1211 ( DOI 10.1103 / PhysRev.76.12.09 ) Astratto . Oggetto proposto in vendita.
- (in) BV Rollin e F. Simon , " Sul" film "fenomeno dell'elio liquido II " , Physica , vol. 6, n o 21939, pag. 219–230 ( DOI 10.1016 / S0031-8914 (39) 80013-1 ) Astratto . Articolo disponibile per gli abbonati a ScienceDirect.
- (in) Fred Ellis, " Terzo suono " , Wesleyan Quantum Fluids Laboratory ,settembre 2005(consultato il 23 giugno 2009 ) .
- (in) D. Bergman , " Hydrodynamics and Third Thin Sound in He II Movies " , Physical Review , vol. 188, n ° 1,ottobre 1949, pag. 370–384 ( DOI 10.1103/FisRev.188.370 ) Astratto . Disponibile per gli abbonati PROLA, o in vendita.
- (en) " Tavola periodica: elio " (consultato il 23 giugno 2009 ) .
- (in) Naima Tariq Nada Taisan, Vijay Singh e Jonathan Weinstein, " Rilevazione spettroscopica della molecola LiHe " , Physical Review Letters , vol. 110, n . 15,8 aprile 2013, pag. 153201 ( PMID 25167262 , DOI 10.1103 / PhysRevLett.110.153201 , lettura online , accesso 10 dicembre 2017 ).
- SB " L'elio si lega al sodio ad alta pressione " Per la scienza , n o 474,aprile 2017, pag. 10.
- (in) Xiao Dong, Artem R. Oganov et al. , " Un composto stabile di elio e sodio ad alta pressione " , Nature Chemistry ,6 febbraio 2017( leggi in linea )
- " La chimica dell'elio, sconosciuta sulla Terra, potrebbe esistere nei pianeti giganti " , su futura-sciences.com ,9 febbraio 2017(consultato il 9 febbraio 2017 )
- (in) Jurong Zhang Jian Lv, Hefei Li, Feng Xiaolei Cheng Lu et al. , " Composto raro contenente elio FeO 2 He stabilizzato in condizioni di terra profonda " , Physical Review Letters , vol. 121, n . 25,21 dicembre 2018, pag. 1-6, articolo n o 255703 ( DOI 10.1103 / PhysRevLett.121.255703 , leggi online [PDF] ).
- (in) R. Mark Wilson, " Un composto contenente elio nelle profondità della Terra si trova computazionalmente " , Physics Today ,10 gennaio 2019( DOI 10.1063/PT.6.1.20190110a ).
- (in) " Focus: Una casa per l'elio all'interno della Terra " , Fisica (in) , vol. 11,21 dicembre 2018, articolo n . 133 ( leggi online ).
- (in) J. Ackerman e G. Maitland , " Calcolo della velocità relativa del suono in una miscela di gas " , Undersea Biomed. Ris. , vol. 2, n ° 4,dicembre 1975, pag. 305-310 ( leggi online ).
- (in) Joe Wolfe, "La fisica nel discorso " , phys.unsw.edu.au. (consultato il 23 giugno 2009 ) .
- Perché l'elio cambia la voce? su futura-sciences.com .
- (en) Martin Grassberger e Astrid Krauskopf , “ Asfissia suicida con elio: resoconto di tre casi. Suizid mit Helium Gas: Bericht über drei Fälle. » , Wiener Klinische Wochenschrift , vol. 119, nn . 9-10,2007, pag. 323–325 ( DOI 10.1007 / s00508-007-0785-4 )Riassunto in tedesco. Prima pagina disponibile. Oggetto proposto in vendita.
- (in) Daniel Engber, " Stai fuori da quel pallone! " , Slate.com,2006(consultato il 23 giugno 2009 ) .
- (in) JC Eotain , C. Lemaire , MC-Gardette Chauffour , J. Doucet e R. Naquet , " Stima della suscettibilità umana alla sindrome nervosa ad alta pressione " , Journal of Applied Physiology , vol. 54, n . 4,aprile 1983, pag. 1063-1070 ( leggi in linea )Disponibile su abbonamento personale o istituzionale.
- (in) WL Hunger Jr. e PB Bennett , " Le cause, i meccanismi e la prevenzione della sindrome nervosa da alta pressione " , Undersea Biomedical Research , vol. 1, n ° 1,1974, pag. 1-28 ( ISSN 0093-5387 , OCLC 2068005 , PMID 4619860 , leggi online ).
- (a) Glenn D. Considine (ed.) Di Van Nostrand Encyclopedia of Chemistry , Wylie-Interscience, ( ISBN 0-471-61525-0 ) , cap. "Elio" , p. 764-765 .
- (in) IE Beckwith e CG Miller III , " Aerotermodinamica e transizione nella galleria del vento ad alta velocità alla NASA's Langley " , Annual Review of Fluid Mechanics , vol. 22,1990, pag. 419–439 ( DOI 10.1146 / annurev.fl.22.010190.002223 ).
- (in) CI Morris, Shock Induced Combustion in High Speed Wedge Flows , Stanford University Thesis , 2001 [ leggi online (consultato il 23 giugno 2009)] .
- https://www.lemondeinformatique.fr/actualites/lire-un-disque-dur-helium-16-to-pour%C2%A0datacenter%C2%A0chez-toshiba-75335.html
- (in) James R. Belcher e William V. Slaton, Richard Raspet Henry E. Bass, Jay Lightfoot , " Gas funzionanti nei motori termoacustici " , The Journal of the Acoustical Society of America , vol. 105, n . 5,1999, pag. 2677–2684 ( DOI 10.1121 / 1.426884 )Disponibile su abbonamento.
- (in) Arjun Makhijani Kevin Gurney, Riparare il buco dell'ozono: scienza, tecnologia e politica , MIT Press , 1995 ( ISBN 0-262-13308-3 ) .
- (in) H. Jakobsson , " Simulazione della dinamica del grande telescopio solare terrestre " , Transazioni astronomiche e astrofisiche , vol. 13, n ° 1,1997, pag. 35–46 ( DOI 10.1080 / 10556799708208113 ) Astratto . Articolo in abbonamento.
- (in) O. Engvold e RB Dunn RN Smartt, WC Livingston , " Test del vuoto VS elio in un telescopio solare " , Ottica applicata , vol. 22,1983, pag. 10–12 ( DOI 10.1364/AO.22.000010 , leggi online ) Astratto . Oggetto proposto in vendita.
- (in) " CERN-LHC: Facts and Figures - LHC booklet guide " ( Archivio • Wikiwix • Archive.is • Google • Cosa fare ) [PDF] , CERN (consultato il 23 giugno 2009 ) .
- (in) " Criogenia: basse temperature, alte prestazioni | CERN ” , su home.cern (consultato il 7 febbraio 2019 ) .
- (in) B. Fowler e KN Ackles, G. Porlier , " Effetti della narcosi da gas inerte è comportamento-A Critical Review " , Undersea Biomedical Research Journal ,1985( PMID 4082343 , leggi online ).
- (in) JR Thomas , " Inversione della narcosi da azoto nei ratti mediante pressione dell'elio " , Undersea Biomed. Ris. , vol. 3, n . 3,1976, pag. 249-259 ( PMID 969027 , leggi online ).
- (it) JC Eotain e MC-Gardette Chauffour, C. Lemaire, R. Naquet , " Effetti di un H 2 -He-O 2miscela sulle HPNS fino a 450 msw ” , Undersea Biomed. Ris. , vol. 15, n ° 4,1988, pag. 257-270 ( ISSN 0093-5387 , OCLC 2068005 , PMID 3212843 , leggi online ).
- (in) Scott J. Butcher e Richard L. Jones, Jonathan R. Mayne, Timothy C. Hartley, Stewart R. Petersen , " La meccanica della ventilazione fisica compromessa con l'apparato respiratorio autonomo è migliorata con l'eliox " , European Journal of Fisiologia applicata , Paesi Bassi, Springer, vol. 101, n . 6,dicembre 2007, pag. 659–669 ( DOI 10.1007 / s00421-007-0541-5 )Prima pagina gratuita, articolo riservato agli abbonati Springer.
- (it) Albert Stwertka, Guida agli Elementi: Revised Edition , Oxford University Press , New York, 1998 ( ISBN 0-19-512708-0 ) , p. 24 .
- (in) BM Oliver e James G. Bradley, Harry Farrar IV , " Concentrazione di elio nella bassa atmosfera terrestre " , Geochimica e Cosmochimica Acta , vol. 48, n . 9,1984, pag. 1759–1767 ( DOI 10.1016 / 0016-7037 (84) 90030-9 ) Abstract gratuito, articolo disponibile su abbonamento ScienceDirect.
- (in) " The Atmosphere: Introduction in JetStream - Online School for Weather " , National Weather Service , 29 agosto 2007 (consultato il 23 giugno 2009 ) .
- (it) Ø. Lie-Svendsen e MH Rees , " L'elio fuoriesce dall'atmosfera terrestre: il meccanismo di deflusso ionico " , Journal of Geophysical Research , vol. 101, n o A21996, pag. 2435–2444 ( DOI 10.1029/95JA02208 ) Abstract , articolo in abbonamento AGU.
- (in) Nick Strobel, " Note di astronomia di Nick Strobel cap. Atmosfere ' ,2007(consultato il 23 giugno 2009 ) .
- (in) Melvin A. Cook , " Dov'è l'elio radiogeno della Terra? » , Natura , vol. 179,1957, pag. 213 ( DOI 10.1038 / 179213a0 ) Riassunto , oggetto messo in vendita.
- (in) LT Aldrich e Alfred O. Nier , " L'occorrenza di Eb 3in Fonti naturali di elio ” , Phys. rev. , vol. 74,1948, pag. 1590–1594 ( DOI 10.1103 / PhysRev.74.1590 ) Abstract , articolo sull'abbonamento PROLA.
- (in) P. Morrison e J. Pine , " Radiogenic Origin of the Helium Isotopes in Rock " , Annals of the New York Academy of Sciences , vol. 62, n . 3,1955, pag. 71–92 ( DOI 10.1111 / j.1749-6632.1955.tb35366.x )Nessun abstract , ringraziamenti, articolo sull'abbonamento a Wiley InterScience.
- (in) RE Zartman , " Elio Argon e carbonio nei gas naturali " , Journal of Geophysical Research , vol. 66, n ° 1,1961, pag. 277–306 ( DOI 10.1029/ JZ066i001p00277 , leggi online )In abbonamento AGU, o in vendita.
- (in) Ronald F. Broadhead , " L'elio nel Nuovo Messico: domanda di distribuzione della geologia e possibilità di esplorazione delle risorse " , New Mexico Geology , vol. 27, n . 4,2005, pag. 93–10 ( leggi online [PDF] ).
- (it) Hand, E (2016) Enormi campi di elio trovati nell'area del rift della Tanzania ; Scienza 08 luglio 2016: vol. 353, numero 6295 , pag. 109-110 DOI : 10.1126 / scienza.353.6295.109 .
- (in) Mark Winter, " Helium: the essentials " , Università di Sheffield ,2008(consultato il 23 giugno 2009 ) .
- (in) L'Enciclopedia degli elementi chimici , op. cit. , pag. 258 .
- (en) EM Smith e TW Goodwin, J. Schillinger , “ Sfide alla fornitura mondiale di elio nel prossimo decennio ” , Advances in Cryogenic Engineering , vol. 49A, n ° 710, 2003, pag. 119–138 ( DOI 10.1063 / 1.1774674 , leggi online [PDF] ).
- (in) " Riepiloghi sulle materie prime minerali - Elio " [PDF] , US Geological Survey ,2004(consultato il 23 giugno 2009 ) .
- (it) VP Belyakov , SG Durgar'yan, BA Mirzoyan et al. , “ Tecnologia delle membrane - Una nuova tendenza nella separazione dei gas industriali ” , Ingegneria chimica e petrolifera , vol. 17, n ° 1,diciannove ottantuno, pag. 19–21 ( DOI 10.1007 / BF01245721 )Prima pagina gratuita, il proseguimento su abbonamento SpringerLink oa pagamento.
- (in) PI Dee e ETS Walton , " A Photographic Investigation of the Transmutation of Lithium and Boron by Protoni e ioni di litio da parte dell'isotopo pesante dell'idrogeno " , Atti della Royal Society of London , vol. 141, n . 8451933, pag. 733-742 ( DOI 10.1098 / rspa.1933.0151 )Accesso a pagamento o in abbonamento per i non membri della Royal Society .
- (in) RK Kochhar , " Astronomi francesi in India durante i secoli XVII-XIX " , Journal of the British Astronomical Association , vol. 101, n . 21991, pag. 95–100 ( leggi online ).
- (in) L'Enciclopedia degli elementi chimici , op. cit. , pag. 256 .
- (in) William Thomson, Frankland e Lockyer trovano le protuberanze gialle per dare una linea molto brillante Decisa non lontano dall'obiettivo D Finora non identificato con alcuna fiamma terrestre. Sembra indicare una nuova sostanza, che propongono di chiamare Elio. , Resp. Brit. Assoc. xcix , 1872.
- definizione di Cleveitis .
- (a) L'Enciclopedia degli elementi chimici , op. cit. , pag. 257 .
- (in) William Ramsay , " era Gas che mostra lo spettro dell'elio, la presunta causa di D3 una delle linee nello spettro coronale. Nota preliminare ” , Atti della Royal Society di Londra , vol. 58,1895, pag. 65–67 ( DOI 10.1098 / rspl.1895.0006 )A pagamento, o in abbonamento per i non membri della Royal Society .
- (in) William Ramsay , " Elio, un costituente gassoso di alcuni minerali. Parte I ” , Atti della Royal Society di Londra , vol. 58,1895, pag. 80–89 ( DOI 10.1098 / rspl.1895.0010 )A pagamento, o in abbonamento per i non membri della Royal Society.
- (in) William Ramsay , " Elio, un costituente gassoso di alcuni minerali. Parte II ” , Atti della Royal Society di Londra , vol. 59,1895, pag. 325–330 ( DOI 10.1098 / rspl.1895.0097 )A pagamento, o in abbonamento per i non membri della Royal Society .
- (De) NA Langlet , " Das Atomgewicht des Heliums " , Zeitschrift für anorganische Chemie , vol. 10, n ° 1,1895, pag. 289–292 ( DOI 10.1002 / zaac.18950100130 )In vendita o in abbonamento a Wiley InterScience.
- (in) ER Weaver, Chimica industriale e ingegneristica , 1919, cap. “ Bibliografia della letteratura sull'elio ” .
- (in) Pat Munday, American National Biography , John A. Garraty e Mark C. Carnes (ed.), Oxford University Press , 1999 " Voce biografica per WF Hillebrand (1853-1925), geochimico e amministratore dell'US Bureau of Standards » , vol. 10-11, pag. 227-228 .
- (in) Dirk van Delft , " Una piccola tazza di elio, una grande scienza " , Fisica oggi ,2008, pag. 36–42 ( leggi online [PDF] ).
- (in) "Il freddo più freddo " , Time Inc. ,1929(consultato il 23 giugno 2009 ) .
- (in) P. Kapitza , " Viscosità dell'elio liquido sotto il punto " , Nature , vol. 141,1938, pag. 74 ( DOI 10.1038 / 141074a0 ).
- (in) DD Osheroff e RC Richardson, DM Lee , " Evidence for a New Phase of Solid Heb 3 " , Phys. rev. Lett. , vol. 28, n . 14,1972, pag. 885-888 ( DOI 10.1103 / PhysRevLett.28.885 ) Astratto . Articolo protetto da copyright di PROLA.
- (in) DF McFarland , " Composizione di gas da un pozzo a Dexter, Kan " , Transazioni della Kansas Academy of Science , vol. 19,1903, pag. 60–62 ( DOI 10.2307 / 3624173 , leggi online )Prima pagina. Articolo completo sotto i termini JSTOR.
- (in) " La scoperta dell'elio nel gas naturale " , American Chemical Society ,2004(consultato il 23 giugno 2009 ) .
- (in) HP Cady e DF McFarland , " Elio nel gas naturale " , Science , vol. 24,1906, pag. 344 ( DOI 10.1126 / scienze.24.611.344 )Nessun astratto . Articolo in vendita, o membri AAAS.
- (in) HP Cady e DF McFarland , " Helium in Kansas Natural Gas " , Transactions of the Kansas Academy of Science , vol. 20,1906, pag. 80–81 ( DOI 10.2307 / 3624645 , leggi online [ archivio di27 maggio 2012] )<Nessun astratto . Articolo in condizioni JSTOR.
- (in) Eugene M. Emme, (a cura di) Aeronautics and Astronautics: An American Chronology of Science and Technology in the Exploration of Space, 1915-1960 , NASA , Washington, DC, 1961 [ leggi online (consultato il 23 giugno 2009 )] , cap. " Cronologia dell'aeronautica e dell'astronautica, 1920-1924 " , p. 11-19 .
- (in) N. Hilleret, S. Turner (ed.) CERN Accelerator School, tecnologia del vuoto: atti: Scanticon Conference Center, Snekersten, Danimarca, 28 maggio - 3 giugno 1999 , CERN , Ginevra, Svizzera, 1999 [ leggi riga ( pagina consultata il 23 giugno 2009)] , cap. " Rilevamento perdite " , pag. 203-212 . “L'inizio del metodo di rilevamento delle perdite di elio deve essere fatto risalire al Progetto Manhattan e ai requisiti di tenuta senza precedenti degli impianti di separazione dell'uranio. La sensibilità richiesta per la verifica della tenuta ha portato alla scelta dello spettrometro di massa ideato dal Dr. AOC Nier, e tarato sulla massa dell'elio. "
- (in) John G. Williamson , " Energia per il Kansas " , Transazioni della Kansas Academy of Science , Kansas Academy of Science , vol. 71, n . 4,inverno 1968, pag. 432–438 ( leggi in linea )Prima pagina. Articolo completo sotto i termini JSTOR.
- (in) - , " Vendita di elio per la conservazione " , Registro federale , vol. 70, n . 193,6 ottobre 2005, pag. 58464 ( leggi online [PDF] ).
- (in) " Riepilogo esecutivo: l'impatto della vendita della Federal Helium Reserve " , nap.edu ( ISBN 978-0-309-07038-6 , accesso 23 giugno 2009 ) .
- (in) PV Mullins, RM Goodling Helium , Bureau of Mining / Minerals Yearbook 1949, 1951 [ leggi online (consultato il 21 giugno 2009)] , p. 599–602 .
- (in) studio Selling the Nation's Helium Reserve ,agosto 2010.
- (in) GR Matos, JB Peterson, " Helium End User Statistic " , US Geological Survey (consultato il 23 giugno 2009 ) .
- (in) Karen H. Kaplan , "La carenza di elio ostacola la ricerca e l'industria " , Physics Today , American Institute of Physics , vol. 60, n . 6,giugno 2007, pag. 31–32 ( DOI 10.1063 / 1.2754594 , leggi online ).
- (in) Sourish Basu e Philip Yam (ed.) , " Aggiornamenti: nell'aria sottile " , Scientific American , Scientific American, Inc. , vol. 297, n . 4,ottobre 2007, pag. 18 ( leggi in linea ).
- Ludovic Pillevesse, " La prefettura concederà o meno, a settembre, un permesso esclusivo per la ricerca sull'elio nella Nièvre ", Le journal du Centre ,31 agosto 2020( leggi in linea )
Vedi anche
Bibliografia
a. (it) Z. Cai, R. Clarke, N. Ward, WJ Nuttall, BA Glowacki, " Modelling Helium Markets " [PDF] , Università di Cambridge ,2007(consultato il 22 giugno 2009 ) .
Articoli Correlati
- Superfluidità
- criogenia
- Chimica dei gas nobili
- Calefaction o effetto Leidenfrost
- Conservare la carne
- Rilevamento perdite
-
Elio metastabile

link esterno
- " La scoperta dell'elio liquido nel 1908 da parte di Kamerlingh " , BibNum (consultato il 21 giugno 2009 ) , testo commentato.
- (it) " Dati tecnici per l'elio " (consultato il 23 aprile 2016 ) , con i dati noti per ciascun isotopo nelle sottopagine
- Registri di autorità :
- Avvisi in dizionari generali o enciclopedie :
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | H | Hey | |||||||||||||||||||||||||||||||
| 2 | Li | Essere | B | VS | NON | oh | F | Nato | |||||||||||||||||||||||||
| 3 | N / A | Mg | Al | sì | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | è | Sc | Ti | V | Cr | mn | Fe | Co | O | Cu | Zn | Ga | Ge | Asso | Vedi | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | sì | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | CD | Nel | Sn | Sb | voi | io | Xe | |||||||||||||||
| 6 | Cs | Ba | Il | Questo | prima | Nd | Pm | Sm | Aveva | Gd | Tb | Dy | come | Er | Tm | Yb | Leggere | HF | Il tuo | W | Ri | osso | Ir | Pt | A | Hg | Tl | Pb | Bi | po | A | Rn | |
| 7 | Fr | RA | AC | questo | papà | tu | Np | Poteva | Am | Cm | Bk | Cf | È | Fm | Md | No | Lr | Rf | Db | Sg | bh | Hs | Mt | Ds | Rg | Cn | Nh | fl | Mc | Lv | Ts | Og | |
| 8 | 119 | 120 | * | ||||||||||||||||||||||||||||||
| * | 121 | 122 | 123 | 124 | 125 | 126 | 127 | 128 | 129 | 130 | 131 | 132 | 133 | 134 | 135 | 136 | 137 | 138 | 139 | 140 | 141 | 142 | |||||||||||
|
Metalli Alcalini |
Terra alcalina |
lantanidi |
Metalli di transizione |
Metalli poveri |
Metal- loids |
Non metalli |
geni dell'alone |
Gas nobili |
Articoli non classificati |
| attinidi | |||||||||
| Superattinidi | |||||||||