diidrogeno
| diidrogeno | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identificazione | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| nome IUPAC | idrogeno | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sinonimi |
idrogeno |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100.014.187 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o EC | 215-605-7 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o E | E949 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SORRISI |
[HH] , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChi |
InChI: InChI = 1 / H2 / h1H |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aspetto | gas inodore, incolore, compresso | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietà chimiche | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Formula |
H 2 [Isomeri] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Massa molare | 2.01588 ± 0.00014 g / mol H 100%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietà fisiche | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T° fusione | -259,1 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T° ebollizione | -252,76 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| solubilità |
21,4 ml in 1 l di acqua (cioè 1,92 mg/l ) ( 0 ° C ) 8,5 ml in 1 l di acqua ( cioè 0,76 mg / l ) ( 80 ° C ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Parametro di solubilità δ | 6,9 MPa 1/2 ( 25 °C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Massa volumica |
0,089 88 g/l (gas, CNTP ), 0,070 8 kg/l (liquido, -253 °C ), equazione:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Temperatura di autoaccensione | da 500 a 571 °C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| punto d'infiammabilità | gas infiammabile | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Limiti di esplosività nell'aria | 4 - 76 % vol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pressione di vapore saturante |
equazione:
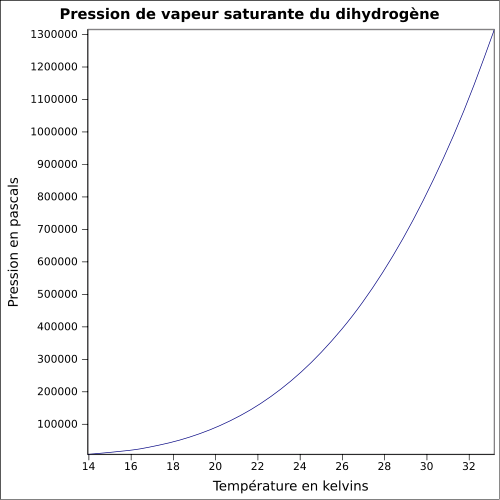
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto critico | 13,0 bar, -239,95 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto triplo |
-259.3467 °C ; 7.205 kPa abs |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conduttività termica | 42,5 × 10 -5 cal cm -1 s -1 K -1 a 16,85 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Velocità del suono | 1310 m s −1 ( 27 ° C , 1 atm ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termochimica | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 gas, 1 bar | 130,68 JK −1 mol −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ fus H ° | 0,058 68 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ vap H ° | 0,90 kJ mol -1 ( 1 atm , -252,76 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Do p | 14 266 J kg −1 K −1 a 293 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PC | 285,8 kJ/mol ( 25 °C , gas) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PCI | 242,7 kJ/mole | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Precauzioni | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Pericolo H220 H220 : Gas altamente infiammabile |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  A, B1, A : Temperatura critica del gas compresso = −239,9 ° C B1 : Limite inferiore di infiammabilità del gas infiammabile = 4,0% Divulgazione all'1,0% secondo i criteri di classificazione |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| gas :
4
0
0
liquido refrigerato: 4 3 0 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Trasporto | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
23 : gas infiammabile Numero ONU : 1049 : IDROGENO COMPRESSO Classe: 2.1 Codice di classificazione: 1F : Gas compresso, infiammabile; Etichetta: 2.1 : Gas infiammabili (corrisponde ai gruppi indicati con la F maiuscola); 
223 : gas liquefatto refrigerato, infiammabile Numero ONU : 1966 : LIQUIDO REFRIGERATO A IDROGENO Classe: 2.1 Codice di classificazione: 3F : Gas liquefatto refrigerato, infiammabile; Etichetta: 2.1 : Gas infiammabili (corrisponde ai gruppi indicati con la F maiuscola);  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Inalazione | soffocamento | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Unità di SI e STP se non diversamente indicato. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Il diidrogeno è la forma molecolare dell'elemento idrogeno che esiste come gas a condizioni standard di temperatura e pressione . Le molecole hanno due atomi di idrogeno; la sua formula chimica è H 2 . Viene anche chiamato "idrogeno molecolare" o, allo stato gassoso, "gas idrogeno". Nel linguaggio quotidiano, quando non c'è ambiguità con l'elemento chimico con lo stesso nome, è molto spesso indicato semplicemente come "idrogeno", e talvolta si parla semplicemente di "molecola di idrogeno" per la molecola di idrogeno.
Veniva utilizzato nei dirigibili di tipo zeppelin , sfruttando le proprietà della spinta di Archimede , prima di essere sostituito dall'elio , meno pericoloso perché non combustibile. Oggi il consumo globale di idrogeno è di circa 50 milioni di tonnellate all'anno. La maggior parte della produzione di idrogeno viene consumata in loco, principalmente nell'industria chimica e petrolchimica: sintesi dell'ammoniaca (50%), raffinazione e desolforazione degli idrocarburi (37%), sintesi del metanolo (12%). È composto per il 96% da idrocarburi (metano, petrolio, carbone) e per il 4% dall'elettrolisi dell'acqua . Questa produzione è accompagnata nel 2020 dalla produzione di 830 milioni di tonnellate di CO 2all'anno, ovvero circa il 2% delle emissioni globali .
È un gas leggero che la gravità terrestre non può trattenere. Brucia nell'aria producendo acqua , da qui il suo nome composto dal prefisso "idro", dal greco ὕδωρ (hudôr) che significa "acqua", e dal suffisso "gene", dal greco γεννᾰν (gennen), "generare" . È stato utilizzato in particolare per la conservazione della carne . Diidrogeno ha una temperatura di vaporizzazione di 20.27 K ed una temperatura di fusione di 14,02 K . Sotto pressioni molto elevate , come quelle che esistono al centro dei giganti gassosi , queste molecole si dissociano e l'idrogeno diventa un metallo liquido. Nello spazio, le nubi di H 2 sono alla base del processo di formazione stellare .
Storico
Il primo scienziato noto ad aver descritto la produzione di diidrogeno fu lo svizzero Paracelso (1493-1541). Fece questa scoperta versando del vetriolo sulla polvere di ferro , ma non comprese l'esatta natura del gas emesso durante l' esperimento .
Il chimico inglese Henry Cavendish (1731-1810), ripetendo gli esperimenti di Paracelso con diversi metalli , scopre che il gas così prodotto è diverso dall'aria, è infiammabile e ha una bassa densità. Ha chiamato questo gas "aria infiammabile" (in inglese: aria infiammabile ) e trova che il suo prodotto di combustione è dell'acqua . Il diossigeno essendo lui chiamato "aria vitale".
Il chimico francese Antoine Lavoisier, dopo aver confermato gli esperimenti di Cavendish, propone la parola "idrogeno" in sostituzione dell'espressione "aria infiammabile". Questa parola si forma con il prefisso hydro (dal greco ὕδωρ (hudôr), “acqua”) e il suffisso gene (dal greco γεννᾰν (gennen), “generare”). La parola idrogeno quindi significa che genera acqua .
Successivamente, in ambito scientifico, si utilizzerà la parola "idrogeno" per denominare l' elemento chimico H e la parola "idrogeno" per la molecola H 2 .
Proprietà chimiche
Test di riconoscimento
Per verificare la presenza di diidrogeno, un ceppo in fiamme viene avvicinato a una provetta contenente diidrogeno. La reazione chimica della combustione dell'idrogeno con l'ossigeno nell'aria, avviata dalla fonte di calore, produce un caratteristico rumore chiamato "abbaiare" o "abbaiare".
Combustione
La combustione dell'idrogeno in diossigeno , che produce acqua , è 2 H 2 (g) + O 2(g) → 2 H 2 O(l). È particolarmente violento (vedi test di riconoscimento) e molto esotermico : il suo potere calorifico è di 141,86 MJ/kg [o 141,79 MJ/kg ] (a 25 °C [o 15 °C ] sotto 1 atm ), ovvero un'entalpia standard di combustione , a 25 ° C , di -285,84 kJ / mol , a 100 ° C , di -283,45 kJ / mo l (H 2 gas, O 2 gas, ma H 2 O liquido , come potere calorifico superiore o PCS), ma di 120.1 MJ / kg [o 119.93 MJ / kg ], cioè un'entalpia di combustione, a 100 ° C , di -242,8 kJ / mol (H 2 gas, gassoso o 2 , H 2 o vapore , come potere calorifico inferiore o PCI , contando 40,660 kJ/mol per la vaporizzazione dell'acqua a 100 °C ), contro, ad esempio, solo 49,51 MJ/kg per il butano . Questa proprietà lo rende un carburante preferito per i veicoli spaziali, ma rende pericoloso il suo stoccaggio.
La stessa ossidazione più lenta viene utilizzata per produrre elettricità nella cella a combustibile .
Forme orto e para
L'idrogeno è una miscela di due tipi di molecole isomeriche che differiscono l'una dall'altra per lo spin dei loro nuclei atomici . Queste due forme sono chiamate orto- e para-idrogeno e la forma orto (spin paralleli, stato di tripletta) corrisponde a uno stato eccitato che non esiste allo stato puro. In condizioni normali di temperatura e pressione , per eccitazione termica, l'idrogeno è composto dal 75% della forma orto e dal 25% della forma para. A 77 K la miscela all'equilibrio (raggiunto spontaneamente in più giorni, ma in poche ore con catalizzatori) è al 50%. Ma a temperature molto basse, la forma orto si trasforma completamente nello stato para (spin antiparalleli, stato singoletto) nel tempo. Le due forme hanno livelli energetici leggermente diversi e quindi proprietà fisico-chimiche leggermente diverse . Ad esempio, il punto di fusione e il punto di ebollizione del para-idrogeno sono circa 0,1 K inferiori a quelli dell'orto- .
Fonti di idrogeno
Il diidrogeno è un gas molto leggero. Poiché la gravità terrestre non può trattenerlo, sfugge naturalmente dall'atmosfera terrestre. Pertanto, è presente solo in tracce (0,5 ppmv ) nell'aria . Questa scarsità atmosferica significa che tutto il diidrogeno utilizzato è prodotto industrialmente da vari processi, da molecole in cui gli atomi di idrogeno sono legati chimicamente.
Tuttavia, ci sono alcuni contesti geologici in cui il diidrogeno scaturisce naturalmente dalla Terra . L'idrogeno che emana da queste zone è designato con il termine idrogeno naturale .
Idrogeno artificiale
La produzione di idrogeno coinvolge molti processi diversi , l'atomo di idrogeno forma una serie di molecole ( acqua , idrocarburi , zuccheri , ecc .).
Metodo storico di produzioneStoricamente, nel XIX ° secolo, la diidrogeno è stato ottenuto mediante emissione di vapore acqueo (H 2 O) in un barile pieno di limatura di ferro e chip. Il vapore acqueo ha ossidato il metallo, creando ossido di ferro da un lato , rilasciando idrogeno dall'altro. Quest'ultimo ha poi lasciato la botte, dove è stato filtrato in un altro barile riempito d'acqua, poi stoccato direttamente in un aerostato . Questo dispositivo ha permesso all'esercito di gonfiare un pallone d'osservazione ovunque e in poche ore .
Metodi attualiNel 2015 l'idrogeno è stato prodotto industrialmente con vari processi:
- per il 49% da steam reforming da idrocarburi (in particolare da metano , vedi Reforming del metano );
- per il 29% per ossidazione parziale del petrolio
- per il 18% mediante gassificazione del carbone
- per il 4% mediante elettrolisi dell'acqua .
Sono allo studio anche altri processi, da cracking o ossidazione parziale, che ha il vantaggio di essere esotermico .
Riformazione del vapore di idrocarburiLa steam reforming di idrocarburi è il metodo che all'inizio del XXI ° secolo, è il più utilizzato a livello industriale. Il suo principio si basa sulla reazione degli idrocarburi (metano, ecc.) in presenza di vapore acqueo e calore. La reazione globale si scrive:
.L' efficienza energetica è di circa il 40-45% in alcuni impianti . Nella pratica industriale è necessario accelerare la reazione mediante catalizzatori o bruciatori. Ha lo svantaggio di produrre anidride carbonica , un gas serra .
Attualmente sono allo studio tecnologie catalitiche, o più innovative come i plasma reformer.
Elettrolisi dell'acquaL' elettrolisi dell'acqua è una tecnologia che consiste nel far passare una corrente elettrica (diretta) nell'acqua (a cui è stato precedentemente aggiunto un elettrolita come la soda caustica ) al fine di ottenere la dissociazione delle molecole d'acqua in idrogeno e ossigeno .
Reazione all'anodo :
2 H 2 O(l) → O 2(g) + 4 H + (acq) + 4 e -Reazione al catodo :
4 H 2 O(l) + 4 e - → 2 H 2 (g) + 4 OH - (aq)Reazione in acqua:
4 H + (acq) + 4 OH - (acq) → 4 H 2 O (l)Reazione generale:
2 H 2 O(l) → 2 H 2 (g) + O 2 (G)dove (l), (g) e (aq) significano rispettivamente "in fase liquida", "in fase gassosa" e "in soluzione acquosa".
Questa tecnologia richiede grandi quantità di elettricità. Secondo Ademe nel 2020, l'efficienza della catena dell'idrogeno in Power-to-H2-to-Power è del 25%, mentre quella delle batterie elettriche è del 70%. È quindi relativamente poco utilizzato.
Ossidazione parziale di idrocarburiQuesta reazione è una combustione “ricca” nel senso che lo scopo è produrre un gas ricco di H 2 e CO (gas di sintesi); al posto dei “classici” prodotti CO 2 e H 2 O.
La reazione è scritta:
.Il più delle volte, l'aria viene utilizzata come ossidante. Abbiamo quindi:
.La reazione è esotermica: per esempio, l'entalpia della reazione con il metano è -35,7 kJ mol -1 .
Come la reazione di steam reforming, è necessario catalizzare la reazione.
L'interesse della reazione di ossidazione parziale risiede nella sua natura esotermica (a differenza della reazione di steam reforming) che favorisce la catalisi (aumento di temperatura).
L'inconveniente maggiore risiede nel fatto che le percentuali di H 2 sono inferiori a quelle ottenute con il steam reforming, a causa della presenza maggioritaria di azoto nell'aria. Inoltre, c'è il rischio di ottenere NO x .
Azione di un acido su un metalloIl diidrogeno è prodotto dall'azione di un acido su un metallo. Esempio :
.Il diidrogeno può anche essere prodotto facendo reagire l'idrossido di sodio con l'alluminio, secondo la formula:
Produzione per fotosintesi (cianobatteri)Alcuni cianobatteri possono scindere chimicamente l'acqua in ossigeno e idrogeno mediante reazioni fotosintetiche. Ciò renderebbe possibile la produzione di idrogeno utilizzando l'energia solare . La ricerca è in corso in questo settore, in particolare in termini di ingegneria genetica .
Idrogeno naturale
L'idrogeno prodotto naturalmente sulla Terra , al contrario dell'idrogeno prodotto artificialmente riformando il metano o gli idrocarburi , si dice che sia idrogeno naturale o idrogeno nativo .
La distribuzione, la capacità produttiva e meccanismi fisico-chimiche delle sue fonti o depositi sono tuttora oggetto di studi esplorativi per l'inizio del XXI ° secolo. Così, nell'aprile 2019, è stato lanciato e cofinanziato dall'Agenzia spaziale europea il progetto di ricerca sen4H2 , che mira a rilevare le emissioni naturali di idrogeno utilizzando immagini satellitari.
Fonti di idrogeno naturaleLa produzione di idrogeno naturale nella spina dorsale è nota fin dagli anni '70 e studiata più di recente. Questi sono serpentinizzazione reazioni ( redox di olivina ) tra l'acqua e la rocce magmatiche filo con il manto terrestre , facilitata dal calore di queste reazioni esotermiche : l'ossigeno delle H 2 O molecole.catturati dal ferro nella roccia, gli atomi di idrogeno sono liberi di associarsi in H 2. L'idrogeno così prodotto fuoriesce attraverso bocche idrotermali e può opzionalmente reagire a sua volta per formare metano , quindi idrocarburi più pesanti. Troppo profondi, questi depositi non possono essere sfruttati nel 2018
Le emissioni di idrogeno sono state scoperte anche nel mezzo dei cratoni continentali dal geologo russo Nicolay Larin, in seguito al suo lavoro sull'ipotesi della Terra idratata. L' IFP Energies nouvelles ha confermato questa scoperta nel 2013, riportando questioni importanti a livello locale, nella maggior parte dei continenti, in Russia , negli Stati Uniti , in Brasile , in Oman o Mali .
Il fenomeno è ancora poco conosciuto e il dibattito sull'esatto meccanismo che genera queste emissioni non è stato ancora definito. Potrebbe trattarsi dell'idratazione del ferro da parte dell'acqua infiltrata, questa essendo presente nelle cinture di pietra verde , presenti nei cratoni. Così, in Kansas , nei pressi di Junction City , è stato individuato un deposito negli anni Ottanta ed è stato oggetto di rinnovato interesse negli anni Duemila; il diidrogeno vi si otterrebbe da tali reazioni di ossidazione del ferro. In Russia, l'IFP ha stimato nel 2010 il flusso giornaliero di una singola depressione a diverse decine di migliaia di metri cubi , ovvero il consumo equivalente di 500 taxi. Un originale geologico o idrogeologico prevale anche per i rilasci di idrogeno studiati in Brasile, in alcuni circoli fatati situati nel bacino di São Francisco .
A Yanartaş , in Turchia, i “fuochi millenari” del Monte Chimera sarebbero la combustione di un gas composto da metano (87%), idrogeno (7,5-11%) e diazoto ( 2-4,9 %), avente una doppia origine: il serpentinizzazione da un lato, un gas termogenico dall'altro. Sarebbero la fonte originale della fiamma olimpica .
Il Mali è, nel 2015, l'unico paese in cui viene utilizzato l'idrogeno naturale, nel villaggio di Bourakébougou , 60 chilometri a nord di Bamako . Il gas proverrebbe da una "sovra maturazione del petrolio" probabilmente interrata nelle vicinanze e le sue riserve sono stimate in circa 1,5 miliardi di metri cubi . La pressione nei pozzi non diminuisce, quindi il riempimento viene costantemente riempito, il che consente la sostenibilità di questa operazione.
I gas vulcanici contengono spesso tracce di idrogeno. Così, alle Hawaii, uno studio spettroscopico condotto su un incendio di gas vulcanico ha mostrato che si trattava di una combustione di diidrogeno.
Qualsiasi roccia ignea conterrebbe idrogeno, fino a circa 5 l/m 3 ; pertanto, tutti i pozzi mostrano degassamento dell'idrogeno. Durante l'esperimento russo di perforazione sg3 , il fango estratto dal foro è stato descritto come gorgogliante con questo gas .
SfideA differenza dell'idrogeno artificiale, che per essere prodotto necessita di energia, che lo riduce ad essere solo un vettore energetico , l'idrogeno naturale è una vera e propria fonte di energia , la cui combustione non produce solo acqua. Inoltre, potrebbero essere possibili coproduzioni con energia geotermica o estrazione di elio , che potrebbero aiutare il settore a essere competitivo. Tuttavia, nel 2020 il potenziale industriale non è quantificato con precisione e la legislazione mineraria non tiene conto dell'idrogeno in molti paesi. La rivelazione dell'idrogeno in situ è infatti difficile sebbene siano stati sviluppati rivelatori più efficienti.
Usi industriali
Il consumo globale di idrogeno oggi è di circa 50 milioni di tonnellate all'anno. La maggior parte della produzione di idrogeno viene consumata in loco, principalmente nell'industria chimica e petrolchimica: sintesi dell'ammoniaca (50%), raffinazione e desolforazione degli idrocarburi (37%), sintesi del metanolo (12%).
I principali usi industriali dell'idrogeno sono:
- il metodo Haber-Bosch (produzione di ammoniaca ), l' idrogenazione di grassi e oli e la produzione di metanolo ;
- la fabbricazione di acido cloridrico , la saldatura , i combustibili per razzi e la riduzione di minerali metallici;
- il diidrogeno liquido viene utilizzato per ricerche a temperature molto basse, compreso lo studio della superconduttività ;
- l'idrogeno è utilizzato come gas tracciante per eseguire operazioni di rilevamento perdite in vari campi (raffinazione del petrolio, automobili, impianti di riscaldamento, rete di distribuzione idrica, serbatoi di aeromobili, ecc.);
- l'idrogeno è un additivo alimentare autorizzato con il codice E949 , nella categoria dei traccianti;
- l'idrogeno è anche utilizzato come fluido termovettore in alcune macchine ad alta potenza (alternatore sincrono di centrali, ad esempio);
- l'idrogeno è stato utilizzato negli aerostati perché è quattordici volte meno denso dell'aria, ma è stato sostituito dall'elio per ragioni di sicurezza; è ancora utilizzato per alcuni palloni meteorologici in stazioni remote.
- Il diidrogeno è stato testato come carburante per l'aeronautica durante un volo il 15 aprile 1988 con il Tupolev Tu-155.
Alcuni isotopi dell'idrogeno hanno anche un particolare uso industriale o tecnologico:
- il deuterio ( 2 H) viene utilizzato nelle applicazioni nucleari come moderatore ( acqua pesante o D 2 O) per rallentare i neutroni . I composti del deuterio sono utilizzati anche in chimica e biologia per studiare o utilizzare l' effetto isotopico ;
- il trizio ( 3 H) un altro isotopo, viene prodotto nei reattori nucleari e viene utilizzato per la costruzione di bombe atomiche . Viene anche utilizzato come marcatore isotopico nelle bioscienze e come fonte di radiazioni nelle vernici luminescenti;
- deuterio e trizio sono anche fusi nei reattori di ricerca e considerati per progetti di fusione nucleare controllata sulla Terra.
Ad oggi, vengono prese in considerazione tre principali modalità di stoccaggio dell'idrogeno a bordo di un veicolo:
- stoccaggio sotto forma di gas compresso;
- conservazione in forma liquida a bassa temperatura;
- stoccaggio in forma solida, l'idrogeno essendo poi legato ad altri componenti (per adsorbimento o sotto forma di composto chimico).
Gas compresso
È la forma più comune di stoccaggio dell'idrogeno.
Lo stoccaggio del gas in forma compressa (attualmente 350 bar) consente di raggiungere una densità di massa soddisfacente con serbatoi compositi. La densità del volume di stoccaggio rimane bassa: una pressione di 700 bar è inevitabile per rendere competitiva la tecnologia.
La tecnologia esiste ed è comunemente usata. Il suo svantaggio risiede nell'energia necessaria per la compressione e nella bassa efficienza in termini di dimensioni rispetto ad altri metodi. Questo ingombro è una delle difficoltà per l'uso del diidrogeno sotto forma di gas compresso nelle applicazioni automobilistiche.
Quando compresso, la densità dell'idrogeno a 20 MPa ( 200 bar) è di circa 16,8 kg/m 3 , a 35 MPa ( 350 bar) di circa 23 kg / m 3 ea 70 MPa ( 700 bar) ) di circa 38 kg / m 3 . Ciò corrisponde a una densità di energia di 767 kWh/m 3 (27 ° C, 35 MPa) e ancora a una densità di energia di 33,3 kWh/kg.
Lo stoccaggio di liquidi a 20 K ( -253 ° C ) sotto i 10 bar consente di raggiungere densità di volume e di massa interessanti ma richiede serbatoi con elevato isolamento termico per ridurre al minimo l'evaporazione.
La tecnologia c'è. Ha una migliore efficienza volumetrica rispetto allo stoccaggio di gas compresso ( 70 kg/m 3 contro 10 kg/m 3 a 115 bar e 0 °C ). Tuttavia, questo vantaggio è moderato dal volume relativamente grande dei necessari involucri isolanti.
Per passare alla fase liquida è invece necessaria una notevole quantità di energia: la liquefazione consuma dal 30 al 40% del contenuto energetico del gas e la perdita nell'uso reale è significativa (attualmente 1,25 per mille all'ora), fortemente penalizzando lo stoccaggio oltre la settimana.
Questa tecnica è utilizzata in particolare nel settore spaziale dove, nonostante i brevi tempi di realizzazione, il riempimento è continuo fino all'ultimo momento.
Idruri metallici
Lo stoccaggio su substrati in forma adsorbita, in particolare su idruri metallici, ha una densità di volume molto interessante ma una bassa densità di peso. Inoltre, la cinetica, la temperatura e la pressione ciclica rimangono punti difficili da controllare.
Gli atomi di idrogeno sono immagazzinati in alcuni composti metallici. L'idrogeno viene recuperato riscaldando o riducendo la pressione. Questa tecnica è poco conosciuta oggi. Ha lo svantaggio di richiedere un diidrogeno estremamente puro per evitare di distruggere la capacità di assorbimento degli idruri. Anche il riscaldamento per recuperare il gas è un handicap. Questo tipo di stoccaggio, che continua ad essere oggetto di ricerca, è in fase di sviluppo industriale e sono previsti alcuni progetti dimostrativi, ad esempio con la start-up McPhy che sta sviluppando la tecnologia dell'idruro di magnesio (tecnologia del CNRS, NEEL Institute) .
Capacità di stoccaggio di alcuni idruri.
| idruro | Percentuale di massa del contenuto di H 2 |
|---|---|
| LaNi 5 H 6.5 | 1.4 |
| ZnMn 2 H 3.6 | 1.8 |
| TiFeH 2 | 1.9 |
| Mg 2 NIH 4 | 3.6 |
| VH 2 | 3.8 |
| MgH 2 | 7.6 |
Un metallo molto studiato è il palladio che, tramite il suo idruro PdH 2, ha la capacità di assorbire una grande quantità di idrogeno all'interno del suo reticolo cristallino. A temperatura ambiente e pressione atmosferica, il palladio può assorbire fino a 900 volte il suo volume di gas idrogeno, essendo il processo reversibile.
L' adsorbimento su carbonio permette di immagazzinare sulla superficie di alcune strutture di carbonio , come il carbone attivo oi nanotubi , le molecole di idrogeno. Consente di immagazzinare dallo 0,05 al 2% in massa di diidrogeno .
Questo tipo di archiviazione è in fase di ricerca.
Produzione e usi
In un rapporto pubblicato su giugno 2019, l' Agenzia internazionale per l'energia rileva la versatilità dell'idrogeno, che può essere prodotto da tutti i combustibili fossili, rinnovabili e nucleare, può essere trasportato in forma gassosa o liquida ed essere trasformato in elettricità o in metano per una vasta gamma di usi.
Possiamo distinguere tre categorie di idrogeno prodotto, a seconda di come viene prodotto (vedi la sezione Metodi correnti ):
- l' idrogeno grigio , prodotto dalla conversione di combustibili fossili senza cattura e stoccaggio del carbonio ;
- l' idrogeno blu , prodotto dalla conversione dei combustibili fossili con cattura e stoccaggio del carbonio;
- l' idrogeno verde prodotto dall'energia elettrica da fonti rinnovabili o nucleare ( viola per alcuni, giallo per altri).
L'idrogeno prodotto nella crosta terrestre (per diagenesi e radiolisi ), così come l'idrogeno primordiale (presente fin dalla formazione della Terra ) sono altre fonti possibili, ma non ancora esplorate.
Nel 2020 il costo dell'idrogeno grigio è compreso tra 1 e 2 €/kg contro i 4-7 €/kg dell'idrogeno verde prodotto in maniera industriale. Secondo Julien Chauvet, direttore di Hydrogen France di Engie Solutions , "il chilo permette di percorrere 100 km il che lo mette alla pari con la benzina ed è simile al diesel per veicoli leggeri" .
Produzione industriale
L'idrogeno è attualmente prodotto quasi interamente da gas naturale , petrolio e carbone .
Per le proprie esigenze, l'industria produce idrogeno ( es: in Francia, più di 900.000 t/anno di idrogeno, in particolare per la desolforazione dei combustibili petroliferi e per produrre ammoniaca nei fertilizzanti nitrati ; l'idrogeno è quindi un input chimico e non un'energia vettore ). Il processo industriale più economico per produrre questo idrogeno, nel 2018, è il reforming degli idrocarburi , il più delle volte mediante steam reforming del gas naturale (che è composto principalmente da metano ). Ad una temperatura compresa tra 700 e 1.100 °C , il vapore acqueo reagisce con il metano per dare monossido di carbonio e idrogeno. La purificazione dell'idrogeno essendo più facile ad alta pressione, il reforming viene effettuato ad una pressione di venti bar . La miscela idrogeno/monossido di carbonio è comunemente indicata come " gas di sintesi ". Se la reazione avviene in presenza di vapore acqueo in eccesso, il monossido di carbonio viene ossidato al livello di ossidazione più elevato, portando ad anidride carbonica , che aumenta la produzione di idrogeno .
L'azienda Air Liquide ha una padronanza particolare di questo processo. Nel 2015, è messa in Arabia Saudita , al Yanbu sito , un'unità con una capacità di produzione di idrogeno complessiva di 340.000 m 3 / h alla CNTPs .
Nel 2019, l'Australian Renewable Energy Agency (ARENA) fornirà 9,41 milioni di dollari australiani (8,5 M€ ) a un progetto del gruppo Hazer (società australiana di energie rinnovabili) volto a convertire il biogas dalla metanizzazione dei fanghi di depurazione in idrogeno e grafite . Hazer vuole costruire un impianto dimostrativo da 15,8 milioni di dollari a Munster (Australia occidentale).
Settore dell'idrogeno e sfide per lo sviluppo sostenibile
La produzione industriale “tradizionale” di idrogeno da idrocarburi fossili ha una scarsa impronta di carbonio ed emette molti gas serra , arrivando a 830 milioni di tonnellate di CO2 .all'anno nel 2020, ovvero circa il 2% delle emissioni globali e quasi quanto il settore dell'aviazione o del trasporto marittimo. In Francia, queste emissioni ammontano a quasi dieci milioni di tonnellate di CO 2 equivalente.all'anno intorno al 2015-2017, ovvero il 7,5% delle emissioni di gas serra dell'industria francese, secondo ADEME . La produzione di idrogeno da energia elettrica rinnovabile, più virtuosa, potrebbe vedere il suo costo scendere del 30% entro il 2030 grazie al boom delle energie rinnovabili e delle relative economie di scala .
Il settore dell'idrogeno produce, immagazzina, promuove e potenzia la ricerca sull'idrogeno e sull'idrogeno. Nel 2015 sono in corso esperimenti con idrogeno verde (carbon free), ma questo gas è ancora "prodotto principalmente da gas naturale ( fossile ) e utilizzato come componente chimico nei processi industriali" , con uno scarso bilancio del carbonio e un contributo significativo alla effetto serra . Il settore si presenta comunque come interessante per lo sviluppo sostenibile , Perché:
- se prodotta per elettrolisi dell'acqua e in maniera carbon free recuperando eccedenze intermittenti di elettricità rinnovabile (principalmente eolica e fotovoltaica), questo vettore energetico può essere immagazzinato, in particolare nei cicli interstagionali, quindi utilizzato in metanazione e/o immesso nella rete del gas (dal 6 al 20% in volume a seconda delle condizioni), facilitando così l'equilibrio e la flessibilità della rete elettrica ;
- l'elettricità accumulabile grazie alla sua trasformazione in gas (idrogeno o metano) permetterebbe di accumulare “dell'ordine di un terrawattora all'anno” e fino a diverse decine di terawattora all'anno di elettricità secondo l'ADEME , quando il tasso di penetrazione delle energie rinnovabili nel mix elettrico raggiungerà l'80%, e come tale potrebbe "dare un importante contributo alla transizione verso un modello energetico a basse emissioni di carbonio, in particolare nel settore dello stoccaggio dell'energia" ;
- l'idrogeno può essere utilizzato per produrre energia elettrica localmente, ma con una perdita di efficienza; quella dell'elettrolisi dell'acqua si avvicina al 70%, ma l'efficienza complessiva della produzione di energia elettrica da H 2 sarebbe intorno al 25% secondo Ademe nel 2020;
- l'idrogeno è compatibile con l' autoconsumo di una casa, isola o quartiere, consentendo lo stoccaggio per più giorni, settimane o mesi, oltre alle batterie più utili per lo stoccaggio a breve termine. Sarebbe già giustificato economicamente Nelle aree non interconnesse alla rete elettrica continentale ( es.: isole isolate, comunità francesi d'oltremare dove la produzione di energia elettrica dipende ancora da combustibili ad alto costo, a 225 €/MWh in media nel 2013 secondo all'ADEME);
- l'idrogeno può alimentare alcune flotte di veicoli professionali, senza richiedere una costosa rete di diverse centinaia di stazioni di servizio in tutto il paese. Secondo Ademe, "il modello economico di una stazione per una flotta è accessibile per un consumo giornaliero superiore a 80 kg H 2 / giorno, per la commercializzazione dell'idrogeno a meno di 10 € / kg " . In questo caso ha i vantaggi di un tempo di ricarica veloce e di una grande autonomia;
- l'idrogeno può essere utilizzato nell'industria siderurgica in sostituzione del carbone o del gas naturale per la riduzione del minerale di ferro. Utilizzando questo processo in Francia si consumerebbero 700.000 tonnellate di idrogeno, ma si eviterebbe l'emissione Di 22 MtCO 2/ anno, o quasi il 5% delle emissioni del paese, indica l'Associazione francese per l'idrogeno e le celle a combustibile (Afhypac).
il 8 luglio 2020, la Commissione Europea presenta un programma per lo sviluppo dell'idrogeno verde, fissando l'obiettivo che l'idrogeno copra dal 12 al 14% del fabbisogno energetico entro il 2050 al fine di decarbonizzare alcuni settori dell'industria e dei trasporti. Si affida all'idrogeno per contribuire alla transizione energetica e alla riduzione delle emissioni di gas serra. Allo stesso tempo, il commissario europeo per il commercio interno, Thierry Breton, annuncia la creazione dell'alleanza dell'idrogeno.
In FranciaL' ADEME sta valutando un mix elettrico al 40% composto da “rinnovabile” nel 2035, poi al 60% e 70% nel 2050 (contro quasi il 18% nel 2017, mentre la maggior parte da fonte idroelettrica).
Il settore cerca di industrializzare i suoi processi per ridurre i suoi costi (in particolare quello della cella a combustibile ). Lo sviluppo della “mobilità a idrogeno” è inoltre ostacolato da un numero ancora molto basso di stazioni di ricarica (e dalla loro ancora bassa capacità: da 10 a 80 kg H 2 / gg a 350 bar). L'idrogeno può migliorare la potenza del veicolo, estenderne l'autonomia e migliorare la velocità di ricarica, rispetto alle batterie.
Ademe ritiene che l'idrogeno avrà un ruolo importante nella transizione energetica, come vettore per l'ottimizzazione delle reti energetiche, per lo stoccaggio di energia nell'autoconsumo solare o fotovoltaico, e per alcuni veicoli professionali, a condizione che ne decarbonizzi la produzione di energia attraverso l'elettrolisi. utilizzo di elettricità verde e trasformazione della biomassa ( steam reforming del biogas , pirogassificazione della biomassa solida). La performance ambientale del settore dipenderà soprattutto dalla “fonte primaria utilizzata per produrre idrogeno”. L'agenzia chiede di limitare a meno di cento chilometri la distanza di trasporto dell'idrogeno tra il punto di produzione e la stazione di distribuzione. I veicoli a batteria dovrebbero essere preferiti, quando possibile (autonomia, disponibilità, ecc.), viste le migliori prestazioni di questo tipo di accumulo, e il risparmio energetico rimane una priorità. Una delle strade di sviluppo (attualmente in fase di sperimentazione nel 2018/2019) è l'iniezione nella rete del gas in Francia tramite due dimostratori: GRHYD e Jupiter 1000 , per rimuovere le barriere tecniche ancora esistenti.
Nel giugno 2018, il governo francese dà mandato ad Ademe di varare il "piano nazionale di impiego dell'idrogeno" (o "piano idrogeno"), per dare slancio a questo settore il cui "alto potenziale" è percepito dagli attori pubblici. L'obiettivo del governo è "creare un settore industriale francese carbon free, aprire nuove prospettive per lo stoccaggio delle energie rinnovabili e sviluppare soluzioni a zero emissioni per i trasporti" . Un anno dopo, l'ente pubblico ha lanciato più bandi per progetti , tra cui "Ecosistemi di mobilità a idrogeno", che hanno permesso di selezionare progetti "in tutti i territori" e diversificati, come "la consegna dell'ultimo miglio in aree urbane. , il trasporto collettivo di passeggeri da parte di bus o navette marittime, noleggio auto, raccolta rifiuti, flotte aziendali e comunitarie, o anche l'utilizzo di mezzi pesanti come mezzi da cantiere” .
Il CEA promette una nuova tecnologia di elettrolisi industriale, denominata rSOC con un unico metallo prezioso: l' indio (un metallo utilizzato negli schermi LCD ), con temperature più basse (da 700 °C a 800 °C ) e un minor consumo di energia. È anche reversibile, consentendo di produrre idrogeno o di ripristinare l'energia elettrica come una cella a combustibile.
Alla fine del 2019, Air Liquide ed Engie hanno unito le forze con Durance-Luberon-Verdon Agglomeration (DLVA) per produrre, immagazzinare e distribuire "idrogeno verde" (nell'ambito del progetto "HyGreen Provence" lanciato nel 2017, che mira a 1.300 GWh di elettricità solare e diverse migliaia di tonnellate: anno di idrogeno prodotto dall'elettrolisi A lungo termine potrebbero essere prodotte diverse decine di migliaia di tonnellate di idrogeno rinnovabile all'anno, che possono essere immagazzinate in una cavità salina locale.
La società francese McPhy , che ha già installato 17 MW di capacità di produzione di idrogeno mediante elettrolisi pressurizzata, di cui 6 MW presso Audi in Germania, annuncia a gennaio 2020 la firma del contratto di ingegneria per un progetto di produzione di idrogeno verde industriale da 20 MW , il più grande progetto fino ad oggi in Europa, situato a Delfzijl nei Paesi Bassi entro il 2022. L'impianto produrrà 3.000 tonnellate di idrogeno all'anno mediante elettrolisi dell'acqua utilizzando l'energia eolica e sarà utilizzato per produrre bioetanolo. Il progetto beneficia di 15 milioni di euro di sovvenzioni dall'Unione Europea e da un fondo olandese. Secondo McPhy, la scala giusta sarà 100 o 200 MW per ottenere un prezzo competitivo nel settore.
La legge sull'energia e il clima del novembre 2019 concede al governo un anno per istituire un meccanismo di sostegno per "l'idrogeno prodotto da energia rinnovabile o per elettrolisi dell'acqua utilizzando elettricità a basse emissioni di carbonio" . Prima del 2023, il programma energetico pluriennale mira a decarbonizzare il 10% dell'idrogeno consumato nell'industria, che richiede la produzione di 90.000 tonnellate di idrogeno verde. A gennaio 2020, il governo lancia un invito a manifestare interesse , destinato a testare l'appetito degli industriali per l'argomento, che riceve più di 160 progetti. Ad esempio, a gennaio H2V Industry ha depositato le domande di permesso di costruire per due impianti di produzione di idrogeno nell'area industriale di Port-Jérôme, in Normandia, e sul grande porto marittimo di Dunkerque da elettricità rinnovabile; se riusciranno a beneficiare di un meccanismo di supporto, la loro messa in servizio potrebbe avvenire nel 2023-2024 e produrrebbero 56.000 tonnellate di idrogeno. Si sono posizionati anche i maggiori player industriali francesi (Engie, EDF, Air Liquide, Vinci, ecc. ).
Il governo Castex ha annunciato a settembre 2020 un piano molto più ambizioso di quello presentato da Nicolas Hulot nel 2018, dotato di 100 milioni di euro: il piano 2020 prevede di destinare 7,2 miliardi di euro entro il 2030 all'idrogeno green o low carbon, di cui 2 miliardi di euro in 2021 e 2022 nell'ambito del piano di risanamento. Il governo prevede di sovvenzionare la produzione di idrogeno verde attraverso gare d'appalto, modellate sulle energie rinnovabili, e la costruzione di impianti di celle a combustibile per veicoli a idrogeno. Al fine di evitare duplicazioni, sono allo studio partnership con la Germania, che a giugno ha presentato un piano per l'idrogeno da 9 miliardi di euro.
Questo piano per l'idrogeno prevede una prima componente di 1,5 miliardi di euro dedicata alla produzione di elettrolizzatori, al fine di ridurre il costo migliorandolo e aumentando i volumi, per una capacità di 6,5 GW . La seconda componente di quasi un miliardo di euro sarà utilizzata entro il 2023 per sviluppare un'offerta di mobilità pesante a idrogeno riducendo i costi e migliorando l'efficienza delle celle a combustibile per treni, camion, autobus e aerei, attraverso diversi bandi (350 milioni di euro per dimostratori, 275 milioni per esperimenti regionali, ecc.). Infine, saranno incentivati gli aiuti alla ricerca e all'innovazione, con una dotazione portata a 650 milioni entro il 2023. Bruno Le Maire auspica che questo piano crei tra i 50.000 ei 150.000 posti di lavoro diretti e indiretti. Il governo sta valutando una cooperazione con la Germania descritta come "Airbus per l'elettrolisi" come "Airbus per batterie". La Francia si è posta l'obiettivo di produrre 600.000 tonnellate all'anno di idrogeno verde, da elettricità senza emissioni di carbonio, di origine rinnovabile o nucleare. A differenza della Germania, Parigi, tuttavia, non sovvenzionerà la cattura del carbonio dall'idrogeno “grigio”. Bruno Le Maire auspica "l'emergere di un settore dell'elettrolisi francese": accanto a colossi come Air Liquide, numerose sono anche le start-up, come Lhyfe , con sede a Nantes, che sta sviluppando siti di produzione di idrogeno verde per produttori ed enti locali, o anche McPhy , un produttore Drôme di elettrolizzatori di cui EDF è azionista.
In BelgioUn team di KUL sta progettando un prototipo di cella fotoelettrochimica da 1,6 m 2 che produce una media di 250 litri di idrogeno al giorno dal vapore acqueo atmosferico. Il dispositivo converte il 15% dell'energia solare in idrogeno e ossigeno. E questa tecnologia non utilizza metalli preziosi o altri materiali costosi. Con venti pannelli una casa ben coibentata sarebbe autosufficiente in elettricità e riscaldamento per un anno.
Colruyt Group (un importante rivenditore belga) vuole decarbonizzare il più possibile le sue attività. Nel 2018 uno dei suoi centri logistici è stato dotato di 75 ascensori alimentati a idrogeno “carbon free” e la sua flotta di camion deve essere riconvertita entro il 2030. Con un player del gas è in preparazione un progetto di installazione da 12 a 25 MW (espandibile) convertire l'energia elettrica da turbine eoliche offshore in idrogeno , su scala industriale.
In GiapponeA fine 2017 il Giappone, importante importatore di energia, ha confermato di voler diventare leader come “ società dell'idrogeno ” con un obiettivo di “cost parity” con benzina e GNL per la produzione di energia elettrica. Come per il nucleare in passato, l'idrogeno è presentato come uno dei principali mezzi di decarbonizzazione dell'energia, ma i progetti pilota trarranno le loro conclusioni intorno al 2020. Nel 2018, il Giappone è in testa alla mobilità dell'idrogeno, con quasi 2.500 auto con celle a combustibile a idrogeno in circolazione e più di cento stazioni di idrogeno (rispetto alle 45 in Germania, 42 negli Stati Uniti e circa 20 in Francia contemporaneamente). Il Paese punta a dividere il costo di produzione di oltre tre prima del 2030, quindi dell'80% prima del 2050. Tra il 2013 e il 2017, lo stato giapponese ha già investito 1,5 miliardi di dollari in R&S e sviluppo dell'idrogeno.
In CaliforniaNel ottobre 2019, la California ha 7.570 auto a idrogeno immatricolate e 42 stazioni pubbliche statunitensi.
In GermaniaIl governo tedesco adotta un ambizioso piano per lo sviluppo dell'idrogeno “verde”, dotato di 9 miliardi di euro.
Motore a idrogeno
Fusione nucleare: bomba H e reattori a fusione
Pericoli, rischi e precauzioni
Il diidrogeno è un gas classificato come "estremamente infiammabile ". È caratterizzato da un campo di infiammabilità molto ampio (dal 4 al 75% del volume in aria), provocando una deflagrazione da un apporto di energia di attivazione molto basso (una scintilla è sufficiente se fornisce un'energia di 0,02 millijoule (mJ) mentre ci vogliono 0,29 mJ per innescare un'esplosione di metano ). Il diidrogeno miscelato con l'ossigeno in proporzioni stechiometriche è un potente esplosivo . Diidrogeno in aria è esplosiva miscela quando l'H 2 / aria rapporto in volume è compreso tra il 13 e il 65%
La storia del suo utilizzo nei dirigibili è disseminata di gravi incidenti, il più famoso dei quali è il disastro di Hindenburg . Lo zeppelin LS 129 , gonfiato con 200.000 metri cubi di idrogeno (perché gli Stati Uniti avevano dichiarato un embargo contro la Germania per l' elio ) bruciò il6 maggio 1937all'arrivo a Lakehurst Airfield , vicino a New York ). Morirono 36 persone su 97 imbarcate. I media presenti hanno ampiamente divulgato le immagini del disastro, che ha portato alla disaffezione del pubblico nei confronti dei palloni. Le indagini sull'origine dell'incidente, agevolate dall'abbondanza di documenti fotografici, non hanno però incriminato un'esplosione di idrogeno, ma un'accensione per contiguità, da un incendio nell'involucro (probabilmente causato da scarica di elettricità statica). La composizione del rivestimento impermeabile dell'involucro (butirrati e alluminio) avrebbe favorito una violenta reazione alluminotermica . Tuttavia, l'incidente sarebbe stato molto meno violento se il pallone fosse stato gonfiato con l'elio.
La sostituzione dell'idrogeno con l' elio (molto più costoso e più denso) non ha prodotto l'atteso risveglio di favore. La paura dell'idrogeno rimase; la “sindrome di Hindenburg” ha probabilmente penalizzato ingiustamente il settore.
Il diidrogeno reagisce ancora più violentemente con il cloro per formare acido cloridrico (HCl), anche senza attivazione, e con il difluoruro per formare pericoloso acido fluoridrico (HF), anche a temperature dove l'idrogeno è liquido e il fluoro solido, quest'ultima reazione essendo la più esotermica reazione c'è .
Gli standard di sicurezza sono rafforzati per far fronte ai rischi posti dal passaggio in galleria e dalla sosta in autorimesse o parcheggi sotterranei.
Le normative globali sui veicoli vengono sviluppate sotto gli auspici delle Nazioni Unite sulla base delle proposte dei produttori, ma per quanto riguarda il diidrogeno, i produttori giapponesi, americani ed europei non sono d'accordo. La Commissione Europea potrebbe decidere su regolamenti comunitari provvisori.
In Francia, INERIS e CEA collaborano con l'Organizzazione internazionale per la standardizzazione ( ISO ) in un comitato tecnico denominato TC 197 sul rischio da idrogeno. Del tema si occupa anche un progetto europeo Hysafe , dove INERIS ha criticato la bozza di regolamento suggerendo un approccio più globale e sistemico e non per componenti per l'omologazione dei veicoli ibridi . Nel 2015 MEDDE ha predisposto un aggiornamento delle normative per le stazioni di servizio e le flotte di veicoli alimentati a idrogeno.
Pericolo da strato di ozono
Un massiccio rilascio di gas idrogeno ha sollevato l'ipotesi di un rischio per lo strato di ozono .
Misure di sicurezza
Si segnalano i seguenti punti:
- l'idrogeno non è intrinsecamente tossico;
- è otto volte più leggero del metano. La sua piccolissima molecola gli conferisce un ottimo coefficiente di diffusione nell'aria (quattro volte quello del metano); in un ambiente non confinato, quindi, l'idrogeno tende a salire ea diluirsi rapidamente nell'aria (è un fattore di sicurezza all'aria aperta, e un fattore di pericolo nei luoghi confinati);
- è la specie chimica più energetica per unità di massa (120 kJ/g ); ma per unità di volume di gas, l'energia esplosiva teorica è 3,5 volte inferiore per l'idrogeno rispetto al gas naturale;
- il suo limite inferiore di accensione è del 4% in volume, paragonabile a quello del gas naturale (5% in volume); ma il suo limite superiore di infiammazione è significativamente più alto (75% contro 15%); ciò significa che in caso di perdita, l'idrogeno si accenderà molto più facilmente del gas naturale o dei combustibili liquidi;
- anche l'energia necessaria per accenderlo alla stechiometria è significativamente inferiore (circa 10 volte) rispetto al gas naturale o al propano;
- la fiamma dell'idrogeno, azzurra, è quasi invisibile di giorno (rischio per i soccorsi);
- la fiamma dell'idrogeno si propaga circa sette volte più velocemente di quella del gas naturale e il rischio di detonazione (esplosione con effetto esplosione molto forte) è aggravato dal suo alto coefficiente di diffusività.
L'infiammabilità può essere ulteriormente ridotta diluendo l'idrogeno nell'elio, anche a temperature molto elevate.
Riferimento ONU per il trasporto di merci pericolose
- Nome (francese): idrogeno compresso
- Classe: 2
- numero: 1049
- Nome (francese): idrogeno liquido refrigerato
- Classe: 2
- numero: 1966
- Nome (inglese): Idrogeno in un dispositivo di stoccaggio a idruri metallici
- Classe: 2
- numero: 3468
Note e riferimenti
- HYDROGENE , scheda/e di sicurezza del Programma internazionale sulla sicurezza delle sostanze chimiche , consultata il 9 maggio 2009
- massa molecolare calcolata da " Pesi atomici degli elementi 2007 " su www.chem.qmul.ac.uk .
- (en) David R. Lide, CRC Handbook of Chemistry and Physics , CRC Press Inc,2009, 90 ° ed. , 2804 pag. , Copertina rigida ( ISBN 978-1-4200-9084-0 ).
- Jean-Louis Vignes ( dir. E membro della Società Chimica di Francia) et al. , " Dihydrogen: Physico-Chemical Data " , Sito di promozione e formazione relativo agli elementi chimici (dalla tavola periodica di Dmitri Mendeleïev ), su lelementarium.fr , Paris & Puteaux , Société Chimique de France & France Chimie (consultato il 3 novembre 2019 ) .
- Pierre Ravarini (ingegnere chimico e idrologo), " Gaz-Hydrogen " , sito di informazioni scientifiche, tecniche ed ecologiche sull'acqua, Côte de Nacre ( Calvados ), 2019(consultato il 3 novembre 2019 ) .
- (in) James E. Mark, Manuale delle proprietà fisiche del polimero , Springer,2007, 2 ° ed. , 1076 pag. ( ISBN 978-0-387-69002-5 e 0-387-69002-6 , leggi in linea ) , p. 294
- (en) Robert H. Perry e Donald W. Green , Perry's Chemical Engineers' Handbook , USA, McGraw-Hill,1997, 7 ° ed. , 2400 pag. ( ISBN 0-07-049841-5 ) , pag. 2-50
- " Proprietà di vari gas " , su flexwareinc.com (consultato il 12 aprile 2010 )
- Verbale del Comitato internazionale dei pesi e delle misure , 78 ° Sessione, 1989, pp. T1-T21 (e pag. T23-T42, versione inglese).
- (in) W. M Haynes, Handbook of Chemistry and Physics , CRC, 2010-2011 91 ° ed. , 2610 pag. ( ISBN 978-1-4398-2077-3 ) , pag. 14-40.
- (in) David R. Lide , CRC Handbook of Chemistry and Physics , Boca Raton, CRC Press,18 giugno 2002, 83 ° ed. , 2664 pag. ( ISBN 0849304830 , presentazione online ) , p. 5-89
- Magalie Roy-Auberger, Pierre Marion, Nicolas Boudet, Gassificazione del carbone , ed. Tecniche dell'Ingegnere, riferimento J5200 , 10 dicembre 2009, p. 4
- " Office of Radiation, Chemical & Biological Safety (ORCBS) " (consultato il 16 aprile 2009 )
- Regolamento CE n . 1272/2008 , 16 dicembre 2008 [PDF] su EUR-Lex , pag. 923 : allegato VI, tabella 3.1, numero indice .
- " Idrogeno " nel database dei prodotti chimici Reptox del CSST (organizzazione del Quebec responsabile per la sicurezza e la salute sul lavoro), accesso 23 aprile 2009
- "idrogeno" , su ESIS , consultato il 15 febbraio 2009
- “ La scoperta delle fonti di idrogeno apre la strada a una nuova energia ” , Le Monde .
- “ Idrogeno naturale, un Eldorado energetico? » , Scienze et Avenir .
- Esperimenti di Lavoisier , su lavoisier.cnrs.fr
- " Energia idrogeno " , sulla Conoscenza delle Energie ,30 agosto 2011(consultato il 10 dicembre 2019 ) (aggiornato9 aprile 2015).
- resa catena idrogeno (scheda tecnica), Ademe ,gennaio 2020( leggi online [PDF] ).
- " Rilevazione delle emanazioni di idrogeno naturale mediante immagini satellitari - Lancio del progetto sen4H2 " , su IFP Énergies nouvelles (consultato il 6 aprile 2019 ) .
- " Risorse minerarie di acque profonde " , su Ifremer (consultato il 28 ottobre 2019 ) .L'articolo presenta una carta dei fondali che dà la nota distribuzione a serpentina lungo le creste.
- Sylvestre Huet , “ l'idrogeno Nativo, una nuova fonte di energia? » , Su sciences.blogs.liberation.fr , Liberation ,23 aprile 2013(consultato il 28 ottobre 2019 ) .
- " Reazione del mantello dell'acqua di mare: formazione di serpentine " , su Ifremer (consultato il 28 ottobre 2019 ) .
- " Sintesi di idrogeno, metano e idrocarburi nelle profondità marine, verso nuove risorse energetiche... " , su Ifremer (consultato il 28 ottobre 2019 ) .
- " Idrogeno, sì, ma idrogeno naturale " , su La Tribune ,28 giugno 2018(consultato il 3 ottobre 2020 ) .
- Idrogeno naturale: un contributo al mix energetico? , IFP Nuove energie ,11 aprile 2013.
- Julia Guélard , Caratterizzazione delle emanazioni di idrogeno naturale in un contesto intracratonico: esempio di interazione gas/acqua/roccia in Kansas (tesi di dottorato in geochimica), Università Pierre-et-Marie-Curie e IFP Énergies nouvelles ,2016( presentazione online , leggi online ).
- (in) J. Guélard , V. Beaumont , V. Rouchon e F. Guyot , " H2 naturale in Kansas: origine superficiale dell'oro profondo? » , Geochimica, Geofisica, Geosistemi , vol. 18, n . 5,3 aprile 2017, pag. 1841–1865 ( ISSN 1525-2027 , DOI 10.1002 / 2016GC006544 , abstract , lettura online , accesso 28 ottobre 2019 ).
- Alain Prinzhofer, Eric Deville, Idrogeno naturale - La prossima rivoluzione energetica? , Ed. Belin, 2015 ( ISBN 978-27011-83848 ) .
- J. Guélard et al. , “ H 2 naturale in Kansas: origine profonda o superficiale? ", Geochimica Geofisica Geosistemi ,aprile 2017( DOI 10.1002 / 2016GC006544 , presentazione online , lettura online [PDF] , accesso 25 ottobre 2109 ).
- (in) Isabelle Moretti, Emyrose Brouilly, Keanu Loiseau, Alain Prinzhofer Eric Deville, " Hydrogen Fumes in Intracratonic Areas: New Guide Lines for Early Screening Basin Exploration " su hmdpi.com ,22 marzo 2021(consultato il 16 giugno 2021 )
- (in) Maria Rosanne Fabian Rupin Louis Gorintin Julio Aguilar, Helena-Fog, Werly Julien Olivier Lhote, Xi Yao, " SISTEMA PARHYS: UN NUOVO APPROCCIO ALLE MISURAZIONI DELLA CONCENTRAZIONE DI H2 NEL SOTTOSUPERFICIE " su hnasummit.com ,26 aprile 2021(consultato il 16 giugno 2021 )
- (in) H. Hosgormez G. Etiope e MN Yalçin , " Nuove prove per un'origine mista inorganica e organica del fuoco olimpico Chimera (Turchia): un'ampia infiltrazione di gas abiogenico " , Geofluids , vol. 8, n ° 4,25 novembre 2008, pag. 263–273 ( DOI 10.1111 / j.1468-8123.2008.00226.x ).
- " Bourakébougou: la promessa di una centrale a idrogeno " ,18 febbraio 2013(consultato il 28 ottobre 2019 ) .
- " L'idrogeno secondo Isabelle Moretti - Sciences et Avenir " , Sciences et Avenir (consultato il 2 giugno 2021 ) .
- (in) "Gas vulcanici: idrogeno che brucia al vulcano Kilauea, Hawaii" su mendeley.com.
- (it) Deep Hydrogen su astrobio.net.
- (it) GJ MacDonald (1988). "Domande principali sulle strutture continentali profonde" Perforazione profonda nella roccia cristallina, v. 1 : 28-48 p., Berlino: Springer-Verlag. .
- " L'idrogeno naturale una fonte molto più importante di quanto si pensasse secondo il CNRS " , su http://erh2-bretagne.mystrikingly.com ,11 maggio2019(consultato il 12 novembre 2019 ) .
- Isabelle Moretti, " Idrogeno naturale: curiosità geologica o grande fonte di energia nel futuro?" » , Sulla Conoscenza delle energie .
- " Il 15 aprile 1988 il Tu-155 vola ad idrogeno " , su Aerobuzz ,2 ottobre 2020(consultato il 12 novembre 2020 )
- Idrogeno, nuove tecnologie energetiche. Le chiavi CEA, n o 50/51, inverno 2004-2005, ( ISSN 0298-6248 )
- Rapporto del progetto europeo StorHy, p. 8, tasso di perdita di idrogeno
- Articolo Tribune L' Europa finanzia una batteria gigante per immagazzinare energia rinnovabile
- (in) T. Mitsui, MK Rose E. Fomin, DF Ogletree e M. Salmeron, "L' adsorbimento dissociativo dell'idrogeno è il palladio richiede aggregati di tre o più posti vacanti " , Nature , vol. 422,17 aprile 2003, pag. 705-707 ( DOI 10.1038/nature01557 , leggi online [PDF] ).
- (en) Il futuro dell'idrogeno: cogliere le opportunità di oggi [PDF] , Agenzia internazionale per l'energia , giugno 2019.
- (in) Percorsi di decarbonizzazione del gas 2020-2050 , Gas for Climate,aprile 2020, 226 pag. ( leggi online [PDF] ) , p. 17.
- " Piano di risanamento: che posto per l'energia? » , Su connancedesenergies.org ,4 settembre 2020.
- (in) " L'idrogeno prodotto dal nucleare sarà considerato 'a basse emissioni di carbonio', afferma un funzionario dell'UE " ["L'idrogeno prodotto dal nucleare sarà considerato "a bassa impronta di carbonio", secondo un funzionario dell'UE »], Su EURACTIV ,19 novembre 2020.
- " Il piano francese per l'idrogeno conferma discretamente il rilancio del nucleare " , su Reporterre ,2 febbraio 2021.
- " Idrogeno naturale: una curiosità geologica o un'importante fonte di energia in futuro?" » , Su connancedesenergies.org ,22 maggio 2020.
- “ Idrogeno verde, l'anello mancante nella transizione ” , Alternatives économique (consultato l'8 agosto 2020 ) .
- Interactions (lettera agli azionisti di Air Liquide), Air Liquide , settembre 2015 [PDF] , p. 5 .
- (in) Liz Gyekye [ https://biomarketinsights.com/australia-backs-tech-that-converts-biogas-into-hydrogen-and-graphite/ "L'Australia sostiene la tecnologia che converte il biogas in idrogeno e grafite"] Attrazioni sul biomarketing , 4 settembre 2019.
- Jérôme Marin, " Lhyfe produrrà idrogeno verde con turbine eoliche " , La Tribune ,17 gennaio 2020.
- "L'Ademe elenca i "maggiori contributi" dell'idrogeno alla transizione energetica" , Connaissance des Energies , 4 aprile 2018.
- Il vettore dell'idrogeno nella transizione energetica , Parere dell'ADEME, aprile 2018 [PDF] .
- Séverine Fontaine, " L'Ademe vuole l'idrogeno da energie rinnovabili ", L'Automobile & L'Entreprise , n o 5,febbraio 2016( leggi in linea ).
- " La Commissione Europea svela il suo piano di sviluppo dell'idrogeno verde " , su EnerGeek ,10 luglio 2020(consultato l'11 luglio 2020 ) .
- L'idrogeno nella transizione energetica , Ademe , febbraio 2016, 7 pagine [PDF] .
- Joseph Martin , " Sviluppo dell'idrogeno, ADEME fa il punto " , su RSE Magazine (consultato il 17 maggio 2019 ) .
- " I ricercatori di Grenoble ottimizzano la fotosintesi artificiale per produrre idrogeno " , su placegrenet.fr ,21 aprile 2018(consultato il 30 marzo 2019 ) .
- Véronique Pouzard, " L'elettrolisi ad alta temperatura del CEA portata dalla start-up Sylfen " , Les Échos ,26 febbraio 2019(consultato il 30 marzo 2019 ) .
- AFP (2019) Idrogeno “verde”: cooperazione tra Air Liquide, Engie e l'agglomerato Durance, Lubéron, Verdon ; 13 novembre 2019
- McPhy al centro della più grande unità di produzione di idrogeno a zero emissioni di carbonio in Europa , Les Échos , 22 gennaio 2020.
- Piano di risanamento: la Francia cambia scala nell'idrogeno , Les Échos , 3 settembre 2020.
- L'idrogeno: Francia dettagli il suo piano di 7 miliardi di euro , Les Echos , 8 Settembre 2020.
- L'idrogeno: il governo vuole creare un "Airbus per l'elettrolisi" , Les Echos , 8 Settembre 2020.
- (in) "Gli scienziati di KU Leuven decifrano il codice per un gas idrogeno economico ed ecologico " , su KU Leuven (consultato il 31 ottobre 2019 ) .
- "I ricercatori belgi stanno sviluppando un pannello solare che produce idrogeno " , su RTBF Info ,1 ° marzo 2019(consultato il 31 ottobre 2019 ) .
- " Colruyt Group: la scommessa sulla mobilità dell'idrogeno " , su RTBF Info ,8 ottobre 2018(consultato il 31 ottobre 2019 ) .
- " Colruyt e Fluxys vogliono costruire un impianto a idrogeno, il primo in Belgio " , Le Soir ,8 ottobre 2019(consultato il 31 ottobre 2019 ) .
- " Guidare a idrogeno: la nostra esperienza " , automobile Le Moniteur (consultato il 31 ottobre 2019 ) .
- (en) Monica Nagashima (Institute of Energy Economics, Japan), La strategia giapponese per l'idrogeno e le sue implicazioni economiche e geopolitiche , Institut français des relations internationales , ottobre 2018 [PDF] .
- "La "strategia dell'idrogeno" del Giappone , Conoscenza delle energie, 9 ottobre 2018.
- (in) " Centro dati sui combustibili alternativi: vacanze nella stazione di rifornimento di idrogeno " , su Centro dati sui combustibili alternativi , Dipartimento dell'energia degli Stati Uniti (consultato il 31 ottobre 2019 ) .
- Benoît Le Floc'h, “ E l'idrogeno per i veicoli commerciali leggeri? » , Su Caradisiaco ,29 novembre 2018(consultato il 30 marzo 2019 ) .
- "La California supera il traguardo delle 7.500 auto a idrogeno in circolazione " , su www.h2-mobile.fr (consultato il 31 ottobre 2019 ) .
- (in) " Il governo tedesco adotta la strategia per l'idrogeno " [ "Il governo tedesco adotta la strategia per l'idrogeno"], sul governo federale (Germania) ,10 giugno 2020.
- Accidentologia dell'idrogeno , Ministero dell'ecologia, dell'energia, dello sviluppo sostenibile e dell'assetto del territorio , 18 p. ( leggi online [PDF] ) , p. 4.
- Radisson, Laurent (2015) Rischi da idrogeno: il Ministero dell'Ecologia sta lavorando a nuovi testi; ; News env, pubblicata il 21 ottobre 2015
- T. Rahn, JM Eiler, KA Boering, PO Wennberg, MC McCarthy, S. Tyler, S. Sc Chauffage, S. Donelly, E. Atlas, L' estremo arricchimento del deuterio nell'idrogeno stratosferico e il bilancio atmosferico globale di H2 , Nature 424 , 918-921, 2003.
- TK Tromp , RL Shia , Mr. Allen , JM Eiler e YL Yung , " Potenziale impatto ambientale di un'economia dell'idrogeno sulla stratosfera " , Science , n o 300,2003, pag. 1740-1742 ( DOI 10.1126 / scienze.1085169 ).
- Céline Duguey, " Un'esperienza esplosiva " , su Espace des sciences ,settembre 2009(consultato il 16 aprile 2020 ) .
- (in) Florent Tonus Mona Bahout , Paul F. Henry e Siân E. Dutton , " Uso della diffrazione in situneutron per monitorare reazioni ad alta temperatura, solido/H2-gas " , Comunicazioni chimiche , n o 18,21 aprile 2009, pag. 2556–2558 ( ISSN 1364-548X , PMID 19532888 , DOI 10.1039/B822419F , lettura online , accesso 16 aprile 2020 ).
Vedi anche
Bibliografia
- Yver, Camille, Quantificare l'uso dell'idrogeno da parte dei suoli: dalla scala locale a quella globale , 2011 DOI: 10.4267 / 2042/47372 ( sommario - Prix Prud'homme 2011.
- Stephen Boucher, La rivoluzione dell'idrogeno. Verso un'energia pulita ed efficiente? , prefazione di Thierry Alleau, Paris, Ed. du Felin, 2006, 160 p. , ( ISBN 2-86645-616-5 ) .
- Alain Prinzhofer, Eric Deville, Idrogeno naturale - La prossima rivoluzione energetica? , Belin, 2015 ( ISBN 978-27011-83848 )
Articoli Correlati
link esterno
- Associazione francese dell'idrogeno
- Rete europea / Polo di competenza
- Sviluppo H2
- CEA Technologies, Idrogeno, nuove tecnologie energetiche , Clefs CEA n o 50-51), 23 marzo 2005
- L'idrogeno visto dal CEA
- INERIS: feedback sull'esperienza legato alle difficoltà di stoccaggio
- L'idrogeno visto dalla Società Chimica Francese
- La polemica sull'uso dell'idrogeno come combustibile
- Tutto sull'alternativa all'idrogeno, con rassegna stampa, link internet e video








