Argon
| Argon | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Argon solido e liquido. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Posizione nella tavola periodica | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Simbolo | Ar | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nome | Argon | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Numero atomico | 18 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gruppo | 18 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Periodo | 3 e periodo | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bloccare | Blocco p | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Famiglia di elementi | gas nobile | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Configurazione elettronica | [ Ne ] 3 s 2 3 p 6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elettroni per livello di energia | 2, 8, 8 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietà atomiche dell'elemento | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Massa atomica | 39,948 ± 0,001 u | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Raggio atomico (calc) | ( ore 71 ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| raggio covalente | 106 ± 22:00 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Raggio di Van der Waals | 188 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Stato di ossidazione | 0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ossido | sconosciuto | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energie di ionizzazione | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 re : 15.759610 eV | 2 e : 27.62966 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3 e : 40,74 eV | 4 e : 59,81 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 5 e : 75.02 eV | 6 ° : 91.009 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 7 e : 124.323 eV | 8 e : 143.460 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 9 e : 422,45 eV | 10 e : 478,69 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 11 e : 538,96 eV | 12 e : 618,26 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 13 e : 686.10 eV | 14 e : 755,74 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 15 e : 854,77 eV | 16 ° : 918,03 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 17 e : 4 120.8857 eV | 18 e : 4 426.2296 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isotopi più stabili | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietà fisiche semplici del corpo | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Stato ordinario | Gas (non magnetico) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
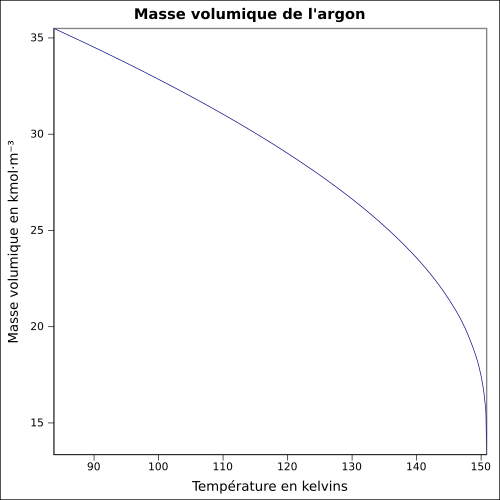
| Massa volumica |
1,7837 g · L -1 ( 0 °C , 1 atm ) equazione:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sistema di cristallo | Cubo a facce centrate | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Colore | incolore | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto di fusione | −189,36 °C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto di ebollizione | -185,85 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energia di fusione | 1.188 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energia di vaporizzazione | 6,43 kJ · mol -1 ( 1 atm , -185,85 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Temperatura critica | −122,3 °C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto triplo | −189,3442 °C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volume molare | 22,414 × 10 -3 m 3 · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pressione del vapore |
equazione:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Velocità del suono | 319 m · s da -1 a 20 °C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Calore massiccio |
520 J · kg -1 · K -1
equazione:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conduttività termica | 0,01772 W · m -1 · K -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Varie | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100.028.315 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o EC | 231-147-0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Precauzioni | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Avvertimento H280 e P403 H280 : Contiene gas sotto pressione; può esplodere se riscaldato P403 : Conservare in luogo ben ventilato. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 A, A : Temperatura critica del gas compresso = −122,4 ° C Divulgazione all'1,0% secondo i criteri di classificazione |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Trasporto | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
20 : gas asfissiante o gas che non presenta un rischio sussidiario Numero ONU : 1006 : ARGON COMPRESSO Classe: 2.2 Codice di classificazione: 1A : Gas compresso, aspssiante; Etichetta: 2.2 : Gas non infiammabili, non tossici (corrisponde ai gruppi indicati con A o O maiuscola); 
22 : gas liquefatto refrigerato, asfissiante Numero ONU : 1951 : ARGON LIQUIDO REFRIGERATO Classe: 2.2 Codice di classificazione: 3A : Gas liquefatto refrigerato, asfissiante; Etichetta: 2.2 : Gas non infiammabili, non tossici (corrisponde ai gruppi indicati con A o O maiuscola);  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Unità di SI e STP se non diversamente indicato. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
L' Argon è l' elemento chimico di numero atomico 18 e simbolo Ar. Appartiene al gruppo 18 della tavola periodica e fa parte della famiglia dei gas nobili , detti anche "gas nobili", che comprende anche l' elio , il neon , cripto , xeno e radon . L'argon è il 3 ° costituente più abbondante dell'atmosfera terrestre , con una frazione di massa dell'1,288%, corrispondente ad una frazione di volume dello 0,934% (o 9340 ppm ), ed è il gas nobile più abbondante al mondo.' La crosta terrestre , contabilizzando 1,5 ppm . Argon nell'atmosfera terrestre è quasi interamente costituito di argon 40 , un nuclide radiogeno risultante dal decadimento di potassio 40 , mentre l'argon osservato nel universo è principalmente costituito di argon 36 , prodotto da nucleosintesi stellare nel supernovae .
Il nome argon deriva dal greco antico ἀργόν, che significa "ozioso", "pigro" [derivato dalla parola greca ἀεργός, formata da ἀ-εργός, che significa "senza lavoro", "ozioso"], con riferimento al fatto che questo elemento è chimicamente inerte. La sua configurazione elettronica presenta uno strato di valenza saturo all'origine della sua stabilità e della virtuale impossibilità di stabilire legami covalenti . La temperatura di 83,805 8 K del suo punto triplo è uno dei punti di riferimento dell'International Temperature Scale del 1990 (ITS-90).
Argon viene prodotto industrialmente per distillazione frazionata di aria liquefatto . Viene utilizzato principalmente come atmosfera inerte per la saldatura e vari processi industriali ad alta temperatura che coinvolgono sostanze reattive. Un'atmosfera di argon viene quindi utilizzata nei forni elettrici ad arco di grafite per impedire la combustione di quest'ultimo. Impiega l'argon anche nell'illuminazione con lampade ad incandescenza , tubi fluorescenti e tubi a gas . Viene utilizzato per produrre laser a gas blu-verde.
Proprietà principali
L'argon è incolore, inodore, non infiammabile e non tossico allo stato gassoso, liquido o solido. La sua solubilità in acqua è approssimativamente paragonabile a quella dell'ossigeno ed è 2,5 volte quella dell'azoto . È chimicamente inerte in quasi tutte le condizioni e non forma sostanze chimiche confermate a temperatura ambiente .
L'argon, tuttavia, è in grado di formare composti chimici in determinate condizioni estreme di squilibrio. L' argon fluoroidrato ḥarf è stato così ottenuto per fotolisi ultravioletta di acido fluoridrico HF in una matrice criogenica di ioduro di cesio CsI e argon di Ar; stabile al di sotto di 27 K ( -246,15 °C ), è stato identificato mediante spettroscopia infrarossa . Il fluoroidruro di argon è l'unico composto noto dell'argon che è neutro e stabile allo stato fondamentale .
L'argon può anche formare clatrati in acqua quando i suoi atomi sono intrappolati nel reticolo tridimensionale formato dal ghiaccio . Esistono anche ioni poliatomici contenenti argon, come il catione argon idruro ArH + , ed ecciplessi , come Ar 2* e ArF *. Vari composti con legami Ar C e Ar If stabili sono stati previsti mediante simulazione numerica ma non sono stati sintetizzati in laboratorio.
I principali isotopi dell'argon presenti nella crosta terrestre sono l' argon 40 ( 40 Ar) per il 99,6%, l' argon 36 ( 36 Ar) per lo 0,34% e l' argon 38 ( 38 Ar) per lo 0,06%. Il potassio-40 ( 40 K) si disintegra spontaneamente in misura dell'11,2% in argon 40 per tomografia a cattura o emissione di elettroni e in quantità dell'88,8% in calcio 40 ( 40 Ca) per disintegrazione - con un tempo di dimezzamento (metà -vita) di 1,25 miliardi di anni. Questa durata e il rapporto tra i sottoprodotti formati consentono di determinare l'età delle rocce con il metodo della datazione potassio-argon .
Nel atmosfera terrestre , l'argon 39 è prodotto principalmente dall'interazione di radiazione cosmica sul argon 40 per cattura di neutroni , seguito da una doppia emissione di neutroni . Nel sottosuolo, può anche essere prodotto dal potassio 39 mediante cattura di neutroni seguita da emissione di protoni .
L' argon 37 viene prodotto durante le prove sotterranee dal calcio 40 mediante cattura di neutroni seguita da disintegrazione α ; ha un'emivita di 35 giorni.
L'argon è notevole in quanto la sua composizione isotopica varia significativamente da una regione all'altra del Sistema Solare . L'argon, la cui fonte principale è il decadimento radioattivo del potassio 40 nelle rocce, è costituito principalmente da argon 40 , come sui pianeti terrestri che trattengono un'atmosfera: Venere , Terra e Marte . D'altra parte, l'argon formato direttamente dalla nucleosintesi stellare è essenzialmente costituito dall'argon 36 prodotto dalla reazione alfa , come nel caso del Sole , il cui argon è l'84,6% dell'argon 36 secondo le misurazioni del vento solare . È lo stesso nei pianeti giganti , dove l'abbondanza relativa di isotopi 36 Ar: 38 Ar: 40 Ar è 8400: 1600: 1.
Oltre all'atmosfera terrestre , che ha una frazione volumetrica di 0,934% di argon, o 9,340 ppm , l' atmosfera di Mercurio contiene 0,07 ppm , quella di Venere contiene 70 ppm e quella di Marte contiene 19,300 ppm , o 1,93%.
La predominanza dell'argon radiogeno 40 nell'atmosfera terrestre è responsabile del fatto che la massa atomica dell'argon terrestre, dell'ordine di 39,95 u , è di 0,85 u maggiore di quella del potassio , che la segue nella tavola periodica degli elementi e la cui massa atomica è dell'ordine di 39,10 u . Ciò sembrò paradossale durante la scoperta dell'argon nel 1894 perché Dmitri Mendeleïev aveva disposto la sua tavola periodica in ordine di massa atomica crescente, il che portò a dover interporre l' argon tra potassio e calcio , con una massa atomica di circa 40,08 u e confuso con quella dell'argon entro 0,13 u , mentre c'era una differenza di massa atomica di 3,65 u tra cloro (35,45 u ) e potassio (39,10 u ). Questo problema fu risolto da Henry Moseley , che dimostrò nel 1913 che la tavola periodica doveva essere organizzata in ordine di numero atomico crescente, e non per massa atomica crescente, che metteva gli elementi nell'ordine corretto.
Il atmosferico abbondanza argon relativa rispetto ad altri gas nobili - 9340 ppm di argon, contro 5,24 ppm di elio , 18.18 ppm di neon , 1,14 ppm di krypton e 0,087 ppm di xenon - può anche essere attribuita a radiogeno argon 40 : argon 36 ha infatti un'abbondanza di soli 31,5 ppm (0,337% di 9340 ppm ), dello stesso ordine di grandezza di quella del neon (18,18 ppm ).
Composti
L' argon atomo ha un elettrone saturo valenza shell , con completa s e p sottolivelli . Questo rende questo elemento chimicamente inerte e molto stabile, vale a dire che forma un legame chimico con altri atomi solo con grande difficoltà. Fino 1962 , i gas nobili sono stati considerati totalmente inerte e non adatti per la formazione di composti chimici ; a questa data, tuttavia, la sintesi dello xeno esafluoroplatinato XePtF 6 spianò la strada alla chimica dei gas nobili .
Il primo composto di argon con tungsteno pentacarbonile, della formula chimica W (CO) 5 Ar, è stato pubblicato nel 1975, ma la sua effettiva esistenza rimane controversa. Nell'agosto del 1962 fu sintetizzato presso l' Università di Helsinki l' argon fluoroidruro Harf mediante fotolisi ultravioletta di acido fluoridrico HF in una matrice criogenica di cesio ioduro CsI e Argon composto stabile al di sotto di 27 K ( -246,15 °C ) identificato mediante spettroscopia infrarossa . Questa scoperta ha portato all'idea che l'argon potrebbe formare composti debolmente legati.
Il dicatione metastabile ARCf 22+ , isoelettronico con fluoruro di carbonile COF 2e fosgene COCl 2dal punto di vista degli elettroni di valenza , è stata osservata nel 2009 l'attuazione di un legame carbonio- argon. Lo ione molecolare 36 ArH + , corrispondente al catione argon idruro 36 (argonium), è stato rilevato nel mezzo interstellare a livello della Nebulosa del Granchio ; è il primo composto di gas nobile rilevato nello spazio .
L'idruro di argon solido Ar (H 2 ) 2è un composto di van der Waals avente la stessa struttura cristallina della fase di Laves (en) MgZn 2. Si forma a pressioni comprese tra 4,3 e 220 GPa , sebbene i risultati ottenuti dalla spettroscopia Raman suggeriscano che le molecole di H 2del composto Ar (H 2 ) 2dissociarsi sopra 175 GPa .
Produzione industriale e applicazioni
Argon viene prodotto industrialmente per distillazione frazionata di aria liquefatto in unità criogeniche di distillazione dell'aria (a) , metodo per separare l' azoto liquido , che bolle a 77,3 K , argon, che bolle a 87,3 K , e l' ossigeno liquido , che bolle a 90.2 K . La produzione mondiale di argon è dell'ordine di 700.000 tonnellate all'anno.
L'argon ha diverse proprietà interessanti che ne giustificano l'uso industriale:
- è un gas chimicamente inerte;
- è un'alternativa economica quando l' azoto non è sufficientemente inerte;
- ha una bassa conducibilità termica (è quindi un isolante termico );
- le sue proprietà elettroniche ( ionizzazione , spettro di emissione ) sono utilizzate in alcune applicazioni di illuminazione.
Altri gas nobili presentano proprietà simili e possono essere utilizzati anche, ma argon è di gran lunga il più economico di tutti, essendo ottenuto come sottoprodotto dell'estrazione di ossigeno e l'azoto dalla dell'aria mediante distillazione frazionata criogenica.
Applicazioni industriali
L'argon è utilizzato in alcuni processi industriali ad alta temperatura in cui le sostanze chimicamente inerti tendono a diventare reattive. Atmosfera di argon viene quindi utilizzata in forni elettrici con grafite elettrodi in modo da evitare la combustione di questo materiale.
Per alcuni di questi processi, la presenza di azoto o ossigeno causerebbe difetti nel materiale. L'argon viene utilizzato in alcuni tipi di saldatura ad arco come la saldatura ad arco con gas e metallo e la saldatura TIG , nonché nel trattamento del titanio e di altri elementi reagenti. Anche i cristalli di silicio e germanio destinati all'industria dei semiconduttori vengono coltivati in atmosfera di argon per garantirne la qualità cristallina.
L'argon è utilizzato nell'industria avicola come metodo di asfissia con gas inerte per asfissiare il pollame , sia per una macellazione di massa dopo l'insorgenza di una malattia, sia come mezzo di macellazione alternata all'elettronarcosi . La densità relativa dell'argon rispetto all'aria fa sì che rimanga vicino al suolo durante la gasazione. La sua natura non reattiva lo rende compatibile con i prodotti alimentari e il fatto che sostituisca parzialmente l'ossigeno nei tessuti prolunga la durata di conservazione degli alimenti.
L'argon viene talvolta utilizzato per estinguere gli incendi preservando apparecchiature di valore, come i server dei computer , che verrebbero danneggiati dall'uso di acqua o schiuma.
Applicazioni mediche
Le procedure di criochirurgia (in) come la crioablazione (in) utilizzano argon liquido per distruggere tessuti come le cellule tumorali . È stato possibile utilizzarlo in una procedura chiamata coagulazione potenziata da argon , che è una forma di elettrochirurgia (in) mediante torcia al plasma , ma che presenta un rischio di embolia gassosa materializzata dalla morte di almeno un paziente.
I laser blu argon sono utilizzati in chirurgia per suturare le arterie , distruggere i tumori nella chirurgia oculare o per l' elettrocoagulazione attraverso lesioni ufficiali endoscopiche emorragie gastrointestinali.
L'argon è stato anche testato per sostituire l' azoto nel gas respiratorio chiamato Argox al fine di accelerare la rimozione dell'azoto disciolto dal sangue .
Ricerca scientifica
L'argon liquido viene utilizzato come bersaglio per il rilevamento dei neutrini e la ricerca sulla materia oscura . Le interazioni tra ipotetiche WIMP ei nuclei degli atomi di argon dovrebbero produrre una scintillazione osservabile attraverso tubi fotomoltiplicatori . Rivelatori a due fasi contenenti gas argon vengono utilizzati per rilevare gli elettroni prodotti dalla ionizzazione durante le interazioni WIMP-nucleo di argon.
Come altri gas nobili liquefatti, l'argon liquido ha un alto tasso di scintillazione (circa 51 fotoni/keV ), è trasparente alla propria scintillazione ed è relativamente facile da purificare. È meno costoso dello xeno e ha un diverso profilo temporale di scintillazione, che consente di distinguere le interazioni elettroniche dalle interazioni nucleari. Ha comunque un forte radioattività β causa della contaminazione da l' argon 39 , ad eccezione di argon dal seminterrato Terra impoverito in 39 Ar cui emivita è solo 269 anni e la cui azione non è ricostituita dal 40 Ar ( n , 2 n ) 39 ar interazione dei raggi cosmici sul atmosferica argon .
In un altro registro, l' argon 39 è stato utilizzato in particolare per datare le acque sotterranee e le carote di ghiaccio in Antartide . La datazione K-Ar e la datazione argon-argon sono utilizzate anche per la datazione radiometrica di sedimenti , metamorfici e ignei .
conservatore
L'argon, numero E938 , viene utilizzato come conservante alimentare per rimuovere l' ossigeno e l' umidità dall'atmosfera negli imballaggi e per ritardarne la data di scadenza. L' ossidazione da parte dell'aria, l' idrolisi e altre reazioni che degradano il prodotto vengono così ritardate o completamente bloccate. I reagenti chimici e le molecole farmaceutiche sono talvolta confezionati in un'atmosfera di argon. Questo gas nobile viene utilizzato anche come conservante per vernici , poliuretano o anche pitture .
L'argon viene anche utilizzato nella vinificazione per proteggere il vino dall'ossigeno e prevenirne l'ossidazione e le interazioni batteriche indesiderate (soprattutto i batteri acetici , che producono acido acetico e trasformano il vino in aceto ). Può essere utilizzato anche come propellente per spray .
Attrezzature da laboratorio
L'argon può essere utilizzato come gas inerte per una linea del vuoto e un vano portaoggetti ; è preferito all'azoto , che è meno costoso, perché l'azoto è in grado di reagire con composti particolarmente reattivi, oltre che con determinate apparecchiature. Inoltre, l'argon ha il vantaggio di essere più denso dell'aria, a differenza dell'azoto, il che lo rende più facile da usare nella pratica.
L'argon può essere utilizzato come gas di trasporto nella gascromatografia e nella ionizzazione elettrospray . È il gas di scelta per il plasma utilizzato nella spettrometria al plasma accoppiato induttivamente . L'argon è preferibilmente utilizzato nella deposizione per polverizzazione (In) sui campioni da esaminare mediante microscopia elettronica a scansione e per la pulizia dei wafer nella microfabbricazione .
Illuminazione
Una lampada ad incandescenza viene solitamente riempito con argon per preservare il suo filamento da alta temperatura di ossidazione . L'argon è utilizzato anche per la sua radiazione per ionizzazione , come nelle lampade al plasma e nei calorimetri nella fisica delle particelle . Le lampade a scarica riempite di argon puro producono una luce viola pallido tirando lebleu lavanda, che diventa blu aggiungendo un po' di mercurio .
L'argon viene utilizzato anche per i laser a ioni (in) blu e verde.
Varie applicazioni
L'argon viene utilizzato come isolante termico per i doppi vetri . Viene anche utilizzato per riempire mute stagne per immersioni subacquee grazie alla sua inerzia chimica e alla bassa conducibilità termica .
L'argon è uno dei gas che possono essere utilizzati in astronautica come propellente per i VASIMR . Nel campo delle armi ad aria compressa , viene utilizzato sotto pressione per raffreddare, rilassando, le teste di alcuni missili aria-aria , inclusi i missili AIM-9 Sidewinder .
L'argon è stato utilizzato nell'atletica come drogante che simula l' ipossia . È stato quindi inserito, insieme allo xeno , nell'elenco dei metodi e delle sostanze vietate dall'Agenzia mondiale antidoping nel 2014 prima di essere ritirato nel 2020.
Storia ed etimologia
La parola argon deriva dal greco antico ἀργός / argós ("ozioso", "pigro", "sterile"), formato dal prefisso greco privato ἀ e dalla parola ἔργον / ergon ("lavoro"), questa etimologia evocando il carattere inerte dell' elemento.
La presenza nell'aria di un gas chimicamente inerte era sospettato da Henry Cavendish come già nel 1785 , ma la sua scoperta da Lord Rayleigh e Sir William Ramsay alla University College di Londra aspettato fino a 1894 . Lo hanno fatto rimuovendo ossigeno , anidride carbonica , vapore acqueo e azoto da un campione di aria pulita , lasciando un gas inerte chiamato argon . Questi due scienziati hanno fatto la comunicazione ufficiale della loro scoperta alla Royal Society il31 gennaio 1895.
Sono stati messi in pista dal fatto che l'azoto prodotto chimicamente era dello 0,5% più leggero di quello estratto dall'aria rimuovendo altri gas atmosferici conosciuti all'epoca. La distillazione frazionata dell'aria liquefatta ha permesso loro di produrre una notevole quantità di argon nel 1898 e contemporaneamente di isolare altri due gas nobili il neon e lo xeno .
L'argon è stato osservato anche nel 1882 durante un lavoro indipendente di HF Newall e WN Hartley, che hanno notato righe spettrali nello spettro di emissione dell'aria non corrispondenti a nessun elemento chimico noto.
Il simbolo chimico dell'argon era A fino al 1957, quando divenne Ar.
Pericoli
Come l' elio , l'argon non è pericoloso a basse concentrazioni. Tuttavia, è 38% più denso rispetto all'aria , e inalare una grande quantità di argon comporta il rischio di asfissia da deprivazione di ossigeno ( anossia ); ciò può verificarsi, ad esempio, durante le operazioni di saldatura in uno spazio ristretto.
Note e riferimenti
- (in) Beatriz Cordero Verónica Gómez, Ana E. Platero-Prats, Marc Revés Jorge Echeverría, Eduard Cremades, Flavia e Santiago Barragan Alvarez , " Radi covalenti rivisitati " , Dalton Transactions ,2008, pag. 2832 - 2838 ( DOI 10.1039/b801115j )
- (in) David R. Lide, CRC Handbook of Chemistry and Physics , TF-CRC,2006, 87 ° ed. ( ISBN 0849304873 ) , pag. 10-202
- (en) David R. Lide, CRC Handbook of Chemistry and Physics , CRC Press Inc,2009, 90 ° ed. , 2804 pag. , Copertina rigida ( ISBN 978-1-420-09084-0 )
- (en) Robert H. Perry e Donald W. Green , Perry's Chemical Engineers' Handbook , USA, McGraw-Hill,1997, 7 ° ed. , 2400 pag. ( ISBN 0-07-049841-5 ) , pag. 2-50
- Verbale del Comitato internazionale dei pesi e delle misure , 78 ° Sessione, 1989, pp. T1-T21 (e pp. T23-T42, versione inglese).
- Database Chemical Abstracts interrogato tramite SciFinder Web 15 dicembre 2009 ( risultati della ricerca )
- inserimento del numero CAS "7440-37-1" nel database chimica GESTIS dell'IFA (ente tedesco responsabile per la sicurezza sul lavoro e la salute) ( tedesco , inglese ), si accede il 30 gennaio 2009 (È necessario JavaScript)
- " Argon " nel database dei prodotti chimici Reptox del CSST (organizzazione del Quebec responsabile per la sicurezza e la salute sul lavoro), accesso 25 aprile 2009
- (in) Markku Räsänen , " Argon dal nulla " , Nature Chemistry , vol. 6, n ° 1, gennaio 2014, Articolo n o 82 ( PMID 24345939 , DOI 10.1038/nchem.1825 , leggi online )
- (en) Leonid Khriachtchev, Mika Pettersson, Nino Runeberg, Jan Lundell e Markku Räsänen , “ A stable argon compound ” , Nature , vol. 406, n ° 6798, 24 agosto 2000, pag. 874-876 ( PMID 10972285 , DOI 10.1038 / 35022551 , Bibcode 2000Natur.406..874K , leggi online )
- (in) VR Belosludov OS Subbotin DS Krupskii, Prokuda OV, RV e Y. Belosludov Kawazoe , " Modello microscopico di composti clatrati " , Journal of Physics: Conference Series , vol. 29, n ° 1, gennaio 2006, pag. 1-7 ( DOI 10.1088 / 1742-6596 / 29/1/001 , Bibcode 2006JPhCS..29 .... 1B , leggi online )
- (in) Arik Cohen, Jan Lundell e R. Benny Gerber , " Primi composti con legami chimici argon-argon e carbonio-silicio " , Journal of Chemical Physics , vol. 119, n . 13, ottobre 2003, pag. 6415-6417 ( DOI 10.1063/ 1.1613631 , Bibcode 2003JChPh.119.6415C , leggi online )
- (en) J. Emsley, Nature's Building Blocks , Oxford University Press, 2001, p. 44-45 . ( ISBN 978-0-19-960563-7 )
- Étienne Roth ( dir. ), Bernard Poty ( dir. ), Robert Delmas et al. ( pref. Jean Coulomb ), Metodi di datazione per fenomeni nucleari naturali , Parigi, Éditions Masson , coll. "Collezione CEA ",1985, 631 pag. ( ISBN 978-2-225-80674-2 , avviso BnF n o FRBNF34836710 ) , cap. 17 ("Silicio 32 e argon 39")
- (in) Il caso scientifico del 37 Ar come monitor per le esplosioni nucleari sotterranee , pagina 1, 2010
- (in) Katharina Lodders , " The Solar Abundance Argon " , The Astrophysical Journal , vol. 674, n . 1, 10 febbraio 2008, pag. 607-611 ( DOI 10.1086 / 524725 , Bibcode 2008ApJ ... 674..607L , arXiv arXiv: 0710.4523 , leggi online )
- (in) AGW Cameron , " Abbondanza elementale e isotopica degli elementi volatili nei pianeti esterni " , Space Science Reviews , vol. 14, n osso 3-4, marzo 1973, pag. 392-400 ( DOI 10.1007 / BF00214750 , Bibcode 1973SSRv ... 14..392C , leggi online )
- (in) Marco Fontani , Mariagrazia Costa e Mary Virginia Orna , The Lost Elements: The Periodic Table's Shadow Side , New York, Oxford University Press ,2015( 1 ° ed. 2014), 531 p. ( ISBN 9780199383344 ) , p. 182.
- (in) Neil Bartlett , " Xenon esafluoroplatinato Xe + [PtF 6 ] - " , Atti della Società Chimica , n o 6,giugno 1962, pag. 197-236 ( DOI 10.1039/PS9620000197 , leggi in linea )
- (in) Nigel A. Young , " Chimica di coordinazione del gruppo principale a bassa temperatura: una revisione dei complessi isolati dalla matrice dal Gruppo 12 al Gruppo 18 " , Coordination Chemistry Reviews , vol. 257 n ossa 5-6, marzo 2013, pag. 956-1010 ( DOI 10.1016/j.ccr.2012.10.013 , leggi online )
- (in) Neil Bartlett , " I gas nobili " , Notizie chimiche e ingegneristiche , vol. 81, n . 36, 8 settembre 2003, pag. 32-34 ( DOI 10.1021/cen-v081n036.p032 , leggi in linea )
- (in) Jessica F. Lockyear Kevin Douglas, Stephen D. Price, Małgorzata Karwowska, Karol J. Fijalkowski Wojciech Grochala Marek Remeš Jana Roithová e Detlef Schroeder , " Generazione dell'ARCf 2 2+ Dication ”, The Journal of Physical Chemistry Letters ,vol. 1,n ° 1,8 dicembre 2009, pag. 358-362 ( DOI 10.1021/jz900274p , leggi in linea )
- (it) J. Barlow, BM Swinyard, PJ Owen, J. Cernicharo, HL Gomez, RJ Ivison, O. Krause, TL Lim, M. Matsuura, S. Miller, G. Olofsson e AND Polehampton , " Detection of a Noble Gas Molecular Ion, 36 ArH + , nella Nebulosa del Granchio ” , Science , vol. 342, n . 6164, 13 dicembre 2013, pag. 1343-1345 ( PMID 24337290 , DOI 10.1126 / science.1243582 , Bibcode 2013Sci ... 342.1343B , leggi online )
- (in) Annette K. Kleppe, Mónica Amboage e Andrew P. Jephcoat , " Nuovo composto van der Waals ad alta pressione Kr (H 2) 4 scoperto nel sistema binario krypton-idrogeno ” , Scientific Reports , vol. 4,16 maggio 2014, articolo n o 4989 ( DOI 10.1038/srep04989 , Bibcode 2014NatSR ... 4E4989K , leggi online )
- " Tavola periodica degli elementi: Argon-Ar " , Environmentalchemistry.com (consultato il 12 settembre 2008 )
- (in) Sara J. Shields e ABM Raj , " A Critical Review of Electrical Water-Bath Stun Systems for Poultry Slaughter and Recent Developments in Alternative Technologies " , Journal of Applied Animal Welfare Science , vol. 13, n . 4, 2012, pag. 281-299 ( PMID 20865613 , DOI 10.1080 / 10888705.2010.507119 , leggi online )
- DL Fletcher , " Slaughter Tecnologia, " Simposio: Recent Advances in Volatili da cortile Macellazione Tecnologia ,1999( Leggi on-line , accessibile 1 ° gennaio 2010 )
- (in) MJ Fraqueza e AS Barreto , " L'effetto è la durata di conservazione della carne di tacchino del confezionamento in atmosfera modificata con una miscela di argon " , Poultry Science , vol. 88, n . 9, settembre 1999, pag. 1991-1998 ( PMID 19687286 , DOI 10.3382 / ps.2008-00239 , leggi online )
- (in) Joseph Z. Su, Andrew K. Kim, George P. Crampton e Zhigang Liu , " Soppressione del fuoco con agenti di gas inerte " , Journal of Fire Protection Engineering , vol. 11, n ° 2 2001, pag. 72-87 ( DOI 10.1106 / X21V-YQKU-PMKP-XGTP , leggi online )
- (in) " Embolia gassosa fatale causata da sovrapressurizzazione durante l'uso laparoscopico della coagulazione potenziata con argon " , Health Devices , vol. 23, n . 6, giugno 1994, pag. 257-259 ( leggi in linea )
- (in) Jerome Canady , Kimberly Wiley e Biagio Ravo , "La coagulazione del plasma di argon e le future applicazioni delle sonde endoscopiche Dual-Mode " , Reviews in Gastroenterological Disorders , vol. 6, n ° 1,2006, pag. 1-12 ( ISSN 1533-001X , PMID 16520707 , lettura online , accesso 9 ottobre 2017 ).
- (in) Andrew A Pilmanis Ulf I. Balldin, James T. Webb e Kevin M. Krause , " Decompressione in scena a 3,5 Psi utilizzando argon-ossigeno e miscele di ossigeno respirabili al 100% " , aviazione, spazio e medicina ambientale , volo. 74, n . 12, dicembre 2003, pag. 1243-1250 ( PMID 14692466 , leggi online )
- (in) Dan Gastler Ed Kearns, Andrew Hime, Laura C. Stonehill Stan Seibert, Josh Klein, Hugh W. Lippincott, Daniel N. McKinsey e James A. Nikkel , " Misurazione dell'efficienza di scintillazione per rinculo nucleari in argon liquido " , Revisione fisica C , vol. 85, n . 6, 27 giugno 2012, articolo n o 065811 ( DOI 10.1103/PhysRevC.85.065811 , Bibcode 2012PhRvC..85f5811G , arXiv 1004.0373 , leggi online )
- (in) J.Xu F. Calaprice, C. Galbiati, A. Goretti Guray G., T. Hohman, D. Holtz, An. Ianni, Mr. Laubenstein, Loer B., C. Lovec, CJ Martov, D Montanari, S. Mukhopadhyay, A. Nelson, SD Rountree, RB Vogelaar e A. Wright , " A study of the trace 39 Ar content in argon from deep underground sources " , Astroparticle Physics , vol. 66, giugno 2015, pag. 53-60 ( DOI 10.1016 / j.astropartphys.2015.01.002 , Bibcode 2015APh .... 66 ... 53X , arXiv 1204.6011 , leggi online )
- Paul Depovere, La tavola periodica degli elementi. La meraviglia fondamentale dell'Universo , De Boeck Supérieur ,2002, pag. 98.
- (it) Henry Cavendish , " XXIII. Esperimenti in onda. ” , Transazioni filosofiche della Royal Society di Londra , vol. 75, 1785, pag. 372-384 ( DOI 10.1098 / rstl.1785.0023 , Bibcode 1785RSPT ... 75..372C , leggi online )
- (in) Robert John Strutt e William Ramsay , " I. Argon, una nuova forma dell'atmosfera " , Atti della Royal Society di Londra , vol. 57, 1895, pag. 265-287 ( DOI 10.1098/rspl.1894.0149 , JSTOR 115394 , leggi online )
- (in) John William Strutt e William Ramsay , " VI. Argon, un nuovo costituente dell'atmosfera ” , Philosophical Transactions of the Royal Society of London , 1895, pag. 187-241 ( DOI 10.1098 / rsta.1895.0006 , JSTOR 90645 , Bibcode 1895RSPTA.186..187R , leggi online )
- (in) Sir William Ramsay, " The Rare Gases of the Atmosphere " , su https://www.nobelprize.org/ , Premio Nobel per la Chimica , 12 dicembre 1904(consultato il 14 giugno 2020 ) .
- (in) John H. Holloway, chimica dei gas nobili , Methuen,1968, pag. 6
- (in) John Emsley, Nature's Building Blocks: An AZ Guide to the Elements , Oxford University Press, 2003, p. 36 . ( ISBN 0198503407 )
- (in) Norman E. Holden, " Storia dell'origine degli elementi chimici e dei loro scopritori " , 41a Assemblea generale IUPAC a Brisbane, Australia, 29 giugno - 8 luglio 2001 , all'indirizzo https: //www.nndc.bnl. gov / , Centro dati nucleare nazionale , 12 marzo 2004(consultato il 14 giugno 2020 ) .
Vedi anche
Articoli Correlati
link esterno
- (it) " Dati tecnici per Argon " (consultato il 24 aprile 2016 ) , con i dati noti per ciascun isotopo nelle sottopagine
- (In) Immagini di argon in diverse forme
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | h | Hey | |||||||||||||||||||||||||||||||
| 2 | Li | Essere | B | VS | NON | oh | F | Nato | |||||||||||||||||||||||||
| 3 | N / A | Mg | Al | sì | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | Quella | Ns | Ti | V | Cr | mn | Fe | Co | o | Cu | Zn | Ga | Ge | Asso | Vedi | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | sì | Zr | Nb | Mo | Tc | Ru | RH | Pd | Ag | cd | Nel | Sn | Sb | Voi | io | Xe | |||||||||||||||
| 6 | Cs | Ba | Il | Questo | prima | Ns | Pm | Sm | Avevo | Gd | Tb | Dy | come | Er | Tm | Yb | Leggi | HF | Il tuo | W | D | Osso | Ir | Pt | In | Hg | Tl | Pb | Bi | po | In | Rn | |
| 7 | FR | RA | Corrente alternata | ns | papà | tu | Np | Poteva | Sono | Cm | Bk | Cf | è | Fm | Md | No | Lr | Rf | Db | Sg | bh | Hs | Mt | Ds | Rg | Cn | Nh | fl | Mc | Lv | Ts | Og | |
| 8 | 119 | 120 | * | ||||||||||||||||||||||||||||||
| * | 121 | 122 | 123 | 124 | 125 | 126 | 127 | 128 | 129 | 130 | 131 | 132 | 133 | 134 | 135 | 136 | 137 | 138 | 139 | 140 | 141 | 142 | |||||||||||
|
Metalli Alcalini |
Terra alcalina |
lantanidi |
Metalli di transizione |
Metalli poveri |
Metal- loids |
Non metalli |
geni dell'alone |
Gas nobili |
Articoli non classificati |
| attinidi | |||||||||
| Superattinidi | |||||||||