Adenosina trifosfato
| Adenosina trifosfato | |
 Struttura dell'adenosina trifosfato ATP 4- , specie dominante in soluzione acquosa   |
|
| Identificazione | |
|---|---|
| nome IUPAC | adenosina-5 '- (tetraidrogeno trifosfato) |
| Sinonimi |
Adenosina-5'-trifosfato |
| N o CAS | |
| N o ECHA | 100.000.258 |
| N o EC | 200-283-2 |
| DrugBank | DB00171 |
| PubChem | 5957 |
| CheBI | 15422 |
| SORRISI |
Nc1ncnc2n (cnc12) [C @@ H] 1O [C @ H] (COP (O) (= O) OP (O) (= O) OP (O) (O) = O) [C @@ H] ( O) [C @ H] 1O , |
| InChi |
Standard InChI: InChI = 1S / C10H16N5O13P3 / c11-8-5-9 (13-2-12-8) 15 (3-14-5) 10-7 (17) 6 (16) 4 (26-10) 1-25-30 (21.22) 28-31 (23,24) 27-29 (18,19) 20 / h2-4,6-7,10,16-17H, 1H2, (H, 21,22 ) (H, 23,24) (H2,11 ,12,13) (H2,18,19,20) / t4-, 6-, 7-, 10- / m1 / s1 Std. InChIKey: ZKHQWZAMYRWXGA-KQYNXXCUSA-N |
| Proprietà chimiche | |
| Formula |
C 10 H 16 N 5 O 13 P 3 [Isomeri] |
| Massa molare | 507.181 ± 0,014 g / mol C 23,68%, H 3,18%, N 13,81%, O 41,01%, P 18,32%, |
| Unità di SI e STP se non diversamente indicato. | |
L' adenosina trifosfato o ATP , è un nucleotide formato da un nucleoside a un trifosfato . Nella biochimica di tutti gli esseri viventi conosciuti, l'ATP fornisce l'energia necessaria per le reazioni chimiche nel metabolismo , per la locomozione , per la divisione cellulare o per il trasporto attivo di specie chimiche attraverso le membrane biologiche . Per rilasciare questa energia, la molecola di ATP viene scissa , per idrolisi , in adenosina difosfato (ADP) e fosfato , una reazione che è accompagnata da una variazione dell'entalpia libera standard ΔG 0 ′ di -30,5 kJ mol -1 . Le cellule quindi rigenerano l'ATP dall'ADP essenzialmente in tre modi: per fosforilazione ossidativa nel contesto della respirazione cellulare , per fotofosforilazione come parte della fotosintesi , e per fosforilazione al substrato durante alcune reazioni chimiche esoergoniche , ad esempio durante la glicolisi o il ciclo di Krebs . Pertanto, il corpo umano contiene in qualsiasi momento solo circa 250 g di ATP, ma consuma e rigenera ogni giorno dell'ordine del proprio peso in ATP.
- Nelle cellule , l'ATP viene continuamente idrolizzato ad ADP e rigenerato dall'ADP.
La molecola di ATP è un gruppo trifosfato legato all'atomo di carbonio 5' di un residuo di ribosio , un pentoso , compreso l'atomo di carbonio 1' è legato all'atomo di azoto 9' di un residuo di adenina , una base purina . I due legami P – O – P fosfoanidride del gruppo trifosfato sono legami ad alto potenziale di trasferimento, vale a dire che la loro scissione per idrolisi libera una grande quantità di energia: questa è una reazione esoergonica . L'accoppiamento di una tale reazione esoergonica con una reazione endorgonica , cioè che assorbe energia, è in grado di rendere quest'ultima termodinamicamente possibile. In questo modo le reazioni metaboliche che richiedono un apporto di energia, come le reazioni di biosintesi , che spontaneamente si verificano molto lentamente o per niente, possono avvenire molto più velocemente nelle cellule.
L'ATP è il precursore di una serie di cofattori enzimatici importanti come il NAD + o CoA . È anche un coenzima di trasferimento del gruppo fosfato associato in modo non covalente con enzimi della famiglia delle chinasi . Questi ultimi sono coinvolti nella trasduzione di alcune vie di segnalazione cellulare , per fosforilazione di proteine ed enzimi bersaglio, la cui attività è così regolata, o per fosforilazione di lipidi . L'ATP è anche il substrato per l' adenilato ciclasi , che lo converte in AMP ciclico . Si tratta di un messaggero intracellulare secondario , subentrando in particolare a ormoni come il glucagone e l' adrenalina per agire sul metabolismo del glicogeno , dei carboidrati e dei lipidi in genere. Il rapporto tra la concentrazione di ATP e la concentrazione di AMP viene utilizzato dalle cellule per determinare il loro carico energetico, ovvero la quantità di energia di cui dispongono, che consente loro, a seconda dei casi, di indirizzare il proprio metabolismo verso la produzione o l'immagazzinamento di energia metabolica. Inoltre, l'ATP viene utilizzato dalle RNA polimerasi nel processo di trascrizione del DNA in RNA ribosomiale e in RNA messaggero .
L'ATP è stato scoperto nel 1929 dal biochimico tedesco Karl Lohmann e, in parallelo, dai biochimici americani Cyrus Fiske e dall'indiano Yellapragada Subbarao (in) . Fu il tedesco Fritz Albert Lipmann a suggerirgli di svolgere il ruolo di intermediario tra le reazioni che rilasciano energia e le reazioni che la assorbono. L'ATP è stato sintetizzato per la prima volta in laboratorio nel 1948 da Alexander Robert Todd .
Proprietà
Fisica e chimica
L'ATP è costituito da adenina , ribosio e tre gruppi fosfato che formano un gruppo trifosfato . Questi tre gruppi fosfato sono designati, dal ribosio verso l'esterno, dalle lettere greche α ( alpha ), β ( beta ) e γ ( gamma ). ATP è quindi strettamente legata alla AMP , uno dei monomeri di RNA , e ad umido , uno dei monomeri di DNA . L'ATP è molto solubile in acqua. Rimane relativamente stabile in soluzione acquosa per pH tra 6,8 e 7,4, ma viene rapidamente idrolizzata da più acide o più basilare pH . Pertanto, l'ATP viene conservato al meglio come sale anidro .
L'ATP, invece, è instabile non appena non si trova più in una soluzione tampone a pH neutro. Quindi idrolizza in ADP e fosfato. Questo perché i legami idrogeno tra le molecole d'acqua da un lato e l'ADP e il fosfato dall'altro sono più forti dei legami P – O – P fosfoanidride che uniscono i gruppi fosfato tra loro nella molecola di ATP. Pertanto, l'ATP tende a dissociarsi quasi interamente in ADP e fosfato dopo un tempo più o meno lungo quando è in soluzione in acqua.
In una soluzione acquosa neutra, l'ATP disciolto viene ionizzato quattro volte per formare l' anione ATP 4- , con una piccola proporzione di ioni ATP 3- .
Poiché l'ATP ha diversi gruppi carichi negativamente in una soluzione neutra, può chelare i cationi del metallo con elevata affinità. Il valore molare della costante di legame per alcuni di questi comuni cationi metallici è il seguente:
Queste interazioni sono abbastanza forti che la maggior parte dell'ATP 4- è presente nelle cellule complessate con Mg 2+ .
Termodinamica
Quando un sistema termodinamico è lontano dall'equilibrio, ha un'entalpia libera che gli consente di svolgere un lavoro , in senso termodinamico . Le cellule viventi mantengono un rapporto di concentrazione tra ATP e ADP vicino a 5, che è circa dieci ordini di grandezza superiore al rapporto di concentrazione che si stabilisce all'equilibrio, dove quasi tutto l'ATP è dissociato in ADP e fosfato. A causa di questa deviazione dall'equilibrio, l'idrolisi dell'ATP in ADP e fosfato rilascia una grande quantità di energia.
È l'idrolisi dei due legami fosfoanidride che legano i gruppi fosfato adiacenti di ATP che rilascia l'energia di questa molecola. Per questo motivo, per comodità ma impropriamente, questi legami di fosfoanidride sono spesso indicati come legami ricchi di energia. Questa caratteristica è però fuorviante, perché questi legami non contengono di per sé più energia degli altri, e la loro rottura richiede un contributo di energia di attivazione come per la rottura di qualsiasi altro legame; è solo il loro ambiente molecolare che la loro idrolisi è esoergonica , con una variazione di entalpia libera standard di -30,5 kJ mol -1 (negativa perché l'energia viene rilasciata durante la reazione):
ATP + 2 H 2 O→ ADP + Pi + H 3 O + : ΔG 0 ′ = −30,5 kJ mol −1 .Al contrario, la reazione di fosforilazione dell'ADP in ATP è endorgonica , con una variazione di entalpia libera standard di 30,5 kJ mol -1 (positiva perché l'energia viene assorbita durante la reazione):
ADP + Pi + H 3 O +→ ATP + 2 H 2 O : ΔG 0 ′ = 30,5 kJ mol −1 .La reazione di idrolisi dell'ATP in AMP e pirofosfato HP 2 O 7 3-è più esoergonico, con una variazione di entalpia libera standard di -45,6 kJ mol -1 :
ATP + 2 H 2 O→ AMP + PPi + H 3 O + : ΔG 0 ′ = −45,6 kJ mol −1 .Funzioni biologiche
Metabolismo, organizzazione e mobilità delle cellule
L'ATP viene consumato nelle cellule da processi biochimici e fisiologici che richiedono energia, noti come endergonici , e continuamente rigenerati da processi che rilasciano energia, noti come esoergonici . In questo modo, l'ATP consente il trasferimento di energia tra processi spazialmente separati. È la principale fonte di energia per la stragrande maggioranza delle funzioni cellulari, come il metabolismo , la biosintesi , il trasporto attivo attraverso le membrane biologiche , o anche la motilità delle cellule e la locomozione di organismi complessi ( contrazione muscolare ).
L'ATP è anche coinvolto nel mantenimento della struttura cellulare e nella sua mobilità facilitando l'assemblaggio e il disassemblaggio degli elementi del citoscheletro . Allo stesso modo, fornisce l'energia per la contrazione muscolare catalizzando l'accorciamento dei filamenti di actina e miosina , che è un bisogno essenziale degli animali , essenziali per la loro locomozione e respirazione - sia dal punto di vista della ventilazione dei loro polmoni che dal funzionamento del loro cuore , responsabile della circolazione del loro sangue ossigenato in tutto il corpo .
Segnalazione cellulare
L'ATP partecipa ai meccanismi di segnalazione cellulare venendo riconosciuto dai recettori purinergici (in) , che sono forse i recettori più abbondanti nei tessuti dei mammiferi . In esseri umani , questo ruolo di segnalazione cellulare è importante sia nel sistema nervoso centrale e del sistema nervoso periferico . I recettori P2-purinergici vengono quindi attivati dal rilascio di ATP da sinapsi , assoni e cellule gliali . I recettori P2Y (in) sono ad esempio recettori accoppiati alla proteina G che modulano i livelli intracellulari di calcio e, talvolta, quello di AMP ciclico .
All'interno delle cellule, l'ATP viene utilizzato dalle chinasi come fonte di gruppi fosfato per effettuare le fosforilazioni . La fosforilazione delle proteine e dei lipidi di membrana sono forme comuni di trasduzione del segnale . Ad esempio, si osserva un'attivazione di proteine mediante fosforilazioni a cascata con MAP chinasi . L'ATP è anche il substrato per l' adenilato ciclasi , che produce AMP ciclico , un messaggero secondario che innesca il rilascio di calcio dai suoi punti di stoccaggio intracellulari. Questa forma di trasduzione del segnale è particolarmente importante nel funzionamento del cervello , sebbene sia coinvolta anche in una moltitudine di altri processi cellulari.
- Conversione di ATP in AMP ciclico mediante adenilato ciclasi .
Replicazione del DNA e trascrizione in RNA
In tutti gli esseri viventi conosciuti, i desossiribonucleotidi che costituiscono il DNA sono prodotti da una ribonucleotide reduttasi (RNR) dai corrispondenti ribonucleotidi . Questi enzimi riducono il residuo di ribosio nel desossiribosio con un gruppo sulfidrilico -SH di un residuo di cisteina che forma un legame disolfuro con un altro residuo di cisteina nella reazione. La loro forma ridotta viene rigenerata sotto l'azione della tioredossina o della glutaredossina .
La regolazione delle ribonucleotidi reduttasi e degli enzimi correlati mantiene l'equilibrio nella cellula tra deossiribonucleotidi e ribonucleotidi l'uno rispetto all'altro. Una concentrazione troppo bassa di desossiribonucleotidi inibisce la riparazione e la replicazione del DNA , che alla fine uccide la cellula, mentre una relazione anormale tra le concentrazioni di diversi desossiribonucleotidi è mutagena a causa dell'aumentata probabilità di "incorporare una base nucleica errata durante la replicazione del DNA da parte delle DNA polimerasi" . La regolazione o le differenze di specificità delle ribonucleotidi reduttasi sono forse all'origine dell'alterazione di questo equilibrio all'interno del pool di desossiribonucleotidi osservata in una situazione di stress cellulare come l' ipossia .
Durante la trascrizione del DNA in RNA ribosomiale e RNA messaggero , l'ATP è uno dei quattro nucleotidi incorporati nell'RNA dalle RNA polimerasi . L'energia necessaria per alimentare questa polimerizzazione deriva dall'idrolisi del gruppo pirofosfato dell'ATP. Il processo è lo stesso della biosintesi del DNA, tranne per il fatto che viene utilizzato l'ATP al posto della deossiadenosina trifosfato (dATP).
Rigenerazione
La concentrazione intracellulare di ATP è tipicamente dell'ordine di 1-10 mmol/L . L'ATP può essere rigenerato dall'ADP mediante l'energia rilasciata dall'ossidazione di carboidrati o lipidi attraverso un insieme di processi chiamati respirazione cellulare . Per ogni molecola di glucosio ossidata possono essere prodotte circa 30 molecole di ATP . Le ose (zuccheri) sono già molecole parzialmente ossidate, per cui un acido grasso può generare più molecole di ATP per atomo di carbonio (16 per il palmitato e 6 per il glucosio) e costituiscono la maggior parte delle riserve e degli apporti energetici per l'organismo; ma gli zuccheri, essendo solubili in acqua, sono più facilmente disponibili e ossidabili. La maggior parte dell'ATP prodotto dagli eucarioti non fotosintetici proviene dalla fosforilazione ossidativa all'interno dei mitocondri . La β-ossidazione e il ciclo di Krebs avvengono anche nei mitocondri, che possono occupare fino a un quarto del volume di una cellula; il resto dell'ATP prodotto da questi organismi viene rigenerato per fosforilazione a livello del substrato , ad esempio durante la glicolisi o per fermentazione nel citoplasma . Le piante e i batteri fotosintetici , a loro volta, producono ATP essenzialmente fotofosforilazione .
glicolisi
Il glucosio viene convertito in piruvato da una via metabolica chiamata glicolisi . La maggior parte degli esseri viventi realizza questa trasformazione nel citoplasma delle proprie cellule , ma alcuni protozoi , come quelli della classe dei cinetoplastidi , la conducono in organelli specializzati chiamati glicosomi . Per ogni molecola di glucosio ossidata per questa via vengono prodotte due molecole di ATP, a livello di due enzimi che effettuano la fosforilazione a livello del substrato : fosfoglicerato chinasi e piruvato chinasi . Dal NAD + vengono prodotte anche due molecole di NADH , che possono essere ossidate dalla catena respiratoria e produrre ulteriori molecole di ATP. Il piruvato prodotto alla fine della glicolisi è un substrato del ciclo di Krebs .
ciclo di Krebs
Nei mitocondri , il piruvato viene ossidato dal complesso della piruvato deidrogenasi per formare acetil-CoA . Quest'ultimo viene ossidato a CO 2, NADH e FADH 2dal ciclo di Krebs , anche con produzione di GTP , che è energeticamente equivalente ad ATP.
NADH e FADH 2trasferiscono i loro elettroni ad alto potenziale di trasferimento alla catena respiratoria , che produce ulteriori molecole di ATP per fosforilazione ossidativa , a una velocità da 2 a 3 molecole di ATP per molecola di NADH e da 1 a 2 molecole di ATP per FADH 2. La maggior parte dell'ATP nelle cellule non fotosintetiche viene prodotta in questo modo. Sebbene il ciclo di Krebs non richieda direttamente la presenza di ossigeno O 2, non può funzionare senza di essa perché è l'ossigeno che funge da accettore finale di elettroni nella catena respiratoria, consentendo la rigenerazione di NAD + e FAD da NADH e FADH 2prodotta dal ciclo di Krebs: in assenza di ossigeno, quest'ultimo cessa di funzionare per mancanza di NAD + e FAD.
Fosforilazione ossidativa
Il flusso di elettroni attraverso la catena respiratoria consente ai protoni di essere pompati fuori dalla matrice mitocondriale , che genera un potenziale elettrochimico di membrana attraverso la membrana mitocondriale interna a causa del risultante gradiente di concentrazione di protoni . La dissipazione del potenziale di membrana elettrochimica sintasi ATP fornisce l'energia necessaria per la fosforilazione di ADP in ATP: questo viene indicato come accoppiamento chemiosmotico tra la catena respiratoria e fosforilazione di ADP. L'ATP sintasi è un enzima complesso che possiede un rotore molecolare azionato dal riflusso di protoni dallo spazio intermembrana mitocondriale e che trasmette l'energia di quest'ultimo al livello di fosforilazione dell'ADP.
La rigenerazione dell'ATP nei mitocondri da NADH prodotto nel citosol comporta il passaggio della membrana mitocondriale interna attraverso NADH alla matrice mitocondriale e NAD + nell'altra direzione. Infatti, queste molecole non possono attraversare da sole questa membrana, quindi sono i loro elettroni ad alto potenziale di trasferimento che la attraversano. Gli eucarioti usano essenzialmente due modi per farlo: lo shuttle malato-aspartato e, in misura minore, lo shuttle del glicerolo 3-fosfato .
- La navetta malato-aspartato coinvolge prima una malato deidrogenasi , che riduce una molecola di ossalacetato citosolico a malato . Quest'ultimo può attraversare la membrana mitocondriale interna prendendo in prestito un antiporto malato -α-chetoglutarato , e, raggiunta la matrice mitocondriale , il malato viene nuovamente ossidato ad ossalacetato da un'isoforma mitocondriale della mitocondriale malato deidrogenasi (mMDH), convertendo una molecola di NAD + in NADH. L'ossalacetato mitocondriale viene convertito in aspartato sotto l'azione di un'aspartato aminotransferasi mitocondriale (mAST) mediante trasferimento di un gruppo amminico dal glutammato , quest'ultimo dando poi α-chetoglutarato . L'aspartato prende in prestito un'antiporta glutammato-aspartato per attraversare la membrana mitocondriale interna e unirsi al citosol, mentre l' α-chetoglutarato fa lo stesso utilizzando un antiporta malato-α-chetoglutarato . L'aspartato citosolico viene convertito in ossalacetato dall'aspartato aminotransferasi citosolico (cAST), che produce anche glutammato dall'α-chetoglutarato .
- Lo shuttle glicerolo-3-fosfato è meno diffuso del precedente ma non richiede l'attraversamento della membrana mitocondriale interna, il che lo rende più veloce anche se porta alla generazione di meno ATP per molecola di NADH ossidato, tanto da essere utilizzato di preferenza da cellule che richiedono una rapida mobilitazione di grandi quantità di energia, vale a dire principalmente i muscoli e il cervello . Una glicerolo-3-fosfato deidrogenasi solubile ( EC ) converte prima il diidrossiacetone fosfato (DHAP) in glicerolo-3-fosfato , che rigenera NAD + da NADH. Una membrana mitocondriale interna la glicerolo-3-fosfato deidrogenasi ( EC ) scarica elettroni dal glicerolo-3-fosfato su una molecola FAD per dare FADH 2e rigenerante DHAP; il FADH 2a sua volta riduce un ubichinone , i cui elettroni si uniscono poi alla catena respiratoria a livello del coenzima Q - citocromo c reduttasi (complesso III ).
Traslocazione ATP/ADP
Analogamente a quanto osservato per il NAD + , l'ATP rigenerato nei mitocondri viene consumato principalmente nel citoplasma e nel nucleo , dove si forma l' ADP che deve essere fosforilato ad ATP all'interno delle cellule mitocondri. Questi flussi di materiale comportano la circolazione dell'ADP attraverso la membrana mitocondriale interna dal citosol alla matrice mitocondriale, mentre l'ATP rigenerato nei mitocondri attraversa questa membrana nella direzione inversa per essere consumato nel citosol e nel nucleo. Poiché la membrana mitocondriale interna è impermeabile anche all'ADP e all'ATP, queste molecole devono prendere in prestito proteine integrali di membrana chiamate ATP/ADP traslocasi per attraversarla.
Nelle piante , l'ATP è prodotto dalla fotofosforilazione nella membrana dei tilacoidi all'interno dei cloroplasti . Il principio è simile a quello attuato nell'ambito della fosforilazione ossidativa , con un accoppiamento chemiosmotico della stessa natura, con la differenza che l'energia proviene dai fotoni catturati dai pigmenti fotosintetici e non dall'ossidazione di carboidrati e lipidi . Parte di questo ATP viene consumato nel cloroplasto per produrre carboidrati attraverso il ciclo di Calvin .
Le scorte di ATP del corpo non superano alcuni secondi di consumo. In linea di principio, l'ATP viene costantemente riciclato e qualsiasi processo che ne blocchi la rigenerazione provoca rapidamente la morte dell'organismo contaminato. È il caso ad esempio di alcuni gas da combattimento progettati per questo scopo, o di veleni, come il cianuro , che blocca la citocromo c ossidasi della catena respiratoria nei mitocondri , o l' arsenico , che sostituisce il fosforo e rende inutilizzabili le molecole di fosforo.
La creatina può fungere da accumulatore immagazzinando un trasferimento di gruppo fosfato ad alto potenziale da una molecola di ATP, che può essere successivamente trasferito a una molecola di ADP per rigenerare l'ATP:
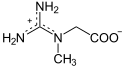
|
+ ATP ADP + |

|
| Creatina | Fosfocreatina | |
| Creatina chinasi - EC | ||
ATP come tale non può essere immagazzinato nelle cellule, così energia metabolica è memorizzata per esempio come lipidi nel tessuto adiposo o carboidrati come glicogeno in animali o amido in animali. Piante .
Regolamento
La produzione di ATP in cellule di eucarioti aerobico è strettamente regolata da allosterica , per il feedback e dalla concentrazione dei substrati di vari enzimi della glicolisi e la fosforilazione ossidativa . I checkpoint si trovano in reazioni così termodinamicamente favorevoli da essere di fatto irreversibili in condizioni fisiologiche.
glicolisi
L' esochinasi è direttamente inibita dal prodotto della reazione che catalizza , cioè il glucosio 6-fosfato , mentre la piruvato chinasi è inibita dallo stesso ATP. Il principale punto di regolazione della glicolisi è la fosfofruttochinasi (PFK), che è inibita allostericamente quando l'ATP è abbondante, ma viene attivata quando l' AMP è abbondante. L'inibizione di questo enzima da parte dell'ATP è insolita poiché l'ATP è un substrato per la reazione che catalizza. La forma biologicamente attiva di questo enzima è un tetramero che esiste in due possibili conformazioni, di cui solo una può legarsi al fruttosio-6-fosfato , che è il secondo substrato di questo enzima. La proteina ha due siti di legame dell'ATP: il sito attivo è accessibile in entrambe le conformazioni, ma il legame dell'ATP al sito inibitorio stabilizza la conformazione che si lega solo debolmente al fruttosio-6-fosfato. Un certo numero di altre piccole molecole sono in grado di compensare l'effetto inibitorio dell'ATP e quindi di riattivare la fosfofruttochinasi; è ad esempio il caso dell'AMP ciclico , degli ioni ammonio , degli ioni fosfato , del fruttosio 1,6-bisfosfato e del fruttosio 2,6-bisfosfato .
ciclo di Krebs
Il ciclo di Krebs è essenzialmente regolato dalla disponibilità dei suoi substrati chiave, in particolare dal rapporto tra la concentrazione di NAD + e NADH , nonché le concentrazioni di calcio , fosfato , ATP, ADP e AMP . Il citrato è un inibitore della citrato sintasi che agisce per feedback e un inibitore della fosfofruttochinasi , che lega la regolazione del ciclo di Krebs a quella della glicolisi .
Fosforilazione ossidativa
La regolazione della fosforilazione ossidativa si basa essenzialmente sulla citocromo c ossidasi , che è regolata dalla disponibilità del suo substrato, ovvero il citocromo c ridotto. La quantità di citocromo c ridotto disponibile dipende direttamente dalla quantità di altri substrati:
1 ⁄ 2 NADH + cyt c ossidato + ADP + Pi 1 ⁄ 2 NAD + + cyt c ridotto + ATP,da qui la seguente equazione, dedotta da questo equilibrio:
Pertanto, un elevato rapporto di concentrazione [NADH] ⁄ [NAD + ] o un elevato rapporto di concentrazione [ADP] [Pi] ⁄ [ATP] (a destra di questa uguaglianza) implica un [ ridotto cyt c ] ⁄ rapporto di concentrazione [ ossidato cyt c ] (arto sinistro), cioè un'elevata concentrazione di citocromo c ridotto e una forte attività della citocromo c ossidasi.
Un ulteriore livello di regolazione è introdotto dalla velocità di trasporto di ATP e NADH tra la matrice mitocondriale e il citosol .
Legami proteici
Alcune proteine che si legano all'ATP hanno un ripiegamento caratteristico chiamato piega di Rossmann , un motivo strutturale generale delle proteine che si legano ai nucleotidi , come quelle che si legano al NAD . Le più comuni proteine che legano l'ATP, chiamate chinasi , condividono alcune caratteristiche strutturali comuni. Le protein chinasi , che sono il gruppo più numeroso di chinasi e condividono caratteristiche strutturali specializzate nel legame dell'ATP e nei trasferimenti di gruppi fosfato.
L'ATP richiede generalmente la presenza di un catione bivalente per formare un complesso con le proteine . È quasi sempre un catione di magnesio Mg 2+ , che si lega ai gruppi fosfato dell'ATP. Questo catione riduce significativamente la costante di dissociazione del complesso ATP-proteina senza influenzare la capacità dell'enzima di catalizzare la sua reazione chimica una volta che l'ATP è legato. La presenza di cationi magnesio può costituire un meccanismo di regolazione delle chinasi.
Analoghi dell'ATP
Gli esperimenti in vitro sono spesso utilizzati per studiare i processi biochimici che coinvolgono l'ATP e gli inibitori di enzimi che utilizzano l'ATP, come le chinasi , sono strumenti utili per esaminare gli stati di legame e di transizione coinvolti nelle reazioni che coinvolgono l'ATP. Sono anche usati come l' ATP nella cristallografia a raggi X per determinare la struttura delle proteine che formano un complesso con l'ATP, spesso in combinazione con altri substrati. Gli analoghi dell'ATP più utili sono quelli che non si idrolizzano come farebbe l'ATP e bloccano l'enzima in uno stato vicino al complesso ATP-enzima. L' adenosina 5'- [γ-tio] trifosfato (ATPγS), ad esempio, è un analogo dell'ATP molto comunemente usato in laboratorio: uno degli atomi di ossigeno del fosfato γ è sostituito da un atomo di zolfo , e ATPγS idrolizza ad una velocità notevolmente più lenta di quella dell'ATP, per cui agisce da inibitore dei processi dipendenti dall'idrolisi di una molecola di ATP. Esistono però enzimi in grado di idrolizzarli a velocità piuttosto elevate quando sono in concentrazione sufficiente, il che implica dover interpretare con cautela i risultati ottenuti con tali inibitori.
In cristallografia, gli stati di transizione all'idrolisi vengono studiati utilizzando complessi di ioni vanadato .
Note e riferimenti
- massa molecolare calcolata da " Pesi atomici degli elementi 2007 " su www.chem.qmul.ac.uk .
- (in) cambiamento di energia libera , sul sito di Marc Kirschner (in) , Harvard Medical School .
- (in) " Le batterie della natura" potrebbero aver aiutato le prime forme di vita " su Science Daily , 25 maggio 2010(consultato il 23 agosto 2016 )
- (in) David E. Bryant, Katie ER Marriott Stuart A. Macgregor, Colin Kilner, Matthew A. Pasek e Terence P. Kee , " Sul potenziale prebiotico dello stato di ossidazione del fosforo ridotto: il sistema piruvato H-fosfinato " , Chimica Comunicazioni , vol. 46, n . 21, 7 giugno 2010, pag. 3726-3728 ( PMID 20386792 , DOI 10.1039/C002689A , Bibcode 2010LPICo1538.5264B , leggi online )
- (in) Susanna Törnroth-Horsefield e Richard Neutze , " Apertura e chiusura del metabolita del cancello " , Atti della National Academy of Sciences degli Stati Uniti d'America , vol. 105, n . 50, 16 dicembre 2008, pag. 19565-19566 ( PMID 19073922 , PMCID 2604989 , DOI 10.1073/pnas.0810654106 , leggi online )
- (in) Eunus S. Ali, Hua Jin, Claire H. Wilson, George A. Tallis, Fiona H. Zhou, Y. Grigory Rychkov e Greg J. Barritt , " L'analogo del peptide-1 simile al glucagone exendin-4 si inverte alterata segnalazione intracellulare di Ca 2+ negli epatociti steatotici ” , Biochimica et Biophysica Acta (BBA) - Molecular Cell Research , vol. 1863 n ° 9, settembre 2016, pag. 2135-2146 ( PMID 27178543 , DOI 10.1016 / j.bbamcr.2016.05.06 , leggi online )
- (in) D. Grahame Hardie e Simon A. Hawley , " Proteina chinasi attivata da AMP: rivisitata l'ipotesi del carico di energia " , BioEssays , vol. 23, n . 12, dicembre 2001, pag. 1112-1119 ( PMID 11746230 , DOI 10.1002 / bies.10009 , leggi online )
- (in) Karl Lohmann , " Über die im Pyrophosphatfraktion Muskel " , Naturwissenschaften , vol. 17, n . 31, agosto 1929, pag. 624-625 ( DOI 10.1007 / BF01506215 , leggi in linea )
- (in) Koscak Maruyama , " La scoperta dell'adenosina trifosfato e l'istituzione della sua struttura " , Journal of the History of Biology , vol. 24, n ° 1, marzo 1991, pag. 145-154 ( DOI 10.1007 / BF00130477 , JSTOR 4331161 , leggi online )
- (in) AC Storer e A. Cornish-Bowden , " Concentrazione di MgATP 2 e altri ioni in soluzione. Calcolo delle vere concentrazioni di specie presenti in miscele di ioni associati ” , Biochemical Journal , vol. 159, n ° 1, ottobre 1976, pag. 1-5 ( PMID 11772 , PMCID 1164030 , DOI 10.1042/bj1590001 , leggi online )
- (in) John E. Wilson e Arnold Chin , " Chelation of bivalent cations by ATP Studyed by titotion calorimetry " , Analytical Biochemistry , vol. 193, n . 1, 15 febbraio 1991, pag. 16-19 ( PMID 1645933 , DOI 10.1016 / 0003-2697 (91) 90036-S , leggi online )
- (in) " Il magnesio nel metabolismo energetico cardiaco " , Journal of Molecular and Cellular Cardiology , vol. 18, n . 10, ottobre 1986, pag. 1003-1013 ( PMID 3537318 , DOI 10.1016 / S0022-2828 (86) 80289-9 , leggi online )
- (in) Britton Chance, Howard Lees e John R. Postgate , " The Meaning of" Reversed Electron Flow "e" High Energy Electron "in Biochemistry " , Letters to Nature , vol. 238, n . 5363, 11 agosto 1972, pag. 330-331 ( PMID 4561837 , DOI 10.1038/ 238330a0 , leggi online )
- Biologia molecolare della cellula Di Harvey Lodish, Arnold Berk, Paul Matsudaira, James Darnell , Chris A. Kaiser, Pierre L. Masson - pagina 301
- (in) Neeti Sanan Mishra e Renu Tuteja Narendra Tuteja , " Segnalazione attraverso reti di chinasi MAP nelle piante " , Archivi di biochimica e biofisica , vol. 452, n ° 1, agosto 2006, pag. 55-68 ( PMID 16806044 , DOI 10.1016 / j.abb.2006.05.001 , leggi online )
- (in) Margarita Kamenetsky Sabine Middelhaufe, Erin M. Bank, Lonny R. Levin, Jochen Buck e Clemens Steegborn , " Dettagli molecolari della generazione di cAMP nelle cellule dei mammiferi: una storia di due sistemi " , Journal of Molecular Biology , vol. 362, n . 4, 29 settembre 2006, pag. 623-639 ( PMID 16934836 , PMCID 3662476 , DOI 10.1016 / j.jmb.2006.07.045 , leggi online )
- (in) Jacques e Nicole Defer Hanoune , " Regolazione e ruolo delle isoforme dell'adenilato ciclasi " , Revisione annuale di farmacologia e tossicologia , vol. 41, aprile 2001, pag. 145-174 ( PMID 11264454 , DOI 10.1146 / annurev.pharmtox.41.1.145 , leggi online )
- (in) JoAnne Stubbe , " Ribonucleotide reduttasi: sorprendente e confuso " , Journal of Biological Chemistry , vol. 265, n . 10, 5 aprile 1990, pag. 5329-5332 ( PMID 2180924 , leggi online )
- (in) Catherine M. Joyce e Thomas A. Steitz , " Struttura e funzione della polimerasi: variazioni su un tema? ” , Giornale di batteriologia , vol. 177, n . 22, novembre 1995, pag. 6321-6329 ( PMID 7592405 , PMCID 177480 , leggi online )
- (in) I. Beis e EA Newsholme , " Il contenuto di adenina nucleotidi, intermedi glicolitici e alcuni fosfageni nei muscoli a riposo di vertebrati e invertebrati " , Biochemical Journal , vol. 152, n ° 1, ottobre 1975, pag. 23-32 ( PMID 1212224 , PMCID 1172435 , DOI 10.1042/bj1520023 , leggi online )
- (en) PR Rich , “ Il macchinario molecolare della catena respiratoria di Keilin ” , Transazioni della società biochimica , vol. 31, n . 6, dicembre 2003, pag. 1095-1105 ( PMID 14641005 , DOI 10.1042/bst0311095 , leggi online )
- http://biochimej.univ-angers.fr/Page2/COURS/Zsuite/3BiochMetab/8BetaOxydation/1BetaOxydation.htm
- (in) Marilyn Parsons , " glicosomi: parassiti e divergenza di scopo perossisomiale " , Microbiologia molecolare , vol. 53, n . 3, agosto 2004, pag. 717-724 ( PMID 15255886 , DOI 10.1111 / j.1365-2958.2004.04203.x , leggi online )
- (in) Jan Pieter Abrahams Andrew GW Leslie Rene Lutter e John E. Walker , " struttura a 2,8 di risoluzione di F1-ATPasi dai mitocondri del cuore bovino " , Nature , vol. 370, n . 6491, 25 agosto 1994, pag. 621-628 ( PMID 8065448 , DOI 10.1038 / 370621a0 , leggi online )
- (in) John F. Allen , " Fotosintesi di ATP Electron, Proton Pumps, Rotors, and Poise " , Cell , vol. 110, n . 3, 9 agosto 2002, pag. 273-276 ( PMID 12176312 , DOI 10.1016 / S0092-8674 (02) 00870-X , leggi online )
- (in) C. Dahout-Gonzalez, H. Nury, V. Trezeguet, GJ-M. Lauquin, E. Pebay-Peyroula e G. Brandolin , " Aspetti molecolari, funzionali e patologici del vettore mitocondriale di ADP/ATP " , Fisiologia , vol. 21, n ° 4, 25 luglio 2005, pag. 242-249 ( PMID 16868313 , DOI 10.1152 / fisiol.00005.2006 , leggi online )
- (in) ST Rao e Michael G. Rossmann , " Confronto di strutture super-secondarie nelle proteine " , Journal of Molecular Biology , vol. 76, n . 2 15 maggio 1973, pag. 241, IN1, 251-250-256 ( PMID 4737475 , DOI 10.1016 / 0022-2836 (73) 90388-4 , leggi online )
- (in) Eric D. Scheeff e Philip E. Bourne , " Evoluzione strutturale della superfamiglia simile alla proteina chinasi " , PLoS Computational Biology , vol. 1, n . 5, ottobre 2005, e49 ( PMID 16244704 , PMCID 1261164 , DOI 10.1371 / journal.pcbi.0010049 , leggi online )
- (in) Phillip Saylor Chengqian Wang, John T. Hirai e Joseph A. Adams , " Un secondo ione di magnesio è fondamentale per il legame dell'ATP nel dominio della chinasi dell'oncoproteina v-fps " , Biochimica , vol. 37, n . 36, 8 settembre 1998, pag. 12624-12630 ( PMID 9730835 , DOI 10.1021/bi9812672 , leggi online )
- (in) Xiaofeng Lin, Marina K e Ayrapetov Gongqin Sun , " Caratterizzazione dell'interazione tra i siti attivi di una proteina tirosina chinasi e un attivatore di metalli bivalenti " , BMC Biochemistry , vol. 6, 23 novembre 2005, pag. 25 ( PMID 16305747 , PMCID 1316873 , DOI 10.1186 / 1471-2091-6-25 , leggi online )
- (in) Clive R. Bagshaw , " in sintesi analoghi dell'ATP " , Journal of Cell Science , vol. 114, n . 3, febbraio 2001, pag. 459-460 ( PMID 11171313 , leggi online )
- (in) SM Honigberg, DK Gonda, J. Flory e CM Radding , " L'accoppiamento di filamenti nucleoproteici ad attività costante costituiti da proteina RecA, DNA a filamento singolo e adenosina 5'- (gamma-tio)trifosfato " , del Journal Biological Chemistry , vol. 260, n . 21, 25 settembre 1985, pag. 11845-11851 ( PMID 3840165 , leggi online )
- (it) JA Dantzig, JW Walker, DR Trentham et YE Goldman , " Rilassamento delle fibre muscolari con adenosina 5 '- [gamma-tio] trifosfato (ATP [gamma S]) e mediante fotolisi laser di ATP in gabbia [gamma S] : prove dell'affinità dipendente dal Ca 2+ di ponti trasversali a forza zero a distacco rapido ” , Proceedings of the National Academy of Sciences degli Stati Uniti d'America , vol. 85, n . 18, settembre 1988, pag. 6716-6720 ( PMID 3413119 , PMCID 282048 , DOI 10.1073/pnas.85.18.6716 , JSTOR 32451 , Bibcode 1988PNAS ... 85.6716D , leggi online )
- (in) T. Kraft, SC Yu HJ Kuhn e B. Brenner , "L' effetto del Ca 2+ è una debole interazione del ponte incrociato con l'actina in presenza di adenosina 5 '- [gamma-tio] trifosfato) " , Atti di l'Accademia Nazionale delle Scienze degli Stati Uniti d'America , vol. 89, n . 23, dicembre 1992, pag. 11362-11366 ( PMID 1454820 , PMCID 50550 , DOI 10.1073/pnas.89.23.11362 , JSTOR 2360707 , Bibcode 1992PNAS ... 8911362K , leggi online )
- (in) Andrea M. e Joseph M. Resetar Chalovich , " Adenosina 5'- (gamma.-tiotrifosfato): un analogo dell'ATP che dovrebbe essere usato con cautela negli studi sulla contrazione muscolare " , Biochimica , vol. 34, n ° 49, 12 dicembre 1995, pag. 16039-16045 ( PMID 8519760 , DOI 10.1021/bi00049a018 , leggi online )

![{\ displaystyle {\ frac {[\ mathrm {cyt ~ c_ {ridotto}}]} {[\ mathrm {cyt ~ c_ {ossido}}]}} = \ left ({\ frac {[\ mathrm {NADH}] } {[\ mathrm {NAD}] ^ {+}}} \ destra) ^ {\ frac {1} {2}} \ sinistra ({\ frac {[\ mathrm {ADP}] [\ mathrm {P_ {i }}]} {[\ mathrm {ATP}]}} \ destra) K _ {\ mathrm {eq}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/89e75ceb7b27981ba88688fe6369101117a55af0)