Idrazina
| Idrazina | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 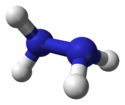 Dimensioni e modello 3D dell'idrazina |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identificazione | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nome IUPAC | idrazina | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sinonimi |
diazane, diammina |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100.005.560 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CE | 206-114-9 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 8058 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SORRISI |
NN , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1 / H4N2 / c1-2 / h1-2H2 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aspetto | Liquido igroscopico, incolore, fumoso con un odore pungente. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietà chimiche | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Formula bruta | N 2 H 4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Massa molare | 32,0452 ± 0,0007 g / mol H 12,58%, N 87,42%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Momento dipolare | 1,75 D | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Diametro molecolare | 0,390 nm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietà fisiche | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fusione | 2 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° bollitura | 114 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solubilità | miscibile con acqua e solventi organici polari |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Parametro di solubilità δ |
37,3 MPa 1/2 ( 25 ° C ) 36,2 J 1/2 · cm -3/2 ( 25 ° C ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Massa volumica |
1010 kg · m -3
equazione:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| punto d'infiammabilità | 38 ° C ( cf ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Limiti di esplosività in aria | 1,8 - 100 % vol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pressione del vapore saturo | anidro: 21 mbar ( 20 ° C ), soluzione al 64 % m : equazione:
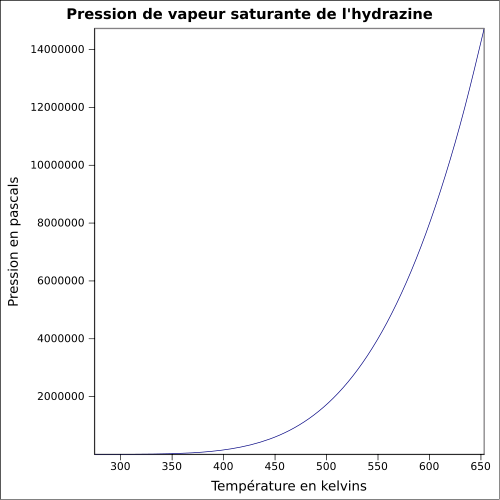
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Viscosità dinamica | 0,9 mPa · s a 25 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto critico | 147,0 bar , 379,85 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termochimica | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 gas, 1 bar | 238,68 J · K -1 · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 liquido, 1 bar | 121,52 J · K -1 · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 gas | 95,35 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 liquido | 50,63 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ vap H ° |
41,8 kJ · mol -1 ( 1 atm , 113,55 ° C ); 44,7 kJ · mol -1 ( 1 atm , 25 ° C ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C p |
equazione:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PC | 667,1 kJ · mol -1 ( 25 ° C , gas) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PCI | -622,08 kJ · mol -1 (gas) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietà elettroniche | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 re energia di ionizzazione | 8,1 ± 0,15 eV (gas) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietà ottiche | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Indice di rifrazione | 1.469 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Precauzioni | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
     Pericolo H226, H301, H311, H314, H317, H331, H350, H410, P201, P261, P273, P280, P301 + P310, P305 + P351 + P338, H226 : Liquido e vapori infiammabili H301 : Tossico se ingerito H311 : Tossico a contatto con la pelle H314 : Provoca gravi ustioni cutanee e gravi lesioni oculari H317 : Può provocare una reazione allergica cutanea H331 : Tossico se inalato H350 : Può provocare il cancro (indicare la via di esposizione se è definitivamente dimostrato che nessun'altra via di esposizione causa il pericolo) H410 : Molto tossico per gli organismi acquatici con effetti di lunga durata P201 : Procurarsi istruzioni speciali prima dell'uso. P261 : Evitare di respirare la polvere / i fumi / i gas / la nebbia / i vapori / gli aerosol. P273 : evitare il rilascio nell'ambiente. P280 : Indossare guanti / indumenti protettivi / Proteggere gli occhi / il viso. P301 + P310 : In caso di ingestione: contattare immediatamente un CENTRO ANTIVELENI o un medico. P305 + P351 + P338 : In caso di contatto con gli occhi: sciacquare accuratamente per parecchi minuti. Rimuovere le lenti a contatto se la vittima le indossa e possono essere rimosse facilmente. Continua a risciacquare. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
   B3, D1A, D2A, E, B3 : Liquido combustibile D1A : Materiale molto tossico che causa effetti gravi immediati D2A : Materiale molto tossico che causa altri effetti tossici E : Materiale corrosivo Divulgazione dello 0,1% secondo l'elenco di divulgazione degli ingredienti |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3 3 3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Altro | Può attaccare il sistema nervoso. Fatale a dosi elevate. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Trasporto | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
0113 : GUANYL NITROSAMINOGUANYLIDENE IDRAZINA UMIDIFICATA con almeno il 30 percento (massa) di acqua Classe: 1 Codice di classificazione: 1.1A : Sostanze e articoli che comportano un rischio di esplosione di massa (un'esplosione di massa è un'esplosione che colpisce quasi istantaneamente quasi intero carico). Materiale esplosivo primario. Etichetta: 1 : Materie e articoli esplosivi 
663 : materiale molto tossico e infiammabile (punto di infiammabilità uguale o inferiore a 60 ° C ) Numero UN : 1163 : DIMETILIDRAZINA ASIMMETRICA Classe: 6.1 Codice di classificazione: TFC : Sostanze tossiche corrosive infiammabili. ; Etichette: 6.1 : Materiali tossici 3 : Liquidi infiammabili 8 : Materiali corrosivi   
663 : materiale molto tossico e infiammabile (punto di infiammabilità uguale o inferiore a 60 ° C ) Numero UN : 1244 : METILIDRAZINA Classe: 6.1 Codice di classificazione: TFC : Sostanze tossiche corrosive infiammabili. ; Etichette: 6.1 : Materiali tossici 3 : Liquidi infiammabili 8 : Materiali corrosivi   
886 : materiale molto corrosivo e tossico Numero UN : 2029 : IDRAZINA ANIDRA Classe: 8 Codice di classificazione: CFT : Materie corrosive liquide, infiammabili, tossiche; Etichette: 8 : Materiali corrosivi 3 : Liquidi infiammabili 6.1 : Materiali tossici Confezione: Gruppo di imballaggio I : materiali molto pericolosi;   
86 : corrosivo o con un grado minore di corrosività e tossicità Numero ONU : 2030 : IDRATO DI IDRAZINA contenente più del 37% ma non più del 64% (massa) di idrazina; o HYDRAZINE AQUOUS SOLUTION contenente più del 37 percento ma non più del 64 percento (in massa) di idrazina Classe: 8 Codice di classificazione: CT1 : Corrosivi tossici: Liquidi; Etichette: 8 : Materie corrosive 6.1 : Materie tossiche Confezione: Gruppo di imballaggio I / II : sostanze molto / moderatamente pericolose;  
86 : corrosivo o con un grado minore di corrosività e tossicità Numero ONU : 2030 : IDRATO DI IDRAZINA contenente più del 37% ma non più del 64% (massa) di idrazina; o HYDRAZINE AQUOUS SOLUTION contenente più del 37 percento ma non più del 64 percento (in massa) di idrazina Classe: 8 Codice di classificazione: CT1 : Corrosivi tossici: Liquidi; Etichette: 8 : Materie corrosive 6.1 : Materie tossiche Confezione: Gruppo di imballaggio III : sostanze poco pericolose.  
663 : materiale molto tossico e infiammabile (punto di infiammabilità uguale o inferiore a 60 ° C ) Numero UN : 2382 : DIMETILIDRAZINA SIMMETRICA Classe: 6.1 Codice di classificazione: TF1 : Materiali tossici infiammabili: Liquidi; Etichette: 6.1 : Materiali tossici 3 : Liquidi infiammabili Confezione: Gruppo di imballaggio I : materiali molto pericolosi;  
60 : materiale tossico o che presenta un grado di tossicità minore Numero UN : 2572 : FENILIDRAZINA Classe: 6.1 Codice di classificazione: T1 : Sostanze tossiche senza rischio sussidiario: Organici, liquidi; Etichetta: 6.1 : Materie tossiche Confezione: Gruppo di imballaggio II : sostanze moderatamente pericolose; 
3165 : SERBATOIO DEL CARBURANTE DEL MOTORE IDRAULICO DELL'AEROMOBILE contenente una miscela di idrazina anidra e monometilidrazina (carburante M86) Classe: 3 Codice di classificazione: FTC : Liquidi infiammabili , tossici, corrosivi Etichette: 3 : Liquidi infiammabili 6.1 : Sostanze tossiche 8 : Sostanze corrosive Confezione: Gruppo di imballaggio I : sostanze molto pericolose;   
60 : materiale tossico o con un grado di tossicità minore Numero UN : 3293 : SOLUZIONE ACQUOSA DI IDRAZINA contenente non più del 37% (in massa) di idrazina Classe: 6.1 Codice di classificazione: T4 : Sostanze tossiche senza rischio sussidiario: Inorganico, liquido; Etichetta: 6.1 : Materie tossiche Confezione: Gruppo di imballaggio III : sostanze poco pericolose.  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Classificazione IARC | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gruppo 2B: Possibilmente cancerogeno per l'uomo | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ecotossicologia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LogP | -3.1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Soglia di odore | basso: 3 ppm alto: 4 ppm |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Unità di SI e STP se non diversamente specificato. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
L' idrazina , nome ufficiale diazane , di formula chimica N 2 H 4 e formula strutturale H 2 N-NH 2 , è un composto chimico liquido incolore con un odore che ricorda l' ammoniaca . È miscibile con l'acqua in tutte le proporzioni.
Le idrazine costituiscono anche una famiglia di composti chimici derivati dall'idrazina (H 2 N-NH 2 per sostituzione di uno o più atomi di H con radicali idrocarburici (ad esempio 2,4-dinitrofenilidrazina ).
La produzione annuale di idrazina è di 260.000 tonnellate. La maggior parte di questa produzione viene utilizzata come agente schiumogeno per la produzione di polimeri espansi. La parte restante di questa produzione è suddivisa in vari settori come la chimica organica per la sintesi di farmaci o la chimica inorganica per la produzione della sodio azide , l'agente esplosivo per il gonfiaggio degli " airbag " (airbag). L'idrazina può anche essere utilizzata come carburante per motori a razzo .
Struttura e proprietà molecolari
La struttura dell'idrazina si presenta come due molecole di ammoniaca accoppiate tra loro rimuovendo un idrogeno per ciascuna delle due molecole. Ciascuna subunità -NH 2 ha una forma piramidale. La distanza tra i due atomi di azoto è di 145 µm e la molecola assume una conformazione anticlinale. La coppia è doppia rispetto a quella dell'etano . Le sue proprietà strutturali assomigliano a quelle del perossido di idrogeno gassoso, che adotta una conformazione "asimmetrica" simile a una struttura alcano lineare, con una coppia elevata.
Ha le proprietà di una base paragonabile all'ammoniaca , ma 15 volte più debole.
Il sostituente su ciascuna ammina rende il doppietto elettronico meno disponibile per raccogliere un protone e quindi meno basico. L'idrazina è un nucleofilo migliore dell'ammoniaca a causa della repulsione tra i doppietti non leganti degli atomi di azoto adiacenti.
La seconda protonazione è più difficile:
[N 2 H 5 ] ++ H + → [N 2 H 6 ] 2+ ; K = 8,4 × 10-16L'idrazina è un agente riducente molto più forte in un ambiente di base che in un ambiente acido. (E = -0,23 V a pH = 0 ed E = -1,16 V a pH = 14). Quando l'idrazina reagisce con gli ossidanti si possono formare vari prodotti azotati, ma di solito è diazoto. La reazione dell'idrazina con il diossigeno forma diazoto e acqua, mentre rilascia una grande quantità di calore.
Idrazina N 2 H 4si degrada sotto l'azione del calore e dei raggi ultravioletti in azoto N 2, idrogeno H 2e ammoniaca NH 3.
Alcuni sali di idrazina sono esplosivi : nitrato idrazina , clorato idrazina perclorato idrazina e azide idrazonio.
Proprietà fisico-chimiche
L'idrazina anidra è un liquido incolore che fuma aria con un odore di ammina. La soglia di odore è di 3 ppm .
Sintesi
Theodor Curtius sintetizzò per la prima volta l'idrazina semplice nel 1889 attraverso la porta sul retro.
L'idrazina è prodotta dal processo di Olin Raschig da ipoclorito di sodio e ammoniaca , un metodo inventato nel 1907. Questo processo si basa sulla reazione delle clorammine con l'ammoniaca.
NH 2 Cl+ NH 3→ H 2 N - NH 2+ HCl .La necessaria monoclorammina prodotta in anticipo dalla reazione: NH 3 + HOCl → NH 2 Cl + H 2 OUna variante del processo di Olin Raschig è l'ossidazione dell'urea da parte dell'ipoclorito di sodio :
(H 2 N) 2 C = O+ NaOCl + 2 NaOH → N 2 H 4+ H 2 O+ NaCl + Na 2 CO 3.Nel ciclo Atofina-PCUK, l'idrazina viene prodotta in più fasi da acetone , ammoniaca e perossido di idrogeno. L'acetone e l'ammoniaca reagiscono prima per dare un'immina , seguita dalla reazione di ossidazione con perossido di idrogeno in ossaziridina , un eterociclo a tre atomi comprendente un atomo di carbonio, un atomo di azoto e un atomo di ossigeno, seguito da ammoniolisi che si traduce in idrazone , un processo che riunisce due atomi di azoto. L'idrazone reagisce con l'acetone in eccesso e l' acetone azina prodotta viene idrolizzata per formare idrazina, rigenerando l'acetone. A differenza del processo Raschig, questo metodo non genera sale. PCUK è associata a Ugine Kuhlmann , un produttore francese di prodotti chimici.
L'idrazina può anche essere prodotta con un metodo noto come processo di chetazina e perossido .
Nel 2001, Marc Strous, un microbiologo dell'Università di Nijmegen nei Paesi Bassi, ha scoperto che l'idrazina è prodotta da lieviti e un batterio oceanico, Brocadia anammoxidans , attraverso una reazione anammox effettuata in organelli specializzati chiamati anammoxosomi . Sono gli unici organismi viventi attualmente conosciuti in grado di produrre naturalmente idrazina.
Derivati
Sono noti molti derivati di sostituzione dell'idrazina e molti di essi sono prodotti naturalmente. Qualche esempio :
- la giromitrina (in) e l' agaritina (in) sono fenilidrazine presenti in una specie di funghi coltivati e commercializzati, l' Agaricus bisporus . La giromitrina viene metabolizzata a monometilidrazina ;
- l' iproniazide , l' idralazina e la fenelzina (en) sono farmaci a base di idrazina;
- l' 1,1-dimetilidrazina (UDMH) e l' 1,2-dimetilidrazina (en) sono idrazine in cui due atomi di idrogeno sono sostituiti da gruppi metilici ;
- la 2,4-dinitrofenilidrazina (2,4-DNPH) è comunemente usata per testare chetoni e aldeidi in chimica organica ;
- la fenilidrazina , C 6 H 5 NHNH 2 , idrazina è la prima ad essere scoperta.
Utilizzare in chimica
Le idrazine sono utilizzate nella sintesi di molte molecole organiche e molte di esse sono di importanza pratica nell'industria farmaceutica , come farmaco antitubercolare , nonché nei tessuti come colorante e nella fotografia.
Si trova anche nell'industria in generale e più particolarmente in miscela con acqua di alimentazione per caldaie a vapore. Il suo scopo è distruggere le ultime molecole di ossigeno e quindi prevenire la corrosione delle linee del vapore in acciaio.
Reazione con carbonili
Per illustrare la condensazione dell'idrazina con un radicale carbonile, citiamo la reazione con l' acetone che porta alla formazione di diisopropilidene idrazina. Questo reagisce di nuovo con l'idrazina per formare un idrazone:
2 (CH 3 ) 2 CO+ N 2 H 4→ 2 H 2 O+ [(CH 3 ) 2 C = N] 2. [(CH 3 ) 2 C = N] 2+ N 2 H 4→ 2 (CH 3 ) 2 C = N - NH 2.Acetone e diisopropilidene idrazina sono intermedi nella sintesi di PCUK-Atofina. L' alchilazione indirizza le idrazine con alogenuri alchilici in presenza di una forma base dei derivati alchilati delle idrazine, ma la reazione è generalmente inefficace a causa dello scarso controllo sul grado di sostituzione (come per le ammine comuni). Ridurre l' idrazone in idrazina è un modo elegante per produrre idrazine 1,1 dialchilate.
In un'altra reazione, la 2-ciano piridina reagisce con l'idrazina per formare idrazidi ammidate che possono essere convertite in triazine usando 1,2-dichetoni.
Reazione di Wolff-Kishner
L'idrazina è utilizzata in chimica organica nella riduzione di Wolff-Kishner , una reazione che converte il gruppo carbonile di un chetone o aldeide in un ponte metilenico (o gruppo metilico ) tramite una molecola di idrazone . La produzione di diazoto molto stabile dall'idrazina favorisce la reazione.
Sintesi di molecole policicliche
Avendo due funzioni amminiche, l'idrazina è una parte fondamentale per la preparazione di molti composti eterociclici tramite condensazione con una parte avente due funzioni elettrofile . Con acetilacetone , si condensa per dare 3,5-dimetilpirazolo . Nella reazione di Einhorn-Brunner, le idrazine reagiscono con le immidi per dare triazoli .
Solfonazione
Essendo un buon nucleofilo, N 2 H 4 è vulnerabile all'attacco di alogenuri sulfonilici e alogenuri acilici. La tosil idrazina forma anche idrazoni dopo il trattamento con carbonili.
Ripartizione delle ftalimmidi
L'idrazina viene utilizzata per suddividere la N- ftalimmide in derivati alchilici. Questa reazione di scissione consente di utilizzare l'anione ftalimmide come precursore dell'ammina nella sintesi di Gabriel.
Agente riducente
L'idrazina è un popolare agente riducente perché i suoi sottoprodotti di decomposizione sono generalmente azoto gassoso e acqua. Pertanto, viene utilizzato come antiossidante , scavenger di ossigeno e inibitore della corrosione nell'acqua di caldaie e circuiti di riscaldamento (in questo ruolo, ora si preferisce N, N-dietilidrossilammina , di minore tossicità, ma è ancora ampiamente utilizzato contro la corrosione in grandi centrali termiche e nucleari in particolare). Viene anche utilizzato per ridurre i sali di metalli e ossidi metallici allo stato metallico nell'elettrolisi del nichel nonché nell'estrazione del plutonio dai combustibili nucleari esauriti .
Sali di idrazina
L'idrazina viene convertita in sali solidi mediante trattamento con acidi minerali. Il sale più comune è l'idrazina idrogenosolfato, N 2 H 5 HSO 4 , che dovrebbe probabilmente essere chiamato idrazina bisolfato. L'idrazina bisolfato è usata come trattamento alternativo per la cachessia indotta dal cancro. Il sale dell'idrazina e dell'acido azotidrico N 5 H 5 era di interesse scientifico a causa del suo alto contenuto di azoto e delle proprietà esplosive.
Usi industriali
L'idrazina è utilizzata in molti processi, ad esempio la produzione di fibre di spandex , come catalizzatore di polimerizzazione , agente espandente, per celle a combustibile , come il flusso di saldatura per saldatura , per lo sviluppo di fotografie, come la catena di estensione per la polimerizzazione del poliuretano , come un composto riducente per il condizionamento dell'acqua nelle centrali termiche e circuiti secondari nelle centrali nucleari e come stabilizzatore termico. Inoltre, è stata recentemente testata una tecnica che utilizza depositi di idrazina su semiconduttori, con possibile applicazione alla produzione di transistor a film sottile utilizzati per schermi a cristalli liquidi . L'idrazina in soluzione al 70% con il 30% di acqua viene utilizzata per alimentare l'EPU (unità di alimentazione di emergenza), sugli aerei da combattimento F-16 ( General Dynamics F-16 Fighting Falcon ).
Nell'uso militare, un derivato dell'idrazina, la dimetilidrazina asimmetrica (UDMH) , combinata con il nitrato di ammonio è l'ingrediente base dell'astrolite (in) , un esplosivo estremamente potente inventato negli anni '60.
Carburante per missili
L'idrazina fu usata per la prima volta come carburante per missili durante la seconda guerra mondiale per gli aerei Messerschmitt Me 163 (il primo aereo a razzo), sotto il nome di B-Stoff (infatti, idrazina idrata ). Questo B-Stoff è stato miscelato con metanolo ( M-Stoff ) per dare C-Stoff , che è stato utilizzato come combustibile con T-Stoff , un concentrato di perossido di idrogeno , utilizzato come ossidante a contatto con il quale si è acceso spontaneamente in un reazione molto energica.
Oggi l'idrazina viene generalmente utilizzata da sola come monopropellente nei motori a bassa spinta (ma ad alta precisione) permettendo il posizionamento in orbita di satelliti e sonde spaziali ; in questo caso la spinta è fornita dalla decomposizione catalitica dell'idrazina e non dalla combustione. Questa decomposizione è davvero una reazione molto esotermica . Si ottiene facendo passare l'idrazina su un catalizzatore il cui componente attivo è l' iridio metallico depositato su un'ampia superficie di allumina (ossido di alluminio), o nanofibre di carbonio, o più recentemente nitruro di molibdeno su allumina, o anche nitrato di molibdeno . La sua decomposizione in ammoniaca , azoto e idrogeno risulta dalle seguenti reazioni:
Questa decomposizione si attiva in pochi millisecondi e consente di misurare la spinta in modo molto preciso. Queste reazioni sono molto esotermiche (il catalizzatore nella camera può raggiungere gli 800 ° C in pochi millisecondi) e producono un grande volume di gas caldi da un piccolo volume di idrazina liquida, rendendolo un buon propellente per la propulsione spaziale .
Alcuni derivati dell'idrazina sono anche usati come propellenti liquidi: monometilidrazina H 2 N - NHCH 3(o MMH) e dimetilidrazina asimmetrica , H 2 N - N (CH 3 ) 2(o UDMH). Sono generalmente utilizzati con perossido di azoto N 2 O 4come ossidante, con il quale formano un propellente liquido ipergolico immagazzinabile .
Celle a combustibile
Il produttore italiano di catalizzatori Acta ha proposto di utilizzare l'idrazina come soluzione alternativa all'idrogeno nelle celle a combustibile . Il vantaggio principale di questo prodotto è la sua capacità di produrre oltre 200 mW / cm 2 , più di una simile cella a combustibile a idrogeno senza la necessità di costosi catalizzatori contenenti platino . Poiché il carburante è liquido a temperatura ambiente, può essere maneggiato e conservato più facilmente dell'idrogeno. Conservando l'idrazina in un serbatoio contenente un carbonile con un doppio legame carbonio- ossigeno , il carburante reagisce e forma un materiale solido e sicuro chiamato idrazone . Quindi basta riempire il serbatoio con acqua calda per rilasciare l' idrazina idrato in forma liquida. La manipolazione del carburante liquido è in pratica molto più sicura di quella dell'idrogeno gassoso, e il liquido ha un potenziale redox maggiore (1,56 V ) rispetto a 1,23 V dell'idrogeno. La molecola di idrazina viene rotta nella batteria per formare atomi di diazoto e idrogeno che si legano a un atomo di ossigeno per formare acqua.
sicurezza
Tossicità, ecotossicità
L'idrazina è altamente tossica e pericolosamente instabile, soprattutto nella sua forma anidra . Viene generalmente utilizzato come monoidrato stabile.
I sintomi di esposizione acuta ad alti livelli di idrazina possono manifestarsi nell'uomo come irritazione degli occhi , naso e gola , vertigini, mal di testa , nausea , edema polmonare , convulsioni , coma . L'esposizione acuta può anche danneggiare il fegato , i reni e il sistema nervoso centrale negli esseri umani. Il liquido è corrosivo e può produrre eczema da contatto nell'uomo e negli animali. Sono stati riportati effetti avversi a polmoni , fegato, milza e tiroide in animali esposti cronicamente all'idrazina per inalazione. Un aumento del numero di polmone, cavità nasale, fegato e tumori è stata osservata nei roditori esposti a idrazina.
La sua tossicità è soggetta a periodiche rivalutazioni, man mano che la conoscenza evolve.
Riferimenti
- IDRAZINA (anidro) , scheda di sicurezza (s) del Programma internazionale sulla sicurezza chimica , consultato il 9 maggio 2009
- (en) Yitzhak Marcus, The Properties of Solvents , vol. 4, Inghilterra, John Wiley & Sons Ltd,1999, 239 p. ( ISBN 0-471-98369-1 )
- massa molecolare calcolata dal " peso atomico degli elementi 2007 " su www.chem.qmul.ac.uk .
- (in) James E. Mark, Physical Properties of Polymer Handbook , Springer,2007, 2 ° ed. , 1076 p. ( ISBN 978-0-387-69002-5 e 0-387-69002-6 , leggi online ) , p. 294
- (en) Robert H. Perry e Donald W. verde , di Perry Chemical Engineers' Handbook , Stati Uniti d'America, McGraw-Hill,1997, 7 ° ed. , 2400 p. ( ISBN 0-07-049841-5 ) , p. 2-50
- Entry "idrazina" nel database chimica GESTIS dell'IFA (ente tedesco responsabile per la sicurezza sul lavoro e la salute) ( tedesco , inglese ), si accede 11 Febbraio 2010 (JavaScript necessario)
- " Properties of Various Gases " su flexwareinc.com (accesso 12 aprile 2010 )
- (en) "Hydrazine" , su NIST / WebBook , accesso 11 febbraio 2010
- (a) David R. Lide, CRC Handbook of Chemistry and Physics , CRC Press,2009, 90 ° ed. , 2804 p. , Rilegato ( ISBN 978-1-4200-9084-0 )
- (a) David R. Lide , CRC Handbook of Chemistry and Physics , Boca Raton, CRC Press,18 giugno 2002, 83 ° ed. , 2664 p. ( ISBN 0849304830 , presentazione online ) , p. 5-89
- (a) David R. Lide, Manuale di chimica e fisica , Boca Raton, CRC,2008, 89 ° ed. , 2736 p. ( ISBN 978-1-4200-6679-1 ) , p. 10-205
- Gruppo di lavoro IARC sulla valutazione dei rischi cancerogeni per gli esseri umani, " Valutazioni Globales de la Carcinogenicité pour l'Homme, Gruppo 2B: Possibilmente cancerogeno per l'uomo " , su http://monographs.iarc.fr , IARC,16 gennaio 2009(visitato il 22 agosto 2009 )
- Numero indice nella tabella 3.1 dell'appendice VI del regolamento CE n. 1272/2008 (16 dicembre 2008)
- SIGMA-ALDRICH
- " Hydrazine " nel database delle sostanze chimiche Reptox del CSST (organizzazione del Quebec responsabile per la sicurezza e la salute sul lavoro), accesso 24 aprile 2009
- " Hydrazine " , su hazmap.nlm.nih.gov (visitato il 14 novembre 2009 )
- "hydrazine" , su ESIS , accesso 17 febbraio 2009
- Miessler, Gary L. e Tarr, Donald A. Inorganic Chemistry, Third Edition . Pearson Prentice Hall (2004). ( ISBN 978-0-13-035471-6 ) .
- Chimica inorganica, DF Shriver, Peter William Atkins
- Fondamenti di chimica organica, Michael Hornby, Josephine Peach
- (in) Holleman, AF, Wiberg, E. "Inorganic Chemistry" Academic Press: San Diego, 2001. ( ISBN 978-0-12-352651-9 ) .
- Scheda di sicurezza INRS
- Curtius, Journal für praktische Chemie , 39, 1889, p. 107-39
- Adams, R.; Marrone, BK, solfato di idrazina, 1, 309, 1941, cv1p0309
- " Hydrazine: Chemical product info, chemindustry.ru, 2007-01-08 " ( Archive • Wikiwix • Archive.is • Google • Cosa fare? ) (Accesso 25 marzo 2013 )
- Riegel, Emil Raymond. "Hydrazine" Riegel's Handbook of Industrial Chemistry p. 192 (1992).
- (a) Brian Handwerk , " Bacteria Eat Human Sewage, Produce Rocket Fuel " , National Geographic Society ,9 novembre 2005( letto online , consultato il 12 novembre 2007 )
- National Geographic http://news.nationalgeographic.com/news/2005/11/1109_051109_rocketfuel.html
- [Giorno, CA; Whiting, MC; Acetone Hydrazone; vol 6 | pagina 10; cv6p0010;]
- [Wiley, RH; Hexner, PE; 3,5-dimetilpirazolo, volume 4, pagina 351; cv4p0351]
- [Friedman, L; Litle, RL; Reichle, WR; p -Toluensolfonil idrazide; vol 5; pagina 1055, cv5p1055]
- [Weinshenker, NM; Shen, CM; Wong, JY, carbodiimmide polimerica; vol 6, pagine 951; (1988); cv6p0951]
- 2013 La centrale nucleare versa sostanze chimiche nella baia di Fundy La centrale nucleare del New Brunswick segnala la perdita di sostanze chimiche nella Baia di Fundy (Canadian Press in Energy and Resources ) 3013-11-05, accesso 3013-11-06
- (it) R. Vieira , “ Nuovo nanofibre di carbonio / grafite feltro composito per l'uso come supporto di catalizzatore per la decomposizione catalitica idrazina ” , Chemical Communications , n o 9,2002, p. 954—955 ( DOI 10.1039 / b202032g )
- (it) Xiaowei Chen , “ catalitica di decomposizione di idrazina oltre supportati molibdeno nitruro di catalizzatori in un monopropellente propulsore ” , Catalysis Letters , vol. 79,Aprile 2002, p. 21-25 ( DOI 10.1023 / A: 1015343922044 )
- " Liquid asset - News - The Engineer - News: notizie di ingegneria, informazioni di ingegneria, tecnologia più recente, notizie di produzione, informazioni di produzione, notizie automobilistiche, notizie aerospaziali, notizie sui materiali, ricerca e sviluppo " ( Archive • Wikiwix • Archive.is • Google • Cosa fare? )
- ARC, Monograph, volume 71 (1999) Re-evaluation of Some Organic Chemicals, Hydrazine and Hydrogen Peroxide .
- Sylvie Tissot, Annick Pichard, " Soglie di tossicità acuta idrazina (NH 2 NH 2 ) - Rapporto finale " [PDF] , su ineris.fr , Istituto nazionale per l'ambiente industriale e i rischi ,agosto 2003(visitato il 29 ottobre 2015 ) .
Articoli Correlati
link esterno
- Il Late Show con Rob! Ospite speciale di stasera: Hydrazine (PDF) - Robert Matunas
- xMSDS-Hydrazine-9924279 (PDF) - Scheda di sicurezza per l'idrazina
- (fr) Scheda tossicologica INRS
- (en) Scheda di dati di sicurezza internazionale








