Leucemia mieloide acuta
Leucemia mieloide acuta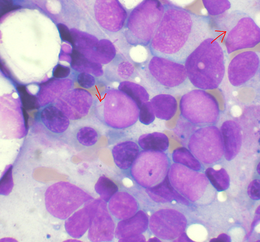 Leucemia mieloide acuta, le frecce indicano i bastoncini di Auer.
Leucemia mieloide acuta, le frecce indicano i bastoncini di Auer.
| Specialità | Oncologia ed ematologia |
|---|
| ICD - 10 | C92.0 |
|---|---|
| CIM - 9 | 205.0 |
| ICD-O | M 9861/3 |
| OMIM | 601626 |
| MalattieDB | 203 |
| MedlinePlus | 000542 |
| eMedicina | 197802 |
| eMedicina | medio / 34 |
| Maglia | D015470 |
| Sintomi | infezioni, sanguinamento |
| complicazioni | reazione del trapianto contro l'ospite (GvH) |
| cause | radiazioni, benzene |
| Diagnostico | emocromo, mielogramma, citogenetica |
| Trattamento | chemioterapia antitumorale, terapia mirata, trapianto allogenico di midollo osseo |
| Farmaco | Idarubicina , mitoxantrone , etoposide , ciclofosfamide , daunorubicina , tioguanina idrato ( d ) , gemtuzumab ozogamicin , dasatinib monoidrato ( d ) , énasidénib , vénétoclax , doxorubicina , idrossiurea , citarabina , everolimus , azacitidina , metotrexato , deferasirox , tretinoina , nivolumab , clofarabina , decitabine , midostaurina , busulfan , sorafenib , ruxolitinib e 6-tioguanina |
| paziente del Regno Unito | Acuta-mieloide-leucemia-pro |
La leucemia mieloide acuta (LMA), nota anche come leucemia acuta mieloide, è una neoplasia ematologica di tipo canceroso che colpisce le cellule ematopoietiche del midollo osseo . Le cellule leucemiche, chiamate blasti , sono caratterizzate da un'incapacità di differenziarsi in cellule mature e da una proliferazione incontrollata. Questa disfunzione del midollo osseo impedisce la normale produzione di cellule del sangue e provoca varie sindromi cliniche, a volte molto gravi ( infezione , emorragia , ecc.). L'AML si manifesta classicamente negli adulti sopra i 40 anni, in particolare negli anziani, anche se sono identificati anche tra i tumori pediatrici . La gestione è fornita da ematologi , principalmente negli ospedali . La diagnosi utilizza la biologia molecolare per identificare, in particolare , mutazioni genetiche , che consente di determinare il sottotipo di LMA. Questi elementi diagnostici vengono poi presi in considerazione per stabilire la prognosi della malattia insieme ad altri elementi come l'età o la risposta al trattamento. La combinazione di chemioterapia intensiva e trapianto di midollo osseo allogenico determina remissioni complete e durature o addirittura guarigioni in circa il 20-40% dei pazienti.
Campo di interesse per la ricerca medica , sono stati compiuti progressi significativi negli anni 2000 e 2010 . L'avvento di nuove tecniche ad alte prestazioni in ematologia cellulare, biologia molecolare e citogenetica ha fornito l'accesso a una migliore comprensione dei meccanismi coinvolti nello sviluppo dell'AML. L'identificazione di nuovi bersagli terapeutici consente di offrire terapie mirate in alternativa alla chemioterapia citotossica. Pertanto, per un particolare sottotipo, la leucemia promielocitica acuta , la chemioterapia convenzionale tende a non essere più offerta come prima linea di trattamento.
Epidemiologia
Impatto
La LMA può manifestarsi a qualsiasi età, ma colpisce soprattutto gli adulti dopo i 50 anni. Durante il decennio 2010, l'età media della diagnosi era compresa tra 64 e 72 anni a seconda del paese e dell'anno.
| Epidemiologia dell'AML | ||||
| Ambientazione | Francia | Europa | stati Uniti | |
|---|---|---|---|---|
| Prevalenza (per 100.000 abitanti ) | 11 | |||
| Incidenza (per 100.000 ab. ) | 2,3 (V) / 3,1 (M) (2018) | 2 - 3 | 3,5 (F) - 5,2 (M) (2012-2016) | |
| Rapporto tra i sessi (M/F) | 1.3 | 1.2 | 1.5 | |
| Percentuale di emopatie | 7,6% | |||
| Percentuale di tumori | 0,9% | 1,2% | ||
La popolazione pediatrica (0-19 anni) è poco colpita da LMA: l'incidenza è bassa con, nel 2017, un'incidenza dello 0,9%. Questi pazienti sono maggiormente colpiti da un altro sottotipo di leucemia: la leucemia linfoblastica acuta che rappresenta circa l'80% dei casi di leucemia infantile contro il 20% di LMA.
Mortalità
Il tasso di mortalità standardizzato per età associato alla LMA è stimato a 1,3 per 100.000 persone nel 2017 dal Global Burden of Disease . Per la popolazione pediatrica (da 0 a 19 anni) è inferiore a 0,4 per 100.000 persone.
Patogenesi, cause, fattori di rischio
patogenesi
Le neoplasie ematologiche , compresa la parte AML, possono essere ampiamente caratterizzate da due attributi: la maturazione e la proliferazione . Nella LMA queste due caratteristiche sono alterate: i blasti hanno perso la capacità di differenziarsi in cellule ematiche mature ( cellule polimorfonucleate , monociti , piastrine , globuli rossi ) e la divisione cellulare avviene senza controllo con eccessiva proliferazione. Questa difettosa maturazione e proliferazione è legata ad un difetto del ciclo cellulare: generalmente alcuni geni responsabili del controllo di queste funzioni hanno subito mutazioni che interrompono il controllo fisiologico della divisione cellulare. L'identificazione di queste alterazioni serve come base per la diagnosi, la classificazione e il trattamento della LMA.
cause
I tumori e le leucemie non hanno un'unica causa nota, ma il loro sviluppo è comunque associato a determinati fattori ambientali e/o anomalie genetiche. L' Agenzia internazionale per la ricerca sul cancro , un'agenzia dell'OMS , è responsabile in particolare della valutazione e della classificazione degli agenti fisici, chimici e biologici in base al loro effetto cancerogeno . Alcuni di loro favoriscono in particolare la comparsa della leucemia inclusa la LMA. Nel complesso, qualsiasi esposizione che può alterare, modificare o denaturare il DNA delle cellule è un potenziale fattore di rischio. Tuttavia, sono necessari dati epidemiologici e studi sugli effetti cellulari per valutare, con un ragionevole grado di confidenza, il rischio presentato da tale esposizione.
Radiazione ionizzanteLe radiazioni ionizzanti sono particelle energetiche sufficienti a rompere i legami chimici tra gli atomi e quindi ad alterare le molecole . La scoperta della radioattività e il suo uso crescente nel XX ° secolo furono rapidamente mostrano i rischi di esposizione alle radiazioni per la salute. Lo sviluppo della radiobiologia ha successivamente permesso di stabilire che le radiazioni provocano anomalie nel DNA, e aumentano il rischio di sviluppare il cancro e in particolare la leucemia. Marie Curie e Irène Joliot-Curie morirono quindi di leucemia probabilmente indotta da radiazioni a causa del loro lavoro sulla radioattività .
Lo studio INWORKS, pubblicato su Lancet Hematology nel 2015, che ha coinvolto una coorte di poco più di 300.000 lavoratori nucleari in 3 paesi, ha concluso che il rischio di leucemia è aumentato anche a bassa esposizione.
Agenti chimiciGli agenti chimici, compresi i farmaci e in particolare le chemioterapie citotossiche, sono identificati come responsabili della leucemia.
L'esposizione al benzene è una causa nota dello sviluppo della LMA; è stato quindi classificato dal 1979 come cancerogeno di gruppo 1 dalla IARC (cancerogeno provato).
Il glifosato è classificato come probabilmente cancerogeno per l'uomo (Gruppo 2A) ma non è stato riscontrato in relazione ad AML con un alto livello di evidenza ; sebbene i dati siano limitati, rimane sospetto un collegamento.
Farmaci identificati come leucemogeni:
- le antracicline ( doxorubicina , daunorubicina , ecc. ) e affini ( mitoxantrone ) sono farmaci antitumorali noti per essere leucemogeni;
- gli agenti alchilanti ( busulfan , ecc. );
- antimetaboliti (citarabina);
- epidofilotossine: etoposide .
- Agente chimico leucemogeno
-
Benzene
-
doxorubicina
-
Etoposide
L'insorgenza della leucemia mieloide acuta può seguire la trasformazione (o l' acutizzazione ) di un'altra malattia del sangue come la sindrome mielodisplastica o la sindrome mieloproliferativa (leucemia mieloide cronica, ecc .). Varie malattie congenite costituiscono un fattore di rischio ( trisomia 21 , sindrome di Klinefelter , anemia di Fanconi , ecc .).
Una storia di infezione con determinati virus o batteri non sembra essere correlata a un aumento del rischio di LMA.
Segni clinici
Quando i blasti proliferano eccessivamente invadono il midollo osseo e/o altri organi del corpo umano e ne interrompono la funzione, provocando la comparsa dei segni clinici. Tuttavia, la presentazione clinica generalmente non è molto specifica e la diagnosi non può essere fatta sulla base dei soli sintomi.
Insufficienza del midollo osseo
L'invasione del midollo osseo da parte delle cellule leucemiche interromperà l' emopoiesi, vale a dire il processo fisiologico di creazione di nuove cellule del sangue. Nel midollo vengono solitamente prodotti tre tipi di cellule (o lignaggi): globuli rossi ( eritrociti ), globuli bianchi (soprattutto neutrofili polimorfonucleati ) e piastrine (trombociti). La disfunzione del midollo osseo può variare dalla citopenia (una singola linea cellulare interessata) all'anemia aplastica (completa carenza di cellule del sangue da tutte e tre le linee). I sintomi associati dipendono dal tipo di citopenia. La citopenia può essere diagnosticata prima della manifestazione dei sintomi clinici o su una valutazione di laboratorio di routine in un individuo asintomatico.
Malattia della linea di sangue rossaUn deficit quantitativo nei globuli rossi è dimostrato dalla concentrazione totale di emoglobina nel sangue e viene chiamato anemia . La tolleranza del paziente all'anemia è generalmente legata alla velocità di insorgenza: in caso di impianto a bassa rumorosità, l'organismo si adatta tramite sistemi di compensazione, i sintomi possono essere assenti. Una rapida insorgenza sarà invece accompagnata da una ripercussione clinica con in particolare dispnea , astenia , pallore.
Malattia della linea biancaIl problema principale è la diminuzione dei neutrofili polinucleati (PNN): queste cellule appartengono al sistema immunitario innato e costituiscono la prima linea di difesa contro le infezioni, principalmente batteriche e fungine . A seconda dell'entità del deficit, si parlerà di neutropenia o agranulocitosi . Il soggetto neutropenico è estremamente vulnerabile alle infezioni . La comparsa della febbre in questo contesto è chiamata neutropenia febbrile , e costituisce un'emergenza terapeutica che il più delle volte richiede un trattamento in ambiente ospedaliero con la somministrazione di un antibiotico .
Si può parlare di leucemia "iperleucocitica" (cioè con eccesso di globuli bianchi) osservando la neutropenia: un'alta percentuale di leucociti corrisponde infatti a blasti circolanti nel sangue con, allo stesso tempo, una diminuzione del numero cellule polinucleate normali.
Coinvolgimento della linea piastrinicaUna diminuzione del numero di piastrine nel sangue la espone al rischio di emorragie gravi o spontanee. Clinicamente, i segni cutanei come porpora , petecchie o lividi possono riflettere un'emostasi inefficace.
Disturbi significativi della coagulazione si osservano in particolare durante la fase iniziale della leucemia promielocitica acuta . Il consumo di piastrine e fattori della coagulazione causato dalla coagulazione intravascolare disseminata può peggiorare la trombocitopenia.
Sindrome tumorale
La sindrome tumorale è legata alla diffusione di blasti al di fuori del midollo osseo e all'accumulo negli organi. Può risultare clinicamente da:
- un aumento del volume di alcuni organi : splenomegalia , epatomegalia ;
- dolori articolari;
- danni alla pelle (sudorazione notturna);
- danno della mucosa compresa l'ipertrofia gengivale (aumento del volume gengivale);
- danno neuromeningeo quando il sistema nervoso centrale è invaso , che può essere accompagnato da segni neurologici.
Quando la massa tumorale (cioè il numero di blasti) è molto grande, può iniziare la sindrome da lisi tumorale . È legato alla distruzione di esplosioni, sia spontanee che legate al trattamento. Il contenuto intracellulare viene quindi rilasciato nel sangue che provoca disturbi nelle concentrazioni ematiche di ioni (potassio, fosfato), visibili sullo ionogramma. Questo può portare a iperkaliemia , che è dannosa per il battito cardiaco o ad un aumento dell'acido urico (iperuricemia) che può portare a danni ai reni attraverso la formazione di cristalli di urato. La gestione della sindrome da lisi mira a ripristinare uno ionogramma normale mediante idratazione e somministrazione di elettroliti; l'iperuricemia può essere trattata con rasburicase , un enzima che scompone l'acido urico.
La sindrome della leucostasi si osserva in caso di massiccia infiltrazione degli organi da parte delle cellule leucemiche. Si manifesta con un'elevata concentrazione di blasti nel sangue (blastosi), febbre e sintomi respiratori e/o neurologici. Questa sindrome è un'emergenza terapeutica, il cui esito può essere fatale a causa di distress respiratorio .
Diagnostico
L'esame clinico del paziente consente soprattutto di rilevare segni di emopatia maligna. La diagnosi si basa essenzialmente su una valutazione biologica estesa che comprende: emocromo ( CBC ), mielogramma o biopsia del midollo osseo , immunofenotipizzazione , cariotipo , citogenetica e sequenziamento genico .
L'esame del midollo osseo definisce l'aspetto morfologico delle cellule ed è il primo passo per guidare la diagnosi. La diagnosi di leucemia acuta viene fatta in presenza di più del 20% di cellule immature, i blasti. L'esame dell'espressione di vari recettori ( DC ) mediante immunofenotipizzazione consente di classificare lo stadio e il ceppo di appartenenza delle cellule.
Il cariotipo e lo studio del genoma consentono l'identificazione di anomalie cromosomiche (delezioni, inversioni, traslocazioni); Il 50-60% delle LMA presenta anomalie del cariotipo. Si cercano anche mutazioni genetiche . Queste analisi sono decisive per valutare la prognosi e le opzioni terapeutiche.
Prima dello sviluppo della fenotipizzazione e delle tecniche citogenetiche, la diagnosi di LMA si basava principalmente sulla morfologia cellulare ed era guidata dalla classificazione franco-americana-britannica (FAB). Nuove tecniche di studio del DNA hanno permesso di costituire la nuova classificazione dell'OMS che ha sostituito la FAB: la sua categorizzazione è più fine e si basa su anomalie cromosomiche e/o genetiche.
Oltre alle classificazioni, possiamo distinguere anche 3 tipi di AML:
- de novo AML ;
- LMA secondaria a sindrome mielodisplastica o sindrome mieloproliferativa ;
- LMA indotta da citotossici e/o radiazioni.
Classificazione
A causa delle cellule colpite e delle mutazioni coinvolte, le leucemie mieloidi acute sono un insieme disparato che è stato oggetto di categorizzazione. Il FAB (franco-americano-britannico) è il più antico ed è stato sostituito dalla classificazione dell'OMS pubblicata nel 2008. Sebbene il FAB sia obsoleto, è ancora usuale soddisfare i relativi termini diagnostici (LAM0, LAM3, ecc .).
Organizzazione mondiale della SanitàLa classificazione OMS dell'AML è quella attualmente utilizzata per la diagnostica. Pubblicato originariamente nel 2008, è stato aggiornato nel 2016 e pubblicato su Blood (rivista di ematologia di riferimento).
| Classificazione WHO 2016 della leucemia mieloide acuta e delle neoplasie correlate | ||
| Nome | Descrizione | ICD-O |
|---|---|---|
| LMA con anomalie citogenetiche ricorrenti |
|
multiplo |
| LMA con anomalie associate a mielodisplasie | Include le AML associate a MDS prive delle suddette anomalie molecolari; sono generalmente associati a una prognosi sfavorevole.
|
M 9895/3 |
| LMA post-trattamento | Gruppo che comprende le leucemie che si verificano dopo la chemioterapia o l'esposizione alle radiazioni. | M 9920/3 |
| LAM, senza ulteriori indicazioni | Gruppo che include sottotipi che non rientrano in altre categorie.
|
|
| Sarcoma mieloide | ||
| Proliferazione mieloide associata a trisomia 21 |
|
M 9861/3 |
| Leucemia plasmocitoide derivata dalle cellule dendritiche | Precedentemente noto come leucemia/linfoma a cellule NK
Chiamato anche: Blast Plasmacytoid Blast Cell Neoplasma (NCDPB) |
|
| Leucemie acute di lignaggio ambiguo | ||
La classificazione FAB (franco-americana-britannica, 1976) è la vecchia classificazione, ormai abbandonata. Si basa sulla morfologia e sulla quantità di cellule osservate sul mielogramma.
| Classificazione FAB di AML | ||
| LAM | Descrizione | Proporzione |
|---|---|---|
| LAM 0 | indifferenziato | 5% dei casi |
| LAM 1 | mieloblastica senza differenziazione | 15% dei casi |
| LAM 2 | mieloblastica con differenziazione | 25% dei casi |
| LAM 3 | promielocitica | 10% dei casi |
| LAM 4 | mielomonocitico | 20% dei casi |
| LAM 4Eo | mielomonocitica con eosinofilia | 5% dei casi |
| LAM 5 | monoblastico (senza differenziazione: M5a, con differenziazione: M5b) | 10% dei casi |
| LAM 6 | eritroblastica o eritroleucemia | 5% dei casi |
| LAM 7 | megacarioblastico | 5% dei casi |
Questa classificazione non ha alcun impatto in termini di prognosi o trattamento da attuare, a differenza di un'analisi incentrata sullo studio dei geni mutati.
Trattamento
Il trattamento curativo della leucemia mieloide acuta è la chemioterapia intensivamente associata alle cellule staminali ematopoietiche allogeniche (ad eccezione della leucemia acuta (" LA ") promielocitica). La gestione dipende da molti elementi legati sia al paziente che alla leucemia. L'età, le condizioni generali , le comorbilità e la volontà del paziente sono in particolare i fattori predominanti. Il tipo di leucemia acuta, le diverse mutazioni rilevate e le risposte cliniche ai trattamenti precedenti determinano le opzioni di trattamento durante la gestione. Le decisioni terapeutiche vengono prese al termine delle riunioni di consultazione multidisciplinare (RCP).
Il trattamento classico è una successione di cicli chemioterapici in più fasi: induzione, consolidamento poi, se il paziente è idoneo, intensificazione della terapia con trapianto allogenico di midollo osseo. La radiazione non è un trattamento standard per l'AML poiché non esiste un'unica sede della malattia come un tumore solido. Tuttavia, è usato per prevenire o curare la malattia neuro-meningea, cioè quando le cellule leucemiche si trovano nel sistema nervoso centrale ( cervello , midollo spinale ). Altre situazioni particolari possono richiedere il ricorso alla radioterapia (localizzazione testicolare , sarcoma mieloide ).
Il trattamento della leucemia promielocitica acuta (LPA) è un caso speciale: il ruolo della chemioterapia citotossica classica è meno importante poiché lo sviluppo dell'associazione di acido all trans retinoico ( ATRA ) e triossido di arsenico per raggiungere tassi di remissione superiori al 90% .
La gestione della leucemia e del cancro è associata a molte cure di supporto essenziali: prevenzione e gestione degli effetti avversi della chemioterapia, supporto trasfusionale per alleviare le citopenie , monitoraggio nutrizionale , screening per i sintomi depressivi , trattamento del dolore e avvio di cure palliative appropriate se necessario.
Induzione
L'induzione mira a indurre clinicamente e biologicamente la remissione completa ( CR ) con la chemioterapia. Il protocollo 3+7 , a base di citarabina e antraciclina ( daunorubicina o idarubicina ), è convenzionalmente prescritto; questo trattamento provoca nel paziente una profonda anemia aplastica della durata di tre-quattro settimane, durante le quali quest'ultima deve essere attentamente monitorata in un servizio di ematologia specializzato al fine di prevenire il rischio di emorragie e infezioni.
In alternativa all'induzione classica, possono essere utilizzate altre molecole come la decitabina .
Consolidamento
L'ulteriore trattamento dipende in larga misura dalla prognosi della LMA, dalla risposta alla chemioterapia di induzione (raggiungimento della remissione completa), dal paziente (età, comorbidità, ecc. ) e dai suoi desideri di trattamento. I trattamenti di consolidamento mirano ad eliminare le cellule leucemiche residue e quindi a prevenire le recidive. Il trapianto allogenico di midollo osseo è il trattamento preferenziale che consente di ottenere il più alto tasso di remissione duratura, ma a scapito di una gestione piuttosto pesante.
Se il trapianto allogenico viene rifiutato o inappropriato, la chemioterapia standard può essere continuata, ad esempio con citarabina ad alte dosi, azacitidina o clofarabina . Le altre opzioni di trattamento sono terapie mirate. Il midollo osseo autologo è molto raro.
alloinnesto
Il trapianto allogenico di midollo osseo è l'unico trattamento curativo per la LMA. L'obiettivo è quello di distruggere il midollo osseo patologico del paziente e quindi di ricostituire da esso un nuovo midollo utilizzando cellule staminali ematopoietiche raccolte da un individuo sano . La gestione terapeutica è complessa e richiede un adeguato ematologia che offre camere protette e di altre strutture ospedaliere ( unità di terapia cellulare , unità di preparazione la chemioterapia , ecc ).
L'idoneità al trapianto viene valutata collegialmente e decisa in accordo con il paziente . I trattamenti necessari per il trapianto hanno una certa tossicità e inducono un lungo periodo di aplasia e immunosoppressione con un alto rischio di complicanze e infezioni. Il trapianto allogenico è quindi generalmente riservato a soggetti “giovani” (sotto i 60 anni di età) e/o in ottime condizioni generali che potranno sostenere tale trattamento e trarre beneficio a lungo termine dal trapianto.
Possiamo distinguere approssimativamente 3 fasi. In primo luogo, il condizionamento del paziente consiste nell'irradiazione corporea completa , nella somministrazione di immunosoppressori e nella chemioterapia intensiva. Mira all'eradicazione delle cellule leucemiche e all'induzione di una significativa immunosoppressione che consenta di ridurre il più possibile il rigetto del trapianto . Le cellule staminali eterologhe vengono quindi reiniettate. La prosecuzione della gestione consiste nel gestire l' anemia aplastica prolungata indotta dal condizionamento nonché le possibili complicanze ed effetti indesiderati. A medio termine, l'ematologo controlla la salute dell'innesto e controlla l'effettiva scomparsa delle cellule leucemiche.
A livello immunologico, l'introduzione nell'organismo di cellule estranee al paziente (dette “ non-sé ”) può innescare una reazione immunitaria diretta contro le cellule del paziente o contro la leucemia: questi effetti sono rispettivamente denominati “ graft vs. host ”(GvH) e“ innesto vs. leucemia ”(GvL). Il primo è un effetto indesiderato più o meno grave che può manifestarsi in varie sedi (digestivo, cutaneo, ecc. ) e corrisponde ad un attacco agli organi dell'ospite da parte delle cellule trapiantate; può essere acuto o cronico. L'effetto GvL è invece benefico poiché le cellule immunitarie dell'innesto attaccheranno le cellule leucemiche e quindi eserciteranno un effetto antitumorale. Oltre alla GvHD, le complicanze del trapianto allogenico includono: infezioni correlate a immunosoppressione e aplasia, aumento del rischio di tumori secondari, citopenie di lunga durata che richiedono trasfusioni, malattia veno-occlusiva epatica e altri effetti avversi della chemioterapia.
Per i pazienti fragili o anziani che non possono sopportare un allotrapianto standard, esistono protocolli cosiddetti a “intensità ridotta” dove la fase di condizionamento (chemioterapia e radioterapia) prevede dosi ridotte: questa soluzione è un compromesso per preservare il beneficio del trapianto allogenico pur tenendo in conto della minore tolleranza del paziente.
Nel 2016, in Francia, sono stati eseguiti poco più di 700 allotrapianti per il trattamento della LMA. Nel 201, la Società europea per i trapianti di sangue e midollo (EBMT) ha identificato 6943 allotrapianti e 293 autotrapianti con leucemia mieloide acuta per indicazione.
Terapie mirate
Durante la diagnosi, il sequenziamento del genoma delle cellule leucemiche permette di identificare eventuali mutazioni presenti. Alcuni di essi partecipano alla proliferazione e alla mancata maturazione dei blasti: possono, ad esempio, portare alla sintesi di una proteina anormale che attiverebbe in modo permanente il ciclo cellulare , portando così ad una divisione incontrollata delle cellule. Arrestare l'azione dannosa di geni mutati o proteine alterate costituisce dunque un potenziale bersaglio terapeutico: così sono stati sviluppati in oncologia alcuni farmaci che agiscono specificamente su queste anomalie . Sono raggruppate sotto il nome di terapie mirate in opposizione alla classica chemioterapia citotossica; questa designazione comprende anche altri farmaci con differenti meccanismi d'azione, ad esempio anticorpi monoclonali diretti a recettori sulla superficie delle cellule ( cluster di differenziazione ).
Nel 2016, una revisione della letteratura ha stimato che dal 50% all'80% dei casi di LMA presenta mutazioni deleterie. Tra i geni più spesso interessati si può citare FLT3 o NPM1 (le mutazioni possono essere concomitanti). Nell'ambito della cura di un paziente, la conoscenza dei geni mutati consente non solo di classificare la leucemia, di stabilire una prognosi ma anche di prevedere quali terapie mirate possono essere prescritte a questo paziente. Sebbene non esista ancora una molecola per contrastare ogni gene, alcuni sono stati sviluppati durante il decennio del 2010 e talvolta hanno ricevuto l' approvazione dalle autorità sanitarie. Ad esempio, è stato identificato che mutazioni dell'isocitrato deidrogenasi (IDH), un enzima coinvolto nel metabolismo energetico cellulare , possono favorire la proliferazione delle cellule leucemiche. Pertanto, sono stati sviluppati inibitori dell'HDI: enasidenib (mirato a IDH2 ) e ivosidenib (mirato a IDH1 ). Varie altre terapie mirate possono essere prescritte o oggetto di ricerca clinica come glasdegib , venetoclax , ecc.
| Bersaglio | genere | Esempio di terapia mirata |
|---|---|---|
| FLT3 | Proteina | Midostaurina , gilteritinib (en) quizartinib (en) |
| HDI | Proteina | Ivosidenib (IDH1), enasidenib (IDH2) |
| Bcl-2 | Proteina | Venetoclax |
| CD33 | Recettore di membrana | Gemtuzumab ozogamicin |
Anche l'uso degli ormoni androgeni - che non sono terapie mirate propriamente parlando, ma rientrano piuttosto nella terapia ormonale - è stato studiato anche nella ricerca clinica. In particolare, il noretandrolone sembra migliorare la sopravvivenza e la remissione nei pazienti anziani.
Infine, alcune chemioterapie, pur avendo un classico meccanismo di interferenza con la sintesi del DNA, possono anche avere proprietà mirate aggiuntive. L'azacitidina ha, ad esempio, un'azione ipometilante: può indurre la rimozione dei gruppi chimici metilici (-CH 3 )filamenti di DNA e quindi consentire la riespressione di alcuni geni che controllano la divisione cellulare della cellula.
Altre situazioni
Le forme ricorrenti o refrattarie di LMA sono trattate con protocolli specifici, generalmente con chemioterapia (trattamento di salvataggio o di salvataggio).
Per quanto riguarda l' immunoterapia , gemtuzumab ozogamicin è l'unico anticorpo monoclonale approvato per il trattamento della LMA. Gli inibitori dell'immunocheckpoint (come l' ipilimumab , il nivolumab ) o le cellule T CAR (linfociti geneticamente modificati) non sono, nel 2020, indicati nel trattamento della LMA ma sono oggetto di studio per la ricerca clinica.
Sopravvivenza
La prognosi è generalmente espressa dalla sopravvivenza globale a 5 anni, cioè dalla proporzione di pazienti ancora in vita a 5 anni dalla diagnosi, tenendo conto di tutte le cause di morte combinate (se legate alla LAM, alle sue conseguenze, ad un'altra evento non correlato come un incidente stradale). In oncologia si possono utilizzare altri mezzi per stimare la prognosi durante il trattamento o negli studi clinici : si può parlare in termini di sopravvivenza libera da recidive, sopravvivenza libera da progressione o risposta al trattamento (risposta completa, parziale, ecc.).
Negli adulti la sopravvivenza a 5 anni è stimata intorno al 25% e diminuisce con l'età: è del 40% prima dei 65 anni e poi del 5% dopo. In pediatria , la probabilità di sopravvivenza globale a 5 anni è aumentata dal 50% negli anni '90 a circa il 60-70% nel 2010 (nella leucemia linfoblastica acuta ha raggiunto il 90% nel 2010). Anche in questo caso, le possibilità di sopravvivenza dei bambini piccoli sono leggermente superiori a quelle degli adolescenti.
Queste cifre non sono applicabili per la leucemia promielocitica acuta (ex-LMA 3). Associati in precedenza a una prognosi cupa, i nuovi trattamenti (combinazione ATRA / ATO ) a partire dagli anni 2000 hanno permesso di ottenere remissioni a lungo termine nel 90% dei pazienti.
Storia
La prima descrizione nella letteratura medica di un caso di leucemia risale al 1827. Alfred Velpeau descrisse il caso di un fiorista di 63 anni affetto da una malattia con febbre, stanchezza, calcoli renali e un grosso ingrossamento del fegato e della milza . Osservò che il sangue del paziente aveva una consistenza di farina d' avena e ipotizzò che questo aspetto potesse essere causato da particelle bianche. Nel 1845, il patologo JH Bennett riferì una serie di casi di pazienti che morirono con milza dilatata e "cambiamenti nel colore della consistenza del sangue"; usa quindi il termine "leucocitemia" per descrivere questa condizione.
La parola "leucemia" fu usata per la prima volta da Rudolf Virchow , un patologo tedesco, nel 1856. Descrisse, usando un microscopio, un eccesso di globuli bianchi in individui che mostravano i sintomi descritti da Velpeau e Benett. Virchow non conoscendo l'origine di questa anomalia, la chiamò con un termine puramente descrittivo leucemia (in greco: sangue bianco ).
Note e riferimenti
Appunti
(fr) Questo articolo è parzialmente o interamente tratto dall'articolo di Wikipedia in inglese intitolato " Acute myeloid leukemia " ( vedere l'elenco degli autori ) .- anglicismo da acuto , "acuto", intendendo il passaggio da una malattia cronica ad uno stadio acuto; il verbo associato è "acutiser".
Riferimenti
- Grand Dictionnaire Terminologique , Office québécois de la langue française, " leucemia acuta " ,2019(consultato il 28 dicembre 2019 )
- MSD , Ashkan Emadi, Jennie York Law, “ Leucemia mieloide acuta (AML) - Ematologia e oncologia - Edizione professionale del manuale MSD ” ,dicembre 2018(consultato il 29 dicembre 2019 )
- (it) National Cancer Institute , " Adult Acute Myeloid Leukemia Treatment (PDQ®) -Health Professional Version " ,8 febbraio 2019(consultato il 28 dicembre 2019 )
- Institut National Du Cancer, “ Sommario - Stime nazionali dell'incidenza e della mortalità del cancro nella Francia continentale tra il 1990 e il 2018 - Rif: SYNINCNAT2019 ” , su www.e-cancer.fr ,luglio 2019(consultato l'8 settembre 2019 )
- INSERM, " Orphanet: Leucemia mieloide acuta " , su orpha.net ,giugno 2014(consultato l'8 settembre 2019 )
- (in) D. Weber, E. Fromm, S. Erhardt, Mr. Lübbert W. Fiedler, T. Kindler, J. Krauter, P. Brossart, A. Kündgen, HR Salih J. Westermann, G. Wulf, B Hertenstein, M. Wattad, K. Götze, D. Kraemer, T. Heinicke, M. Girschikofsky, HG Derigs, HA Horst, C. Rudolph, M. Heuser, G. Göhring, V. Teleanu, L. Bullinger, F Thol, VI Gaidzik, P. Paschka, K. Döhner, A. Ganser, Hartmut Döhner, RF Schlenk, German-Austrian AML Study Group (AMLSG) Gabriele Nagel , “ Caratterizzazione epidemiologica, genetica e clinica per età di pazienti acuti di nuova diagnosi leucemia mieloide basata su uno studio di registro accademico basato sulla popolazione (AMLSG BiO) ” , Annals of Hematology , vol. 96, n . 12,31 ottobre 2017, pag. 1993 ( DOI 10.1007 / s00277-017-3150-3 , / pmc / articoli / PMC5691091 /? Report = abstract, leggi online )
- SEER, " Acute Myeloid Leukemia - Cancer Stat Facts " , su seer.cancer.gov (consultato l'8 settembre 2019 )
- Visser O, et al., “ Incidenza, sopravvivenza e prevalenza delle neoplasie mieloidi in Europa. » , Su www.ncbi.nlm.nih.gov ,novembre 2012(consultato l'8 settembre 2019 )
- Global Burden of Disease Study , “ Il carico globale del cancro dell'infanzia e dell'adolescenza nel 2017: un'analisi del Global Burden of Disease Study 2017 ” , su www.thelancet.com ,29 luglio 2019(consultato il 14 settembre 2019 )
- Smith MA, Ries LA, Gurney JG, et al., " Incidenza e sopravvivenza del cancro tra bambini e adolescenti: Programma SEER degli Stati Uniti 1975-1995 " , su seer.cancer.gov ,31 gennaio 2019(consultato il 15 settembre 2019 )
- Global Burden of Disease Study, “ globale, regionale, e la mortalità età-sesso-specifico nazionale per 282 cause di morte in 195 paesi e territori, 1980-2017: un'analisi sistematica per il Global Burden of Disease Study 2017 ” , a www .thelancet.com ,10 novembre 2018(consultato il 14 settembre 2019 )
- VJ Cogliano , R. Baan , K. Straif , Y. Grosse , B. Lauby-Secretan , F. El Ghissassi , V. Bouvard , L. Benbrahim-Tallaa , N. Guha , C. Freeman , L. Galichet e CP Wild , " Esposizioni prevenibili associate ai tumori umani " , JNCI Journal of the National Cancer Institute , vol. 103, n . 24,2011, pag. 1827–1839 ( ISSN 0027-8874 , DOI 10.1093/jnci / djr483 )
- " Classificazione IARC per siti di cancro | Cancro e ambiente ” (consultato il 24 novembre 2019 )
- Musée Curie , “ Biografia di Marie Curie ” (consultato il 24 novembre 2019 )
- Musée Curie , “ Biografia di Irene e Frédéric Joliot-Curie ” (consultato il 24 novembre 2019 )
- Klervi Leuraud , David B Richardson , Elisabeth Cardis , Robert D Daniels , Michael Gillies , Jacqueline A O'Hagan , Ghassan B Hamra , Richard Haylock , Dominique Laurier , Monika Moissonnier , Mary K Schubauer-Berigan , Isabelle Thierry-Chef e Ausrele Kesminiene , " Radiazioni ionizzanti e rischio di morte per leucemia e linfoma nei lavoratori sottoposti a monitoraggio delle radiazioni (INWORKS): uno studio di coorte internazionale ", The Lancet Hematology , vol. 2, n . 7,2015, e276 – e281 ( ISSN 2352-3026 , DOI 10.1016 / S2352-3026 (15) 00094-0 )
- INRS, “ Benzene (FT 49). Patologia - Tossicologia - Scheda tossicologica - INRS ” ,2011(consultato l'8 settembre 2019 )
- Loomis A., “ Carcinogenicity of benzene ” , su www.thelancet.com ,26 ottobre 2017(consultato l'8 settembre 2019 )
- IARC, " Benzene - IARC Monographs on the Evaluation of Cancerogenic Risks to Humans " , su iarc.fr ,2018(consultato l'8 settembre 2019 )
- Kathryn Z Guyton , Dana Loomis , Yann Grosse , Fatiha El Ghissassi Lamia Benbrahim-Tallaa , Neela Guha , Chiara Scoccianti Heidi Mattock e Kurt Straif , " cancerogenicità del Tetraclorvinfos, parathion, malathion, diazinon e glifosato ," The Lancet Oncology , vol . 16, n . 5,2015, pag. 490–491 ( ISSN 1470-2045 , DOI 10.1016 / S1470-2045 (15) 70134-8 )
- Gabriella Andreotti , Stella Koutros , Jonathan N Hofmann , Dale P Sandler , Jay H Lubin , Charles F Lynch , Catherine C Lerro , Anneclaire J De Roos , Christine G Parks , Michael C Alavanja , Debra T Silverman e Laura E Beane Freeman , " Uso del glifosato e incidenza del cancro nello studio sulla salute agricola ", JNCI: Journal of the National Cancer Institute , vol. 110, n . 5,2018, pag. 509–516 ( ISSN 0027-8874 , DOI 10.1093/jnci / djx233 )
- Centre Léon-Bérard , IARC, “ Classificazione dell'IARC per sedi cancerose | Cancro e ambiente ” ,29 novembre 2019(consultato il 29 dicembre 2019 )
- Centre National Hospitalier d'Information sur le Médicament (CNHIM), “ Foglio di reazione avversa ” , su theriaque.org (consultato il 15 settembre 2019 )
- (in) Sachiko Ezoe , " Leucemia secondaria associata all'agente anti-cancro, Etoposide, un inibitore della topoisomerasi II " , International Journal of Environmental Research and Public Health , vol. 9, n . 7,30 novembre 12, pag. 2444 ( DOI 10.3390 / ijerph9072444 , / pmc / articoli / PMC3407914 /? Report = abstract, leggi online )
- Barbara Deschler e Michael Lübbert , “ Leucemia mieloide acuta: epidemiologia ed eziologia ”, Cancro , vol. 107, n . 9,2006, pag. 2099–2107 ( ISSN 0008-543X , DOI 10.1002 / cncr.22233 )
- LLSCanada, " www.llscanada.org " (accessibile il 1 ° marzo 2020 )
- Hoffman, Ronald et al. (2005). Ematologia: principi di base e pratica (4a. Ed.). St. Louis, Mo.: Elsevier Churchill Livingstone. pag. 1074–75
- Leucemia mieloide acuta , N Engl J Med 1999; 341.
- Botton 2017 , p. 500-501
- Schmidt, Cornu, Angellilo-Scherrer et al. , “Le basi fisiopatologiche dell'ematologia generale: un aiuto alla memoria per l'ematologia ” [PDF] , su www.2bib.ch ,2015(consultato il 10 dicembre 2019 ) , p. 149
- Ifrah 2018 , p. 68
- Società francese di ematologia, " Leucemia acuta, 3 - Segni biologici e diagnosi " [html] ,1 ° aprile 2010(consultato il 15 dicembre 2019 )
- Botton 2017 , p. 500
- (in) James W. Vardiman , " La revisione 2016 della classificazione dell'Organizzazione mondiale della sanità delle neoplasie mieloidi e della leucemia acuta " , Blood , American Society of Hematology, vol. 127, n . 20,19 maggio 2016, pag. 2391-2405 ( ISSN 1528-0020 , DOI 10.1182 / blood-2016-03-643544 , abstract , leggi online )
- (in) Karen Seiter, Emmanuel C. Besa et al. , " Stadiazione della leucemia mieloide acuta - Classificazioni FAB e OMS per la leucemia mieloide acuta " , su emedicine.medscape.com ,30 dicembre 2015(consultato il 23 aprile 2016 ) .
- "Aggiornamento sulla leucemia mieloide acuta, settembre 2016, p 3/16"
- " Tutto sulla donazione | Don de Moelle Osseuse ” , su www.dondemoelleosseuse.fr (consultato l'11 novembre 2018 )
- Hartmut Döhner , Elihu Estey , David Grimwade , Sergio Amadori , Frederick R. Appelbaum , Thomas Büchner , Hervé Dombret , Benjamin L. Ebert , Pierre Fenaux , Richard A. Larson , Ross L. Levine , Francesco Lo-Coco , Tomoki Naoe , Dietger Niederwieser , Gert J. Ossenkoppele , Miguel Sanz , Jorge Sierra , Martin S. Tallman , Hwei-Fang Tien , Andrew H. Wei , Bob Löwenberg e Clara D. Bloomfield , “ Diagnosi e gestione della LMA negli adulti: Raccomandazioni ELN 2017 di un gruppo di esperti internazionali ”, Blood , vol. 129, n . 4,2017, pag. 424-447 ( ISSN 0006-4971 , DOI 10.1182 / sangue-2016-08-733196 )
- Martin S. Tallman , Eunice S. Wang , Jessica K. Altman , Frederick R. Appelbaum , Vijaya Raj Bhatt , Dale Bixby , Steven E. Coutre , Marcos De Lima , Amir T. Fathi , Melanie Fiorella , James M. Foran , Aric C. Hall , Meagan Jacoby , Jeffrey Lancet , Thomas W. LeBlanc , Gabriel Mannis , Guido Marcucci , Michael G. Martin , Alice Mims , Margaret R. O'Donnell , Rebecca Olin , Deniz Peker , Alexander Perl , Daniel A. Polyea , Keith Pratz , Thomas Prebet , Farhad Ravandi , Paul J. Shami , Richard M. Stone , Stephen A. Strickland , Matthew Wieduwilt , Kristina M. Gregory , Lydia Hammond e Ndiya Ogba , “ Leucemia mieloide acuta, versione 3.2019 , Linee guida per la pratica clinica del NCCN in oncologia , Journal of the National Comprehensive Cancer Network , vol. 17, n . 6,2019, pag. 721–749 ( ISSN 1540-1405 , DOI 10.6004 / jnccn.2019.0028 )
- (in) Cancer Research UK, " Radioterapia al cervello - Leucemia mieloide acuta " ,16 luglio 2019(consultato il 29 dicembre 2019 )
- (it + es) American Cancer Society, " Radioterapia per la leucemia mieloide acuta (AML) " ,21 agosto 2018(consultato il 29 dicembre 2019 )
- Miguel A. Sanz , Pierre Fenaux , Martin S. Tallman , Elihu H. Estey , Bob Löwenberg , Tomoki Naoe , Eva Lengfelder , Hartmut Döhner , Alan K. Burnett , Sai-Juan Chen , Vikram Mathews , Harry Iland , Eduardo Rego , Hagop Kantarjian , Lionel Adès , Giuseppe Avvisati , Pau Montesinos , Uwe Platzbecker , Farhad Ravandi , Nigel H. Russell e Francesco Lo-Coco , “ Gestione della leucemia promielocitica acuta: raccomandazioni aggiornate da un panel di esperti della European LeukemiaNet ”, Blood , vol. . 133, n ° 15,2019, pag. 1630–1643 ( ISSN 0006-4971 , DOI 10.1182 / sangue-2019-01-894980 )
- Gustave Roussy , " Terapia di supporto - Gustave Roussy " (consultato il 18 marzo 2020 )
- Institut Curie , " Aiutarti durante i trattamenti dell'Institut Curie " (consultato il 18 marzo 2020 )
- (in) . PDQ Adult Treatment Editorial Board, " Adult Acute Myeloid Leukemia Treatment (PDQ®) - Cancer Information Summaries PDQ - NCBI Bookshelf " [html] , Bethesda (MD): National Cancer Institute (US)8 febbraio 2019(consultato il 17 dicembre 2019 )
- Agenzia europea per i medicinali , " Dacogen " ,13 maggio 2019(consultato il 3 gennaio 2020 )
- Botton 2017 , p. 504
- Agenzia di biomedicina , “Attività nazionale di trapianto di CSH (2016) ” [PDF] , su www.agence-biomedecine.fr ,2017(consultato il 7 gennaio 2020 )
- Carreras 2019 , p. 27
- EMA , " Bulsilvex (busulfan) - Riassunto delle caratteristiche del prodotto " [PDF] ,31 agosto 2017(consultato il 23 giugno 2020 )
- Canadian Cancer Society, " Trapianto di cellule staminali per la leucemia mieloide acuta " (consultato il 23 giugno 2020 )
- Ifrah 2018 , p. 77
- “ Ematologia. Oncoematologia - Presentazione - Consulto EM » ,5 dicembre 11(consultato il 7 gennaio 2020 )
- (in) Cancer Research UK, " Radioterapia corporea totale (TBI) Leucemia mieloide acuta " ,16 luglio 2019(consultato il 29 dicembre 2019 )
- The Leukemia & Lymphoma Society of Canada, " Trapianto di cellule staminali allogeniche " (consultato il 7 gennaio 2020 )
- The Leukemia & Lymphoma Society of Canada, " Trapianto di cellule staminali allogeniche a intensità ridotta " (consultato il 23 giugno 2020 )
- (it) European Society for Blood and Marrow Transplant , " Rapporto annuale 2019 " [2019]2019(consultato il 23 giugno 2020 ) ,p. 68
- Jeanette Prada-Arismendy , Johanna C. Arroyave e Sarah Röthlisberger , “ Biomarcatori molecolari nella leucemia mieloide acuta ”, Blood Reviews , vol. 31, n . 1,2017, pag. 63–76 ( ISSN 0268-960X , DOI 10.1016 / j.blre.2016.08.005 )
- (in) American Cancer Society, " Cosa c'è di nuovo nella ricerca sulla leucemia mieloide acuta (AML)? " ,24 giugno 2019(consultato il 23 giugno 2020 )
- Elihu Estey , Judith E. Karp , Ashkan Emadi , Megan Othus e Robert Peter Gale , “ Recenti approvazioni di farmaci per la leucemia mieloide acuta di nuova diagnosi: regali o un cavallo di Troia? », Leucemia , vol. 34, n . 3,2020, pag. 671–681 ( ISSN 0887-6924 , DOI 10.1038 / s41375-019-0704-5 )
- (in) " mutazioni dell'isocitrato deidrogenasi nelle neoplasie mieloidi " (Revisione " Leucemia " pubblicata online l'11 novembre 2016), Nature (rivista) , n o 31,2017, pag. 272–281 ( DOI 10.1038 / leu.2016.275 , leggi online )
- "Ash, Clinicak News, 21 ottobre 2016, AG-221 I risultati clinici promettono un approccio “rivoluzionario” all'AML"
- Starr P, " Midostaurin la prima terapia mirata per migliorare la sopravvivenza nell'AML: potenzialmente in grado di cambiare la pratica ", Am Health Drug Benefits , vol. 9, n o Spec Emissione,febbraio 2016, pag. 1-21 ( PMID 27014400 , PMCID 4782225 )
- Alexander E. Perl , Giovanni Martinelli , Jorge E. Cortes , Andreas Neubauer , Ellin Berman , Stefania Paolini , Pau Montesinos , Maria R. Baer , Richard A. Larson , Celalettin Ustun , Francesco Fabbiano , Harry P. Erba , Antonio Di Stasi Robert Stuart , Rebecca Olin , Margaret Kasner , Fabio Ciceri , Wen-Chien Chou , Nikolai Podoltsev Christian Recher , Hisayuki Yokoyama , Naoko Hosono , Sung-Soo Yoon , I-Hwan Lee , Timothy Pardee , T. Amir Fathi , Nahlaeng Liu , Hasabou , Xuan Liu , Erkut Bahceci e Mark J. Levis , " Gilteritinib o chemioterapia per LMA mutata FLT3 recidivante o refrattaria ", New England Journal of Medicine , vol. 381, n . 18,2019, pag. 1728–1740 ( ISSN 0028-4793 , DOI 10.1056 / NEJ Moa1902688 )
- Arnaud Pigneux , Marie C. Béné , Philippe Guardiola , Christian Recherche , Jean-Francois Hamel , Mathieu Sauvezie , Jean-Luc Harousseau , Olivier Tournilhac , Francesco Witz , Christian Berthou , Martine Escoffre-Barbe , Denis Guyotat , Nathalie Fegueux , Chantal Himberlin , Mathilde Hunault , Martine Delain , Bruno Lioure , Eric Jourdan , Frédéric Bauduer , Francois Dreyfus , Jean-Yves Cahn , Jean-Jacques Sotto e Norbert Ifrah , " L'aggiunta di androgeni migliora la sopravvivenza nei pazienti anziani con leucemia mieloide acuta: Un GOELAMS Study " , Journal of Clinical Oncology , vol. 35, n . 4,2017, pag. 387–393 ( ISSN 0732-183X , DOI 10.1200 / JCO.2016.67.6213 )
- Agenzia europea per i medicinali , " VIDAZA - Riassunto delle caratteristiche del prodotto " [PDF] , su www.ema.europa.eu ,9 luglio 2019(consultato il 25 giugno 2020 )
- Agenzia europea per i medicinali , " www.ema.europa.eu " [PDF] ,25 ottobre 2019(consultato il 18 marzo 2020 )
- Ceylad, " Celyad riporta la prima risposta completa in un paziente con LMA refrattaria e recidivante nello studio THINK " , sul sito web ,3 ottobre 2017(consultato il 18 marzo 2020 )
- Yuxin Liu , Jan Philipp Bewersdorf , Maximilian Stahl e Amer M. Zeidan , “ Immunoterapia nella leucemia mieloide acuta e nelle sindromi mielodisplastiche: l'alba di una nuova era? ", Recensioni di sangue , vol. 34,2019, pag. 67–83 ( ISSN 0268-960X , DOI 10.1016 / j.blre.2018.12.001 )
- (in) American Society of Clinical Oncology , " Leucemia - Mieloide acuta - LMA: Statistiche | Cancer.Net ” , su www.cancer.net ,gennaio 2020(consultato il 27 giugno 2020 )
- (it) National Cancer Institute , " Trattamento per la leucemia mieloide acuta adulta (PDQ®) - Versione per professionisti della salute " su www.cancer.gov ,22 gennaio 2020(consultato il 27 giugno 2020 )
- (a) Cancer Research UK , " Sopravvivenza | Leucemia mieloide acuta | Cancer Research UK ” , su www.cancerresearchuk.org ,19 luglio 2019(consultato il 27 giugno 2020 )
- Mareike Rasche , Martin Zimmermann , Lisa Borschel , Jean-Pierre Bourquin , Michael Dworzak , Thomas Klingebiel , Thomas Lehrnbecher , Ursula Creutzig , Jan-Henning Klusmann e Dirk Reinhardt , " Successi e sfide nel trattamento della leucemia mieloide acuta pediatrica: una retrospettiva analisi degli studi AML-BFM dal 1987 al 2012 ”, Leucemia , vol. 32, n . 10,2018, pag. 2167-2177 ( ISSN 0887-6924 , DOI 10.1038 / s41375-018-0071-7 )
- Fondazione ARC, " Cosa sono le leucemie infantili?" | Fondazione ARC per la Ricerca sul Cancro ” , sul sito web ,14 febbraio 2020(consultato il 18 marzo 2020 )
- American Cancer Society , " Tasso di risposta al trattamento per la leucemia mieloide acuta (AML), " su www.cancer.org ,21 agosto 2018(consultato il 27 giugno 2020 )
- Hoffman et al. 2005, pag. 1071.
- Bennett JH, “ Due casi di ipertrofia della milza e del fegato, in cui la morte è avvenuta per suppurazione del sangue ”, Edinburgh Med Surg J , vol. 64,1845, pag. 413
- (de) R Virchow , Gesammelte Abhandlungen zur Wissenschaftlichen Medizin , Francoforte, Meidinger,1856( leggi online ) , “Die Leukämie” , 190
Bibliografia
![]() : documento utilizzato come fonte per questo articolo.
: documento utilizzato come fonte per questo articolo.
-
Norbert Ifrah ( direttore e coordinatore), Marc Maynadié ( direttore e coordinatore) et al. , Società francese di ematologia, ematologia , Issy-les-Moulineaux, Elsevier Masson, coll. "Gli archivi dei collegi",maggio 2018, 3 e ed. , 400 pag. ( ISBN 978-2-294-75108-0 e 9782294752636 , EAN 9782294752636 , avviso BnF n o FRBNF45533912 ).

-
R. Costello, G. Venton, J. Colle, V. Ivanov, C. Mercier, L. Delassus e V. Baccini (Articolo 13-018-G-50), Leucemia mieloide acuta negli adulti , Elsevier Masson , coll. "EMC / Ematologia",2018, 13 pag. ( ISBN 978-2-84299-505-8 , ISSN 1155-1984 , OCLC 726481102 , DOI 10.1016 / S1155-1984 (18) 83321-0 , leggi online [html] ). .

-
Stéphane Vignot ( dir. E editore), Jean-Charles Soria ( dir. ) E Stéphane de Botton , Gustave Roussy & Université Paris Sud XI, Corso di chemioterapia antitumorale e trattamento medico del cancro , Parigi,gennaio 2018, 32 ° ed. , 534 pag. ( ISBN 978-2-9555469-9-4 ) , cap. 83 ("Leucemia mieloide acuta").

-
(it) Enric Carreras , Carlo Dufour , Mohamad Mohty e Nicolaus Kröger , European Society for Bone Marrow Transplantation, The EBMT Handbook: Hematopoietic Stem Cell Transplantation and Cellular Therapies , Cham, Svizzera, Springer,2019, 688 pag. ( ISBN 978-3-030-02277-8 (correttamente modificato) e 978-3-030-02278-5 , DOI 10.1007 / 978-3-030-02278-5 , leggi online [PDF] ).

Vedi anche
Articoli Correlati
link esterno
Pubblico in generale- Orphanet
- Guida per i pazienti pubblicata dalla European Society of Medical Oncology (ESMO)
- Società Francese di Ematologia
- cancro.be
- cancro.ca
- Fondazione ARC
- Laurette Fugain , associazione impegnata nella lotta alla leucemia
- (it + es) National Cancer Institute Cancer
- Hématocell.fr (laboratorio di ematologia dell'ospedale universitario di Angers)
- (it) European LeukemiaNet
- (it + es) National Cancer Institute Cancer