Fenolo (composto)
| Fenolo | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Struttura del fenolo | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identificazione | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nome IUPAC | fenolo | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sinonimi |
Fenico |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100.003.303 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CE | 203-632-7 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| DrugBank | DB03255 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 996 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| FEMA | 3223 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SORRISI |
c1 (ccccc1) O , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1 / C6H6O / c7-6-4-2-1-3-5-6 / h1-5.7H |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aspetto | cristalli da incolori a gialli o rosa chiaro, con un odore caratteristico | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietà chimiche | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Formula bruta |
C 6 H 6 O [Isomeri] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Massa molare | 94,1112 ± 0,0055 g / mol C 76,57%, H 6,43%, O 17%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| pKa | pKa (PhOH 2 + / PhOH) = -6,4 pKa (PhOH / PhO - ) = 9,95 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Momento dipolare | 1,224 ± 0,008 D | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Diametro molecolare | 0,557 nm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietà fisiche | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fusione | 43 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° bollitura | 182 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solubilità | 76,04 g · l -1 acqua | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Parametro di solubilità δ |
25.1 J 1/2 · cm -3/2 ( 40 ° C ); 11.4 cal 1/2 · cm -3/2 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Massa volumica |
1.073 g · cm -3
equazione:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Temperatura di autoaccensione | 715 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| punto d'infiammabilità | 79 ° C (vaso chiuso) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Limiti di esplosività in aria | 1,36 - 10 % vol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pressione del vapore saturo | a 20 ° C : 47 Pa
equazione:

|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto critico | 61,3 bar , 694,2 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termochimica | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
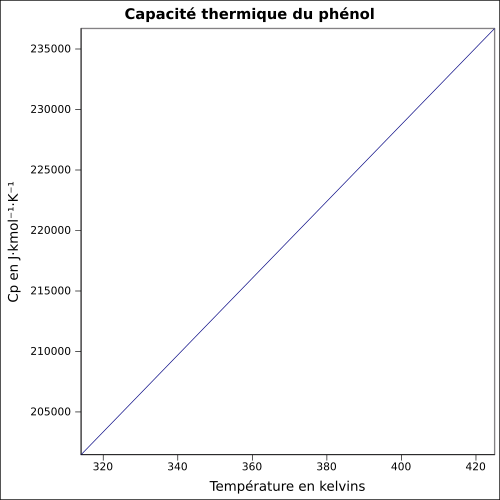
| C p |
equazione:
equazione:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PC | 3053,5 kJ · mol -1 ( 25 ° C , solido) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cristallografia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Classe di cristallo o gruppo spaziale | P 112 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Parametri della mesh |
a = 6,050 Å b = 8,925 Å |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volume | 788.01 Å 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietà ottiche | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Indice di rifrazione | 1.5427 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Precauzioni | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
   Pericolo H301, H311, H314, H331, H341, H373, H301 : Tossico se ingerito H311 : Tossico a contatto con la pelle H314 : Provoca gravi ustioni cutanee e gravi lesioni oculari H331 : Tossico se inalato H341 : Sospettato di provocare difetti genetici (indicare la via di l'esposizione porta allo stesso pericolo) H373 : Presunto rischio di gravi danni agli organi (indicare tutti gli organi interessati, se noti) a seguito di esposizione ripetuta o prolungata (indicare la via di esposizione se è definitivamente dimostrato che nessun'altra via di esposizione porta a lo stesso pericolo) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  D1A, E, D1A : Materiale molto tossico con gravi effetti immediati Trasporto di merci pericolose: classe 6.1 gruppo II E : Materiale corrosivo necrosi della pelle negli animali Divulgazione all'1,0 % secondo l'elenco di divulgazione degli ingredienti |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2 4 0 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Trasporto | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
60 : materiale tossico o che presenta un grado di tossicità minore Numero UN : 1671 : PHENOL SOLID Classe: 6.1 Etichetta: 6.1 : Materie tossiche Confezione: Gruppo di imballaggio II : sostanze moderatamente pericolose; 
60 : materiale tossico o che presenta un grado minore di tossicità Numero UN : 2312 : FENOLO MOLTO Classe: 6.1 Etichetta: 6.1 : Materie tossiche Confezione: Gruppo di imballaggio II : sostanze moderatamente pericolose; 
60 : materiale tossico o che presenta un grado minore di tossicità Numero UN : 2821 : FENOLO IN SOLUZIONE Classe: 6.1 Etichetta: 6.1 : Materie tossiche Confezione: Gruppo di imballaggio II / III : sostanze moderatamente / leggermente pericolose.  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Classificazione IARC | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gruppo 3: non classificabile quanto alla sua cancerogenicità per l'uomo | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ecotossicologia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LogP | 1.46 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Soglia di odore | basso: 0,0045 ppm alto: 1 ppm |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Unità di SI e STP se non diversamente specificato. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Il fenolo , noto anche come idrossibenzene , acido carbolico o acido carbolico , è composto da un nucleo fenile e da una funzione idrossile . È la molecola più semplice della famiglia dei fenoli .
Rappresentazioni
-
Modello compatto
-
Modello di palline e bastoncini
Storia
Viene scoperto allo stato impuro da Johann Rudolf Glauber nel 1650 , dalla distillazione del catrame dal carbone . Glauber lo descrive come " un olio di sangue rosso vivo che secca e guarisce tutte le ulcere umide ".
Nel 1834 , Friedrich Ferdinand Runge riuscì a isolare esso e lo ha chiamato acido fenico .
Nel 1836, Auguste Laurent inventò il termine "fene" per il benzene; questa è la radice dei termini "fenolo" e "fenile".
Nel 1841, il chimico francese Auguste Laurent lo ottenne in forma pura.
Dal 1865 al 1880, il fenolo fu usato come antisettico sotto la guida di Joseph Lister , riducendo il tasso di mortalità durante l'intervento chirurgico dal 65% al 20%.
Il fenolo è stato sintetizzato e prodotto nel 1889 dalla società BASF .
Enol
Il fenolo è anche un enolo (derivato alcolico con funzione alchenica). È la forma tautomerica del cicloesa-2,4-dienone. Ma a differenza della maggior parte degli enoli, è la forma più stabile rispetto al suo chetone tautomerico, stabilità dovuta principalmente alla presenza di un anello aromatico non presente nel corrispondente chetone.

Proprietà fisiche
Il fenolo ha una costante molale crioscopica di 6,84 ° C ∙ kg / mol e una costante molale ebullioscopica di 3,54 ° C ∙ kg / mol.
Di colore bianco puro, tende leggermente a ossidarsi a contatto con l'aria per dare tracce di chinoni che lo colorano rosa, poi rosso.
Produzione
Nel 2005 nel mondo sono state prodotte 8,8 milioni di tonnellate di fenolo, di cui circa il 26% negli Stati Uniti e il 2% in Francia. Il principale produttore è Ineos Phenol (Regno Unito) con una capacità produttiva di 1,6 milioni di tonnellate.
Oggi più dell'85% del fenolo viene prodotto dal processo cumene . Questo processo, messo a punto nel 1944 da Hock e Lang, è stato utilizzato sin dagli anni 50. Il suo vantaggio risiede nella semplicità della sua realizzazione, nella sua buona resa (90%) e nel fatto di ottenere fenolo e acetone dal cumene, disponibile in grandi quantità da prodotti petrolchimici . Consiste in un'ossidazione del cumene da parte dell'aria che fornisce il cumene idroperossido come intermedio che, in un mezzo acquoso acido , dà fenolo e acetone.
uso
- Due terzi della produzione di fenolo vengono utilizzati per produrre materie plastiche ( policarbonati , resine epossidiche ).
- Intermedio importante per molte sintesi di prodotti farmaceutici. Vedi fenolo (gruppo) .
- In profumeria : timolo , estragolo , eugenolo , vanillina , ecc.
- In medicina , è usato principalmente come un forte antisettico . Viene anche utilizzato in dermatologia nel trattamento delle unghie incarnite (fenolizzazione).
- Nella biologia molecolare , il fenolo viene utilizzato per rimuovere le proteine nei protocolli di estrazione degli acidi nucleici .
- Preparazione della fenolftaleina , un indicatore di pH ben noto ai chimici.
- Per azione del cloro gassoso sul fenolo si ottengono clorofenoli , come il 2,4,6-triclorofenolo .
- Utilizzato in entomologia per la conservazione di letti di insetti contro le muffe.
- Negli alimenti , per la conservazione della carne .
- Il fenolo è utilizzato per la produzione di carta.
- In combinazione con acido solforico concentrato, viene utilizzato come metodo di colorazione dei carboidrati per la loro determinazione mediante spettrofotometria .
sicurezza
Il fenolo è altamente corrosivo per gli organismi viventi. Una soluzione acquosa all'1% è sufficiente per causare una grave irritazione.
Le ustioni da fenolo sono molto dolorose e richiedono molto tempo per guarire. Inoltre, possono essere seguite da gravi complicazioni che possono portare alla morte a causa della tossicità di questo composto e della sua capacità di entrare nel corpo attraverso la pelle.
Queste proprietà rendono il fenolo un agente delle mutilazioni genitali femminili . In effetti, il D r Kellogg sosteneva di bruciare il clitoride fenolo come "rimedio" contro la masturbazione.
Durante la seconda guerra mondiale , i prigionieri ad Auschwitz e in altri campi furono giustiziati da una puntura di fenolo nel cuore. Maximilien Kolbe è stato ucciso da un'iniezione di fenolo nel braccio dopo quattordici giorni di detenzione senza cibo. Il medico delle SS Karl Babor che officiava nel campo di Gross-Rosen era uno specialista nell'assassinio con siringhe di fenolo.
Articoli Correlati
- Cresolo , fenolo sostituito con un gruppo metile
-
Benzenediol , fenolo sostituito con un secondo gruppo idrossile
- Pirocatecolo (catecolo), isomero orto
- Resorcinolo (resorcinolo), meta isomero
- Idrochinone , para isomero
- Benzenetriol
- Benzenetetrol
- Benzenepentol
- Benzenehexol
Note e riferimenti
- PHENOL , scheda / e di sicurezza del Programma internazionale sulla sicurezza delle sostanze chimiche , consultato il 9 maggio 2009
- (a) David R. Lide, Manuale di chimica e fisica , Boca Raton, CRC,16 giugno 2008, 89 ° ed. , 2736 p. ( ISBN 978-1-4200-6679-1 e 1-4200-6679-X ) , p. 9-50
- (it) Yitzhak Marcus, Le proprietà di solventi , vol. 4, Regno Unito, John Wiley & Sons Ltd,1999, 239 p. ( ISBN 0-471-98369-1 )
- massa molecolare calcolata dal " peso atomico degli elementi 2007 " su www.chem.qmul.ac.uk .
- (en) Şerban Moldoveanu, Preparazione del campione in cromatografia , Elsevier ,2002, 930 p. ( ISBN 0-444-50394-3 ) , p. 258
- (in) JG Speight, Norbert Adolph Lange, Manuale di chimica di Lange , McGraw-Hill,2005, 16 ° ed. , 1623 p. ( ISBN 0-07-143220-5 ) , p. 2.289
- (en) Robert H. Perry e Donald W. verde , di Perry Chemical Engineers' Handbook , Stati Uniti d'America, McGraw-Hill,1997, 7 ° ed. , 2400 p. ( ISBN 0-07-049841-5 ) , p. 2-50
- " Properties of Various Gases " su flexwareinc.com (accesso 12 aprile 2010 )
- (in) Carl L. Yaws, Handbook of Thermodynamic Diagrams: Organic Compounds C8 to C28 , vol. 2, Huston, Texas, Gulf Pub. Co.,1996, 396 p. ( ISBN 0-88415-858-6 )
- (a) David R. Lide , CRC Handbook of Chemistry and Physics , Boca Raton, CRC Press,18 giugno 2002, 83 ° ed. , 2664 p. ( ISBN 0849304830 , presentazione online ) , p. 5-89
- (in) " fenolo " su www.reciprocalnet.org (accessibile 12 Dicembre 2009 )
- Gruppo di lavoro IARC sulla valutazione dei rischi cancerogeni per l'uomo, " Valutazioni globali di carcinogenicità per gli esseri umani, Gruppo 3: non classificabili per quanto riguarda la loro cancerogenicità per gli esseri umani " , su http://monographs.iarc.fr , IARC,16 gennaio 2009(visitato il 22 agosto 2009 )
- Numero indice (en) nella tabella 3.1 dell'allegato VI del regolamento CE n . 1272/2008 (16 dicembre 2008)
- " Fenolo " nel database dei prodotti chimici Reptox del CSST (organizzazione del Quebec responsabile per la sicurezza e la salute sul lavoro), accesso 25 aprile 2009
- Voce "Phenol" nel database delle sostanze chimiche GESTIS dell'IFA (ente tedesco responsabile della sicurezza e della salute sul lavoro) ( tedesco , inglese ), accesso 25 agosto 2009 (JavaScript richiesto)
- (in) " Phenol " su hazmap.nlm.nih.gov (visitato il 14 novembre 2009 )
- Auguste Laurent, Sugli acidi clorofenici e clorofenisici e clorofenesici ,1836, Do il nome di fene al radicale fondamentale degli acidi precedenti ( φαινω , illumino), poiché la benzina si trova nel gas di illuminazione.
- Annales de chimie et de physique , V. Masson (Parigi), 1816-1913 ( leggi in linea )
- (in) Sito web aziendale
- dati sulla produzione industriale di fenolo , Chemical Society di Francia , 8 ° ed. , 2009
- Heinrich Hock (1887-1971) è un chimico tedesco, formatosi all'Università Tecnica di Monaco da Karl Andreas Hofmann . Ha insegnato dal 1927 al 1958 all'Institut des Charbonnages di Mülheim, poi chimica degli esplosivi all'École des Mines di Clausthal .
- Shon Lang era il collega di Heinrich Hock a Clausthal.
- " Trattamento dell'unghia incarnita dell'unghia del piede incarnita fenolo con e-sante.fr " su e-sante.fr (accesso 6 maggio 2016 ) .
- () Michel. DuBois , KA Gilles , JK Hamilton e PA Rebers , " Metodo colorimetrico per la determinazione degli zuccheri e delle sostanze correlate " , Analytical Chemistry , vol. 28, n o 3,Marzo 1956, p. 350-356 ( ISSN 0003-2700 e 1520-6882 , DOI 10.1021 / ac60111a017 , letto online , accesso 10 novembre 2019 )
- S. Suzanne Nielsen , "Phenol-Sulfuric Acid Method for Total Carbohydrates" , in Food Analysis Laboratory Manual , Springer US,2010( ISBN 9781441914620 , DOI 10.1007 / 978-1-4419-1463-7_6 , leggi online ) , p. 47–53
- (a) John Harvey Kellogg, Plain Facts for Old and Young ,1888, 644 p. ( ISBN 978-0-405-05808-0 )