Silano (famiglia di composti)
In chimica i silani sono, secondo la definizione IUPAC , la famiglia di composti chimici costituiti da uno scheletro di silicio e idrogeno , di formula lorda generale Si n H 2 n +2. Il termine è costruito per strato con quello di " alcani ", i loro analoghi di carbonio , proprio come i tedeschi sono analoghi al germanio . Come gli alcani, i silani possono avere una struttura lineare ( n- silani) o ramificata ( iso e neo- silani). A seconda della lunghezza della catena, possono essere suddivisi in oligosilani (catena corta) o polisilani. Esistono anche sotto forma di composti ciclici, ciclosilani, i cui composti monociclici hanno la formula lorda generale Si n H 2 n.
Il termine silano è anche usato in modo meno rigoroso per denotare derivati idrocarbilici e altri derivati di veri silani.
Struttura e proprietà
Se ci sono silani ramificati e ciclici , sono molto meno numerosi e diversi degli alcani . Nel 2020 erano noti silani aciclici lineari o ramificati aventi fino a otto atomi di silicio e silani ciclici aventi fino a sei atomi di silicio. Tutti loro appaiono come gas o liquidi incolori in condizioni normali di temperatura e pressione. I polisilani diventano rapidamente instabili man mano che si allungano, ma sono molto più stabili come alogenuri o derivati sostituiti con residui organici.
I silani hanno proprietà simili agli alcani a cui corrispondono, come il punto di fusione , il punto di ebollizione e il momento di dipolo . Come gli alcani , in genere adottano una geometria tetraedrica risultante dalla sp 3 ibridazione dei i orbitali di legame . Tuttavia, esistono differenze fondamentali tra la chimica degli idrocarburi e quella dei silani. Poiché il silicio è meno elettronegativo del carbonio e dell'idrogeno , i legami nei silani sono generalmente più polarizzati di quelli in analoghi composti idrocarburici . Gli atomi di idrogeno legati hanno un carattere elettronegativo e quindi reagiscono facilmente con gli atomi di idrogeno degli acidi .
L' energia del legame Si - H è 378 kJ / mol , sensibilmente inferiore a quella del legame C - H , che è piuttosto 414 kJ / mol , il che rende i silani meno stabili termicamente degli alcani.
Silani lineari
La serie omologa di silani lineari corrisponde alla formula Si n H 2 n +2con n = 1, 2, 3, ecc.
| Silano | Formula | Punto di fusione | Punto di ebollizione | Massa volumica | Massa molare |
|---|---|---|---|---|---|
| Silano | SiH 4 | −184,7 ° C | −112,1 ° C | (gas) 1,35 kg / m 3 | 32,12 g / mol |
| Disilano | Se 2 H 6 | −129,4 ° C | −14,8 ° C | (gas) 2,87 kg / m 3 | 62,22 g / mol |
| Trisilano | Si 3 H 8 | −116,9 ° C | 52,9 ° C | 0,739 g / cm 3 | 92,32 g / mol |
| Tetrasilano | Se 4 H 10 | −91,6 ° C | 108,4 ° C | 0,795 g / cm 3 | 122,42 g / mol |
| Pentasilano | Se 5 H 12 | −72,2 ° C | 153,2 ° C | 0,827 g / cm 3 | 152,52 g / mol |
| Esasilano | Se 6 H 14 | −44,7 ° C | 193,6 ° C | 0,847 g / cm 3 | 182,62 g / mol |
| Eptasilano | Se 7 H 16 | −30,1 ° C | 226,8 ° C | 0,859 g / cm 3 | 212,73 g / mol |
| Octasilane | Se 8 H 18 | - | - | - | 242,83 g / mol |
Solo il silano SiH 4può essere conservato indefinitamente a temperatura ambiente: è il più stabile dei silani. In assenza di catalizzatore , si decompone a 500 ° C . I termini superiori della serie lineare dei silani sono sempre meno termicamente stabili e si decompongono anche a temperatura ambiente alla luce del giorno, dando polimeri , silani più leggeri e idrogeno . Il riscaldamento a temperature più elevate porta alla decomposizione dei silani in silicio e idrogeno. Questo forma silano SiH 4durante la termolisi di silani superiori e silani sostituiti come il triclorosilano HSiCl 3e trietossisilano HSi (OCH 2 CH 3 ) 3 :
4 HSiCl 3⟶ 3 SiCl 4+ SiH 4 ; 4 HSi (OCH 2 CH 3 ) 3⟶ 3 Si (OCH 2 CH 3 ) 4+ SiH 4.Silani ramificati e ciclici
Da tetrasilano Si 4 H 10, ci sono isomeri di catena come l'isotetrasilano HSi (SiH 3 ) 3, Analogo di isobutano HC (CH 3 ) 3, isopentasilano SiH 3 SiH 2 SiH (SiH 3 ) 2e neopentasilano Si (SiH 3 ) 4, analoghi rispettivamente dell'isopentano CH 3 CH 2 CH (CH 3 ) 2e neopentano C (CH 3 ) 4. Esistono anche silani ciclici . Questi diversi isomeri differiscono l'uno dall'altro in varie proprietà come i punti di fusione e di ebollizione.
| Silano | Formula | Struttura | Punto di fusione | Punto di ebollizione | Massa volumica | Massa molare | |
|---|---|---|---|---|---|---|---|
| Silani ramificati | |||||||
| Isotetrasilano | Se 4 H 10 |
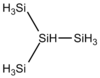
|
−99,4 ° C | 101,7 ° C | 0,793 g / cm 3 | 122,42 g / mol | |
| Isopentasilane | Se 5 H 12 | −109,8 ° C | 146,2 ° C | 0,820 g / cm 3 | 152,52 g / mol | ||
| Neopentasilane | Se 5 H 12 | −57,8 ° C | 130 ° C | - | 152,52 g / mol | ||
| Silani ciclici | |||||||
| Cyclopentasilane | Se 5 H 10 |
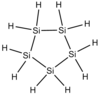
|
−10,5 ° C | 194,3 ° C | 0,963 g / cm 3 | 150,51 g / mol | |
| Cicloesasilano | Se 6 H 12 |

|
16,5 ° C | 226 ° C | - | 180,61 g / mol | |
Reazioni
I silani sono meno stabili degli alcani analoghi. Possono essere prodotti solo in assenza di aria. I quattro silani più leggeri sono molto reattivi e piroforici , cioè possono accendersi nell'aria ed esplodere lì. La loro combustione in ossigeno dà biossido di silicio SiO 2e acqua H 2 O :
SiH 4+ 2 O 2⟶ SiO 2+ 2 H 2 O.La reattività dei silani diminuisce per i composti più pesanti, oltre il tetrasilano. Sono, tuttavia, relativamente stabili in acqua priva di ossigeno e possono essere conservati più a lungo in soluzioni saline. In acqua basica , si decompongono lentamente per formare silice e idrogeno , una reazione che diventa massiccia e immediata in soluzioni fortemente basiche. La reazione può essere controllata per rilasciare una molecola di idrogeno mediante legami Si - H e Si - H , che rende possibile
SiH 4+ 4 H 2 O⟶ Si (OH) 4+ 4 ore 2 ; SiH 4+ 2 KOH + H 2 O⟶ K 2 SiO 3+ 2 ore 2.L' idrolisi degli organosilani è una reazione del primo ordine . La velocità di idrolisi del legame Si - H dipende dal tipo e dal numero di residui organici. L'idrolisi dei trialchilsilani è significativamente più lenta di quella dei triarilsilani. Ciò può essere spiegato da un aumento della densità elettronica sull'atomo di silicio sotto l'effetto dei residui alchilici . La velocità di reazione dei tri- n -alkylsilanes diminuisce quindi nella etile > propile > butile ordine . Tra i trialchilsilani, quelli che sono sostituiti con gruppi n -alchilici reagiscono dieci volte più velocemente di quelli che hanno gruppi alchilici ramificati isomerici.
Il silano SiH 4reagisce con il metanolo CH 3 OHper dare il dimetossisilano SiH 2 (OCH 3 ) 2, trimetossisilano SiH (OCH 3 ) 3e tetrametossisilano Si (OCH 3 ) 4( ortosilicato di tetrametile ), ma non metossisilano SiH 3 OCH 3.
La reazione dei silani con metalli alcalini disciolti in solventi dà i corrispondenti derivati alcalini sililici . A seconda del solvente, possono verificarsi due reazioni concorrenti, ad esempio la prima reazione da sola in esametilfosforammide [(CH 3 ) 2 N] 3 PO(HMPA) ed entrambi contemporaneamente in dimetossietano CH 3 OCH 2 CH 2 OCH 3 :
2 SiH 4+ 2 K ⟶ 2 KSiH 3+ H 2 ; SiH 4+ 2 K ⟶ KSiH 3+ KH .Con i reagenti di Grignard , i silani danno i corrispondenti alchilsilani, formando preferenzialmente i silani peralchilati.
I silani possono anche reagire con l' azoto a circa 500 ° C decomponendosi, dando luogo al silicio che reagisce con l'azoto. È anche possibile utilizzare la radiazione a microonde per promuovere la decomposizione. Questa reazione viene sfruttata ad esempio per depositare matasse di nitruro di silicio , o per produrre microcristalli di questo materiale.
Derivati silani
Derivati alogenati
Il clorosilano SiH 3 Cl, diclorosilano SiH 2 Cl 2, triclorosilano SiHCl 3e tetracloruro di silicio SiCl 4sono noti derivati alogenati del silano SiH 4. Il triclorosilano è particolarmente importante nell'industria perché è di facile ottenimento e viene utilizzato come punto di partenza per la produzione di silano, diclorosilano e silicio ultrapuro. Oltre alla preparazione da silicio e alogenuro di idrogeno con il metodo storico di Friedrich Wöhler , possono essere ottenuti anche facendo reagire silani con un alogenuro di idrogeno anidro in presenza di cloruro di alluminio AlCl 3 a temperatura moderata:
SiH 4+ n HX ⟶ SiH 4– n X n+ n H 2, Dove X = Cl , Br e n = 1, 2, 3 .Sebbene la reazione del silano con cloro e bromo sia esplosiva a temperatura ambiente, può essere condotta in modo controllato a temperature inferiori:
SiH 4+ Br 2⟶ SiH 3 Br(+ H 2 SiBr 2) + HBr a -80 ° C .Organosilani
Il legame Si - C è molto stabile e, già nel 1917, Alfred Stock riferì l'esistenza di più di 50 tetraalchilsilani e tetraarilsilani. Questi composti sono termicamente stabili, sono resistenti all'acqua e possono essere alogenati , nitrati o solfonati sul residuo organico senza che il legame Si-C venga rotto. Il tetrametilsilano Si (CH 3 ) 4è un composto importante, in gran parte chimicamente inerte, utilizzato come standard nella spettroscopia NMR . Data la stabilità del legame Si - C, è possibile ottenere composti come l'esafenildisilano Si 2 (C 6 H 5 ) 6che non hanno carbonio omologo ( esafeniletano (en) C 2 (C 6 H 5 ) 6 non potrebbe mai essere sintetizzato).
Gli organosilani possono essere preparati facendo reagire derivati silanici alogenati o silani con organolitici o tramite una reazione di Grignard :
Si 2 Cl 6+ 6 CH 3 MgCl⟶ Si 2 (CH 3 ) 6+ 6 MgCl 2.Gli organoalosilani sono prodotti su scala industriale mediante sintesi di Müller-Rochow :
2 CH 3 Cl+ Si ⟶ SiCl 2 (CH 3 ) 2.Silanoli, silossani, siliconi
L' idrolisi dei silani, ed in particolare dei loro derivati alogenati, dà facilmente silanoli che, a differenza di alcoli simili, sono relativamente instabili. Essi polimerizzano con l'eliminazione di acqua per dare silossani e siliconi , il cloruro di idrogeno accelerare la polimerizzazione. I monosilanoli formano dimeri , i silanedioli formano polimeri lineari e i silanetrioli formano reti tridimensionali. Queste reazioni sono favorite dal fatto che i legami Si - O - Si sono particolarmente stabili.
2 ClSi (CH 3 ) 3+ H 2 O⟶ 2 HOSi (CH 3 ) 3+ HCl ; 2 HOSi (CH 3 ) 3⟶ (CH 3 ) 3 Si - O - Si (CH 3 ) 3+ H 2 O.Applicazioni
Il triclorosilano SiHCl 3è un prodotto intermedio per la produzione di silicio ultrapuro destinato all'industria dei semiconduttori , per la produzione di promotori di adesione e per trattamenti superficiali. La termolisi dei silani in atmosfera di idrogeno consente inoltre di depositare silicio ultrapuro ( processo Siemens (de) ).
La silice pirogenica , che è in particolare una carica comunemente utilizzato con materia plastica , può essere prodotto da clorosilani e chloroalkylsilanes per reazione in un ossidrica fiamma . Gli organosilani funzionali sono utilizzati per il metodo di funzionalizzazione delle superfici chiamato silanizzazione (in) . Clorometilsilani, in particolare dimetildiclorosilano SiCl 2 (CH 3 ) 2, vengono utilizzati come materia prima per la produzione di siliconi .
È possibile depositare un sottile strato di silicio ossidando il diclorosilano SiH 2 Cl 2sotto pressione ridotta. Nel contesto della fabbricazione di dispositivi semiconduttori , un metodo di deposizione chimica da vapore, plasma potenziato ( PECVD ) consente, in determinate condizioni, di depositare strati dielettrici sul biossido di silicio SiO 2da silano SiH 4e per esempio monossido di azoto .
I silani più pesanti, che non sono più piroforici , sono stati studiati come propellenti in astronautica . Tuttavia, essi hanno un costo elevato ed una inferiore impulso specifico di idrazina o LOX / LH2 propellenti , ma composti come pentasilane Si 5 H 12 potrebbero essere usati come additivi non tossici per alcuni propellenti.
Note e riferimenti
- (in) " silani " Compendio di terminologia chimica [ " libro d'oro "], IUPAC 1997 corretti versione online (2006-), 2 ° ed.
- (en) NN Greenwood e A. Earnshaw, chimica degli elementi , Elsevier, 2012, p. 337 . ( ISBN 978-0-08-050109-3 )
- (en) [PDF] Barry Arkles, " Silani ", pag. 39 , ristampare Kirk-Othmer, Encyclopedia of Chemical Technology , 4 ° edizione, vol. 22, John Wiley & Sons, 1997, pag. 38-69 . ( ISBN 0-471-52691-6 )
- (a) AF Holleman, E. Wiberg e N. Wiberg, Lehrbuch der Chemie Anorganischen , 101 ° ed., Walter de Gruyter, 1995, p. 485 . ( ISBN 3-11-012641-9 )
- (de) Bernhard Hidding, “ Untersuchung der Eignung von Silanenals Treibstoffe in der Luft und Raumfahrt ” , a https://web.archive.org/ , Bundeswehr Università di Monaco di Baviera e Heinrich Heine University di Dusseldorf , gennaio 2004(accesso 23 gennaio 2021 ) .
- (in) Barry Arkles, Youlin Pan, Fernando Jove, Jonathan Goff e Alain Kaloyeros , " Synthesis and Exploratory Studies of Deposition Isotetrasilane and Reactive Intermediates for Epitassial Silicon " , Inorganic Chemistry , Vol. 58, n o 5, 20 febbraio 2019, p. 3050-3057 ( PMID 30785274 , DOI 10.1021 / acs.inorgchem.8b02761 , leggi in linea )
- (in) James C. Sturm e Keith H. Chung , " Chemical Vapor Deposition Epitxy of Silicon-based Materials using Neopentasilane " , ECS Transactions , Vol. 16, n o 10, ottobre 2008, p. 799 ( DOI 10.1149 / 1.2986839 , Bibcode 2008ECSTr..16j.799S , leggi online )
- (de) G. Schott e C. Harzdorf , “ Silane . I Alkalische Solvolyse von Triorganosilanen " , Zeitschrift für anorganische une allgemeine Chemie , vol. 306, n ossa 3-4, Ottobre 1960, p. 180-190 ( DOI 10.1002 / zaac.19603060306 , leggi in linea )
- (in) Jingwei Song Xiying Ma Zui Wang, Chen Wei e Chen Zhongpin , " Fabrication of Si 3 N 4 Nanocrystals and Nanowires Using PECVD " , Advances in Materials Sciences and Engineering , vol. 2010,29 giugno 2010, Articolo n . 892,792 ( DOI 10.1155 / 2010/892792 , leggi online )
- (in) JR Flemish e RL Pfeffer , " Film di nitruro di silicio a basso contenuto di idrogeno dal plasma di risonanza di ciclotrone elettronico " , Journal of Applied Physics , vol. 74, n o 5, Settembre 1993, p. 3277-3281 ( DOI 10.1063 / 1.355318 , Bibcode 1993JAP .... 74.3277F , leggi online )
- (de) Josef Goubeau e Rudolf Warncke , " Zur Hydrolyse von Halogeniden. I. Die Hydrolysis of Siliciumtetrachlorids " , Zeitschrift für anorganische Chemie , vol. 259, n osso 1-4 Luglio 1949, p. 109-120 ( DOI 10.1002 / zaac.19492590109 , leggi in linea )
- (de) Eugen Unger , “ Die Erzeugung dünner Schichten. Das PECVD - Verfahren: Gasphasenabscheidung in einem Plasma " , Chemie in unzerer Zeit , vol. 25, n o 3, Giugno 1991, p. 148-158 ( DOI 10.1002 / ciuz.19910250306 , leggi in linea )
link esterno
- Risorsa relativa alla salute :