Dibroma
| Dibroma | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dibroma | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identificazione | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100.028.890 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CE | 231-778-1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aspetto | liquido fumante, dal rosso al marrone, odore pungente | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietà chimiche | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Formula bruta |
Br 2 [Isomeri] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Massa molare | 159,808 ± 0,002 g / mol Br 100%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietà fisiche | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fusione | −7,2 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° bollitura | 58.8 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solubilità | in acqua a 20 ° C : 31 g · l -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Massa volumica |
3,1 g · ml -1
equazione:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pressione del vapore saturo | a 20 ° C : 23,3 kPa
equazione:

|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Viscosità dinamica |
viscosità cinematica a 20 ° C : 0,314 mm 2 · s -1 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto critico | 103.0 bar , 314,85 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termochimica | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
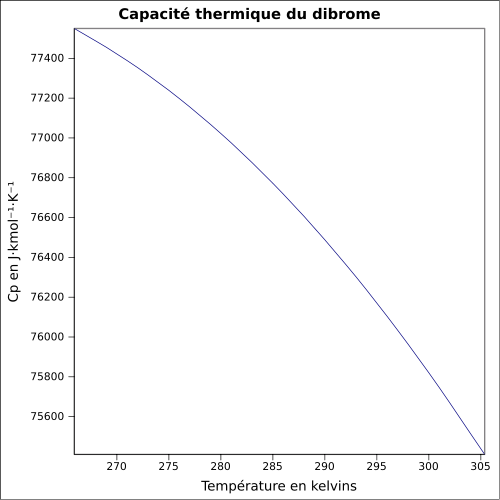
| C p |
equazione:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cristallografia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Simbolo di Pearson | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Classe di cristallo o gruppo spaziale | Cmca ( n o 64) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Strukturbericht | A14 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Struttura tipica | Io 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Precauzioni | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
   Pericolo H314, H330, H400, H314 : Provoca gravi ustioni cutanee e gravi lesioni oculari H330 : Letale se inalato H400 : Molto tossico per gli organismi acquatici |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  D1A, E, D1A : Materiale molto tossico che causa effetti gravi immediati Letalità acuta: LC50 inalazione / 4 ore (topo) = 145 ppm E : Materiale corrosivo Trasporto di merci pericolose: classe 8 Divulgazione all'1,0% secondo l'elenco di divulgazione degli ingredienti |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 0 3 0 BUE | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Trasporto | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
886 : sostanza molto corrosiva e tossica Numero UN : 1744 : BROMO; o BROMO SOLUZIONE Classe: 8 Etichette: 8 : Materie corrosive 6.1 : Materie tossiche Confezione: Gruppo di imballaggio I : sostanze molto pericolose;   |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ecotossicologia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Soglia di odore | basso: 0,0099 ppm alto: 0,46 ppm |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Unità di SI e STP se non diversamente specificato. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Il bromo ( Br 2 ) è una molecola composta da due atomi di bromo . È l'unica forma molecolare ( allotropica ) dell'elemento bromo.
Il dibroma è un liquido rosso molto volatile. È molto tossico per inalazione e provoca gravi ustioni . I vapori attaccano le mucose, la pelle e il sistema respiratorio. La sua soluzione acquosa si chiama " acqua di bromo ", che è molto meno dannosa.
Proprietà ossidante
Bromo ha un alto potere ossidante: E ° (Br 2 / Br - ) = 1,07 V .
Pertanto, l' acqua di bromo consente di dimostrare la presenza di un doppio legame (vedi test Dibroma ) ossidandolo.
Precauzioni
Per il suo forte potere ossidante, ed essendo estremamente volatile, il bromo rilascia vapori tossici, soffocanti e rossastri.
A contatto con la pelle provoca ferite che guariscono molto lentamente.
Il dibroma viene distrutto da una soluzione di tiosolfato di sodio .
Riferimenti
- BROME , scheda / i di sicurezza del Programma internazionale sulla sicurezza delle sostanze chimiche , consultato il 9 maggio 2009
- massa molecolare calcolata dal " peso atomico degli elementi 2007 " su www.chem.qmul.ac.uk .
- (en) Robert H. Perry e Donald W. verde , di Perry Chemical Engineers' Handbook , Stati Uniti d'America, McGraw-Hill ,1997, 7 ° ed. , 2400 p. ( ISBN 978-0-07-049841-9 ) , p. 2-50
- " Properties of Various Gases " su flexwareinc.com (accesso 12 aprile 2010 )
- " The Molecular Iodine (I2) Crystal Structure (A14) " , su cst-www.nrl.navy.mil (consultato il 17 dicembre 2009 )
- "bromine" , su ESIS , accesso 11 febbraio 2009
- Inserimento del numero CAS "7726-95-6" nel database delle sostanze chimiche GESTIS dell'IFA (ente tedesco responsabile della sicurezza e della salute sul lavoro) ( tedesco , inglese ), accesso 27 novembre 2008 (JavaScript richiesto)
- Numero indice nella Tabella 3.1 dell'Allegato VI del Regolamento CE n . 1272/2008 (16 dicembre 2008)
- " Bromo " nel database dei prodotti chimici Reptox del CSST (organizzazione del Quebec responsabile per la sicurezza e la salute sul lavoro), accesso 25 aprile 2009
- " Bromine " , su hazmap.nlm.nih.gov (visitato il 14 novembre 2009 )
link esterno
- Scheda tossicologica , sul sito INRS , 2006