cisteina
| cisteina | |
 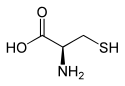 L o R (+) - cisteina e D o S (-) - cisteina |
|
| Identificazione | |
|---|---|
| nome IUPAC | acido 2-ammino-3-mercapto-propanoico |
| Sinonimi |
C, Cis |
| N o CAS |
(racemico) L oR(+) D oS(-) |
| N o ECHA | 100.000,145 |
| N o EC | 200-158-2 L 213-062-0 D |
| N o E | E920 L |
| FEMA | 3263 litri |
| Proprietà chimiche | |
| Formula |
C 3 H 7 N O 2 S [Isomeri] |
| Massa molare | 121,158 ± 0,009 g / mol C 29,74%, H 5,82%, N 11,56%, O 26,41%, S 26,47%, |
| pKa | 1,91 8,14 10,28 |
| Proprietà fisiche | |
| T° fusione | 240 °C |
| solubilità | 280 g · L -1 in acqua ( 25 °C ) |
| Proprietà biochimiche | |
| codoni | UGU , UGC |
| isoelettrico pH | 5.07 |
| Aminoacido essenziale | Secondo il caso |
| Presenza nei vertebrati | 3,3% |
| Precauzioni | |
| WHMIS | |
|
Prodotto non controllatoQuesto prodotto non è controllato secondo i criteri di classificazione WHMIS. |
|
| Direttiva 67/548/CEE | |
 Xn Simboli : Xn : Nocivo Frasi R : R22 : Nocivo per ingestione. Frasi R : 22, |
|
| Unità di SI e STP se non diversamente indicato. | |
La cisteina (Abbreviazioni IUPAC - IUBMB : Cys e C ) del greco antico κύστις ( " vescica ") è un acido α-amino acido il cui enantiomero L è uno dei 22 amminoacidi proteinogenici , codificati sul RNA messaggero dal UGU e UGC codoni . Non è considerato essenziale per l' uomo ma può essere prodotto in quantità insufficiente dall'organismo a seconda dello stato di salute degli individui - soprattutto nel caso di alcune malattie metaboliche e sindromi da malassorbimento - così come nei pazienti, nei bambini e negli anziani.
È un α-amminoacido naturale caratterizzato dalla presenza di un gruppo sulfidrilico –SH che forma un tiolo ; la selenocisteina e la tellurocisteina sono di simili il cui atomo di zolfo è sostituito rispettivamente da un atomo di selenio e di tellurio .
La cisteina è presente in piccole quantità nella maggior parte delle proteine . La sua presenza nelle proteine è molto importante, in particolare perché permette la formazione di ponti disolfuro . Il gruppo tiolico è molto fragile perché si ossida facilmente. La sua ossidazione porta alla cistina , che consiste in due molecole di cisteina unite da un ponte disolfuro. Un ossidante più forte può ossidare la cisteina sul suo zolfo per dare acido cisteico HO 3 S – CH 2 –CH (NH 2 ) COOH, all'origine della taurina , un prodotto di decarbossilazione presente nella bile sotto forma di taurocolato .
Diverse reazioni vengono utilizzate per "proteggere" i tioli dalle cisteine, o per ridurre i ponti disolfuro, in particolare:
- Spostamento da un grande eccesso di tioli liberi:
- da monotioli del tipo R-SH. Il più comunemente usato è il 2-Mercaptoetanolo : HS H 2 C – CH 2 OH,
- da ditioli ciclizzabili, ad esempio ditiotreitolo : HS H 2 C – CHOH – CHOH – CH 2 SH ;
- Alchilazione di tioli liberi.
Il blocco dell'alchilazione è comunemente usato quando si studiano le proteine. Utilizza in particolare la iodoacetammide che porta alla carbossiammidometilazione:
Cis – SH + IH 2 C – CONH 2→ Cis – S – CH 2 –CONH 2.La cisteina può essere assunta come integratore alimentare sotto forma di N- acetilcisteina (NAC).
È stata in grado di svolgere un ruolo importante nello sviluppo della vita sulla terra.
Applicazione
La cisteina è autorizzata come additivo alimentare e porta il numero E920 .
Produzione
L' acido L- cisteico e la L- cisteina possono essere prodotti in quantità industriali da alcuni OGM , in particolare Escherichia coli da glucosio e sali minerali , da piume disciolte in acido cloridrico e da capelli umani , che ne contengono di più. Quest'ultimo modo di produzione è stato bandito in Francia da un parere del Consiglio Superiore di Igiene Pubblica di Francia con parere dell'8 giugno 1999 “vista la raccomandazione generale del Comitato Scientifico per l'alimentazione umana contraria al riciclaggio intra-specie”; questa decisione è tuttavia difficile da applicare perché l'origine della cisteina distribuita non può essere determinata facilmente.
L' Autorità europea per la sicurezza alimentare (EFSA) ha autorizzato, con una direttiva delottobre 2010, L'uso della L- cisteina nei biscotti per neonati e bambini piccoli per prevenire il soffocamento per frammentazione del grasso a basso contenuto di biscotti . Più in generale, la cisteina consente alla pasta di trattenere meglio i gas e di conservare a lungo le forme voluminose, il che favorisce l'afflusso di questi prodotti ai pasticceri .
Alimenti che sono fonti di cisteina
- Lievito di birra
- Germe di grano
- Aglio
- Cipolla
- cavoletti di Bruxelles
- Canapa
- Broccoli
- Latticini
- Noccioline
- Semi
- fonio
- Frutti di mare
- Pesce
- Uova
- La carne
Azione nel corpo umano
La cisteina è coinvolta nella sintesi della melanina , il pigmento naturale della pelle e dei capelli .
È anche coinvolto nella sintesi del coenzima A che svolge un ruolo importante nel metabolismo umano.
E poiché i suoi residui fissano i cationi metallici, sembra essere coinvolto in alcuni processi di contaminazione , bioconcentrazione e disintossicazione naturale dell'organismo ( chelazione di metalli pesanti o metalloidi tossici ).
Note e riferimenti
- massa molecolare calcolata da " Pesi atomici degli elementi 2007 " su www.chem.qmul.ac.uk .
- (in) Francis A. Carey, " Tabella di PK e valori di pH " , nel Dipartimento di Chimica della Università di Calgary , 2014(consultato il 26 luglio 2015 )
- (in) Mr Beals, L. Gross, S. Harrell, " Amino Acid Frequenza " su L'Istituto per la Modellistica Ambientale (ITSH) alla University of Tennessee (accessibile 26 luglio 2015 )
- " Cisteina (l-) " nel database dei prodotti chimici Reptox del CSST (organizzazione del Quebec responsabile per la sicurezza e la salute sul lavoro), accesso 25 aprile 2009
- Estratto del dizionario greco-francese A. Bailly, p. 520 .
- Terminologia medica di Georges Dolisi
- (in) Yannick Vallee , Ibrahim Shalayel , Dung Kieu- Ly e K. Raghavendra Rao , " Agli inizi della vita sulla Terra: l'ipotesi del mondo del peptide ricco di tiolo (TRP) " , International Journal of Developmental Biology , vol. 61, n osso 8-9,8 novembre 2017( ISSN 0214-6282 e 1696-3547 , letto online , consultato il 16 aprile 2018 )
- Cisteina sul sito GMO Compass.
- http://www.economie.gouv.fr/files/files/directions_services/dgccrf/boccrf/00_01/a0010016.htm Parere del Consiglio superiore di igiene pubblica della Francia relativo alla domanda di autorizzazione all'uso di L Cisteina dai capelli umani nel cibo umano].
- Direttiva 2010/69/UE della Commissione del 22 ottobre 2010 che modifica gli allegati alla direttiva 95/2/CE del Parlamento europeo e del Consiglio sugli additivi alimentari diversi dai coloranti e dagli edulcoranti .
- HMCOF SEABIRDS " Contaminazione da metalli pesanti di uccelli marini e focene nel Mare del Nord ;" Bollettino della Società Reale delle Scienze di Liegi 61 (1992): 163.)
- MOENNE, Alejandra. "Metallotioneine eucariotiche: proteine, regolazione genica e omeostasi del rame". Quaderni di biologia marina 42.1-2 (2001): 125-135.
Vedi anche
Articoli Correlati
link esterno
- (it) http://www.chemie.fu-berlin.de/chemistry/bio/aminoacid/cystein_en.html
- (in) natura idrofobica della cisteina.
- Studio pilota sulla tollerabilità dell'ingestione di un isolato proteico ricco di cisteina (Immunocal) nelle persone autistiche
Bibliografia
- Brattström, L., et al. " Omocisteina e cisteina: determinanti dei livelli plasmatici in soggetti di mezza età e anziani ". Journal of internal medicine 236.6 (1994): 633-641 ( abstract ).
- Qui, David. "Metabolismo della cisteina e tossicità dei metalli". Revisione della medicina alternativa 3 (1998): 262-270.
- Rhee, Sue Goo, et al. "Perossido di idrogeno: un messaggero chiave che modula la fosforilazione delle proteine attraverso l'ossidazione della cisteina". Science Signaling 2000.53 (2000): pe1-pe1 ( abstract ).
- Turk, Vito e Wolfram Bode. " Le cistatine: inibitori proteici delle cisteina proteinasi ". Lettere FEBS 285.2 (1991): 213-219.
- Turk, Vito, Boris Turk e Dušan Turk. "Proteasi della cisteina lisosomiale: fatti e opportunità". La rivista EMBO 20.17 (2001): 4629-4633 ( abstract ).
- Van Wart, Harold E. e Henning Birkedal-Hansen. " L'interruttore della cisteina: un principio di regolazione dell'attività delle metalloproteinasi con potenziale applicabilità all'intera famiglia di geni delle metalloproteinasi della matrice " . Atti della National Academy of Sciences 87.14 (1990): 5578-5582 abstract .