Potassio etilxantato
| Potassio etilxantato | |||
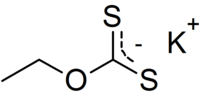
| |||
 | |||
| Identificazione | |||
|---|---|---|---|
| Nome sistematico | Potassio O-etilcarbonoditioato | ||
| N o CAS | |||
| N o ECHA | 100,004.946 | ||
| PubChem | 2735045 | ||
| SORRISI |
[K +] [S-] C (= S) OCC , |
||
| InChi |
Standard InChI: InChI = 1S / C3H6OS2.K / c1-2-4-3 (5) 6; / h2H2,1H3, (H, 5.6); / q; + 1 / p-1 Std. InChiave: JCBJVAJGLKENNC-UHFFFAOYSA-M |
||
| Aspetto | polvere gialla, odore sgradevole | ||
| Proprietà chimiche | |||
| Formula |
C 3 H 5 K O S 2 |
||
| Massa molare | 160,3 ± 0,013 g / mol C 22,48%, H 3,14%, K 24,39%, O 9,98%, S 40,01%, |
||
| Proprietà fisiche | |||
| T° fusione | 209 a 210 ° C ( decomposizione ) | ||
| solubilità | 1090 g · L -1 (acqua, 20 °C ) | ||
| Precauzioni | |||
| SGH | |||
  H228, H302, H315, H319, H332, H335, EUH018, P210, P260, P305 + P351 + P338,
H228 : Solido infiammabile
H228, H302, H315, H319, H332, H335, EUH018, P210, P260, P305 + P351 + P338,
H228 : Solido infiammabile H302 : Nocivo se ingerito H315 : Provoca irritazione cutanea H319 : Provoca grave irritazione oculare H332 : Nocivo se inalato H335 : Può irritare le vie respiratorie EUH018 : Durante l'uso può formare miscele vapore-aria infiammabili / esplosive P210 : Conservare lontano da calore/scintille/fiamme libere/superfici calde. - Vietato fumare. P260 : Non respirare la polvere/i fumi/i gas/la nebbia/i vapori/gli aerosol. P305 + P351 + P338 : In caso di contatto con gli occhi: sciacquare accuratamente con acqua per diversi minuti. Rimuovere le lenti a contatto se la vittima le indossa e possono essere facilmente rimosse. Continua a sciacquare. |
|||
| Trasporto | |||
40 : materiale solido infiammabile o autoreattivo o autoriscaldante Numero ONU : 3342 : XANTATI Classe: 4.2 Etichetta: 4.2 : Sostanze suscettibili di accensione spontanea  |
|||
| Ecotossicologia | |||
| DL 50 |
308 mg · kg -1 (topo, orale ) 199 mg · kg -1 (topo, iv ) 500 mg · kg -1 (topo, ip ) 1700 mg · kg -1 (ratto, orale ) |
||
| Unità di SI e STP se non diversamente indicato. | |||
Il potassio etil xantato è un composto organosulfuro della famiglia degli xantati (ditiocarbonati) di formula CH 3 CH 2 SCO 2 K. Viene utilizzato nell'industria mineraria come agente di flottazione per la separazione dei minerali . A differenza dell'etil xantato di sodio , il sale di potassio esiste allo stato anidro.
Proprietà
L'etilxantato di potassio si presenta sotto forma di una polvere gialla dall'odore sgradevole. È stabile a pH elevato, ma idrolisi rapidamente sotto pH 9, a 25 ° C . A differenza del suo equivalente di sodio, cristallizza in un sale anidro e non è igroscopico . L'etilxantato di potassio è un composto infiammabile. Si decompone a circa 210 °C , prima di poter fondere, liberando solfuro di carbonio , altamente infiammabile (punto di autoaccensione di 90 °C ).
Sintesi
L'etilxantato di potassio fu sintetizzato per la prima volta nel 1822 dal chimico danese William Christopher Zeise da idrossido di potassio , disolfuro di carbonio ed etanolo . Questo metodo è utilizzato ancora oggi: è la reazione tra un alcolato , qui etanolato, e solfuro di carbonio che produce uno xantato. L'alcolato è prodotto in situ , per reazione tra un alcol (qui etanolo), e una base forte (qui idrossido di potassio):
CH 3 CH 2 OH + CS 2 + KOH → CH 3 CH 2 OCS 2 K + H 2 OApplicazioni
L'etil xantato di potassio è utilizzato nell'industria mineraria come agente di flottazione per la separazione di minerali di rame , nichel e argento . Questo metodo sfrutta l'affinità di questi metalli “ morbidi ” con il legante organosolfuro.
Il potassio etil xantato è un utile reagente per la produzione di tiochetoni , per reazione con dicloruri, ma anche di esteri di xantato da alogenuri alchilici e arilici . Questi esteri sono quindi utili intermedi nella sintesi organica .
L'etilxantato di potassio è stato studiato come conservante , come reagente di precipitazione e in Giappone per l' estrazione liquido-liquido di tecnezio e renio .
Note e riferimenti
- (en) / (de) Questo articolo è parzialmente o interamente tratto da articoli intitolati in inglese " Potassium ethyl xanthate " ( vedere l' elenco degli autori ) e in tedesco " Kalium-O-ethyldithiocarbonat " ( vedere l' elenco degli autori ) .
- Voce "Potassium O-ethyl dithiocarbonate" nel database chimico GESTIS dell'IFA (ente tedesco responsabile per la sicurezza e la salute sul lavoro) ( tedesco , inglese ), consultato il 30 settembre 2019 (necessario JavaScript)
- massa molecolare calcolata da " Pesi atomici degli elementi 2007 " su www.chem.qmul.ac.uk .
- Gigiena Truda i Professional'nye Zabolevaniya. Igiene del lavoro e malattie professionali. Volo. 29 (11), Pag. 51, 1985.
- Chvapil M, Zahradnik R, Cmuchalova B., “ Influenza di alcoli e sali di potassio di acidi xantogenici su vari oggetti biologici. », Archives Internationales de Pharmacodynamie et de Therapie , vol. 135,febbraio 1962, pag. 330-343 ( PMID 13879442 )
- Domer FR, Schuler FW., “ Protezione dai raggi X di alcuni composti solfidrilici e dei loro precursori nei topi. », Archives Internationales de Pharmacodynamie et de Therapie , vol. 127,agosto 1960, pag. 128-131 ( PMID 13723622 )
- Gigiena i Sanitariya. Per la traduzione in inglese, vedere HYSAAV. Volo. 41 (6), Pag. 95, 1976.
- (de) Entry Kaliumditiocarbonate su Römpp Online . Georg Thieme Verlag, consultato il 30 maggio 2014.
- Charles C. Price e Gardner W. Stacy, p-nitrofenil) solfuro , Org. Sintet. 28 , col . "volo. 3",1948, 82 pag. , pag. 667
- Kathrin-Maria Roy, "Xanthates" , nell'Enciclopedia della chimica industriale di Ullmann , Weinheim,2005( DOI 10.1002 / 14356007.a28_423 )
- Alexander Schönberg e Emil Frese, “ Organische Schwefelverbindungen, LIV. Synthesen von Thiocarbonylverbindungen durch Einwirkung von Kaliumxanthogenat oder Thioharnstoffen auf gem. Dicloruro ”, Chemische Berichte , vol. 101, n . 2febbraio 1968, pag. 701–715 ( ISSN 0009-2940 , DOI 10.1002 / cber.19681010241 )
- Fabien Gagosz e Samir Z. Zard, un approccio di trasferimento di xantato alle α-trifluorometilammine , Org. Sintet. 84 , col . "volo. 11",1948, 32 pag. , pag. 212