Sostituzione elettrofila aromatica
La sostituzione elettrofila aromatica (o SEA o sear ) è una reazione organica in cui un atomo , solitamente di idrogeno , o un gruppo di atomi attaccati a un anello aromatico viene sostituito da un gruppo elettrofilo . Questa reazione, la principale nel gruppo delle sostituzioni elettrofile , è molto importante nella chimica organica , sia nell'industria che in laboratorio . Permette di preparare composti aromatici sostituiti da un'ampia varietà di gruppi funzionali secondo il bilancio:
ArH + EX → ArE + HXcon ArH un composto aromatico ed E un gruppo elettrofilo.
Meccanismo generale della reazione
Il primo passo del meccanismo è un'aggiunta durante il quale l' elettrofilo composto E + reagisce con un doppietto elettronico del dell'anello aromatico . Questo passaggio richiede generalmente la catalisi con un acido di Lewis . Questa aggiunta porta alla formazione di un cicloesadiénil carbocatico noto di Wheland intermedio (o complesso σ , o catione arenium ). Questo carbocatione è instabile, poiché corrisponde sia alla presenza di una carica sulla molecola sia ad una perdita di aromaticità . Viene comunque stabilizzata dal mesomerismo : la carica è in realtà delocalizzata su più atomi dell'anello aromatico.
Nella seconda fase, un atomo di idrogeno legato all'anello che ha subito l'aggiunta elettrofila esce come ione H + . Il doppietto elettronico utilizzato per il legame C-H permette quindi al sistema di ritrovare la sua aromaticità.
Principali sostituzioni elettrofile aromatiche
Questo capitolo descrive le principali sostituzioni aromatiche elettrofile utilizzate nell'industria e in laboratorio. Per ciascuno di essi viene fornito il meccanismo di reazione nel caso particolare del benzene . Questo meccanismo è simile per altri tipi di composti aromatici, ad eccezione delle condizioni operative ( temperatura , solvente, ecc.).
Nitrazione aromatica
La nitrazione aromatica è una particolare sostituzione elettrofila aromatica in cui un atomo di idrogeno legato ad un atomo di carbonio della anello aromatico è sostituito da nitro - N O 2 a forma nitrobenzene . L' elettrofilo utilizzato per la sostituzione è lo ione nitronio NO 2 + , prodotto in situ .
In pratica per effettuare la sostituzione, il benzene viene riscaldato a circa 50 ° C in una miscela di acido solforico e acido nitrico . Lo schema di reazione è il seguente:
(1) 2H 2 SO 4 + HNO 3 → 2HSO 4 - + NO 2 + + H 3 O +(2) C 6 H 6 + NO 2 + → C 6 H 5 NO 2 + H +(3) H + + H 3 O + + 2HSO 4 - → H 3 O + + H 2 SO 4 + HSO 4 -L'acido solforico agisce come una sorta di catalizzatore per la formazione dello ione nitronio. La reazione è possibile anche con acido nitrico da solo, ma poi è molto più lenta. Tra gli altri reagenti che possono essere utilizzati per la nitrazione aromatica, si può citare il tetrafluoroborato di nitronio NO 2 BF 4, che è un sale di nitronio ottenuto da acido fluoridrico , acido nitrico e trifluoruro di boro .
Se la reazione è catalizzata in presenza di acido solforico, la fase determinante la velocità era la nitrazione dell'anello benzenico per formare l' intermedio Wheland. In presenza del solo acido nitrico, questa è la formazione dello ione nitronio.
Il nitrobenzene formato durante questa reazione può in particolare essere utilizzato per produrre anilina mediante riduzione :
C 6 H 5 NO 2 + 3H 2 → C 6 H 5 NH 2Sulfonazione aromatica
La solfonazione aromatico è un particolare sostituzione elettrofila aromatica in cui un atomo di idrogeno legato ad un atomo di carbonio della anello aromatico è sostituito con un acido solfonico . Nel caso del benzene , la reazione forma acido benzensolfonico .
La sostituzione può essere effettuata in due modi:
- il benzene viene mantenuto a 25 ° C in un oleum , una soluzione di SO 3 in acido solforico (H 2 SO 4 ) o una miscela di SO 3 e acqua (con la maggioranza SO 3 ). I risultati della reazione sono:
- il benzene viene riscaldato in acido solforico concentrato . La SO 3 viene quindi formata in situ per reazione dell'acido solforico su se stesso. I risultati della reazione sono:
In entrambi i casi, il meccanismo di reazione è il seguente:

Per la solfonazione, la rimozione dell'atomo di idrogeno avviene mediante una reazione intramolecolare .
Questa reazione non ha una fase cineticamente determinante .
Questa è una reazione reversibile: è possibile rimuovere il gruppo dell'acido solfonico e rigenerare il benzene riscaldando l'acido benzensolfonico in una soluzione diluita di acido solforico in acqua surriscaldata. I risultati sono:
C 6 H 5 SO 3 H + H 2 O(vapore) → C 6 H 6 + HSO 4 - + H 3 O +L'acido benzensolfonico formato durante questa reazione è un importante intermedio sintetico nell'industria, utilizzato ad esempio nella fabbricazione di coloranti e prodotti farmaceutici . Inoltre, è possibile ridurlo in presenza di idrossido di sodio fuso per formare fenolo .
Alogenazione aromatica
L' alogenazione aromatica è la sostituzione elettrofila aromatica in cui un atomo di idrogeno legato ad un atomo di carbonio della anello aromatico è sostituito da un membro di alogeno secondo la seguente valutazione:
C 6 H 6 + X 2 → C 6 H 5 X + HXLa reazione non è spontanea, ma richiede la presenza di un catalizzatore di tipo acido di Lewis . Viene quindi eseguito in un mezzo anidro . È possibile senza un catalizzatore (ma è poi lento) nel caso di cicli attivati, come il fenolo . L'alogenazione aromatica consente di sostituire un atomo di idrogeno con un atomo di cloro , bromo o iodio . D'altra parte, non è possibile con il fluoro . Si tratta infatti di un potente ossidante che provoca la degradazione del composto aromatico. Il meccanismo di reazione è il seguente (esempio nel caso della clorazione ):

Durante la prima fase del meccanismo, l'acido di Lewis usato come catalizzatore forma un complesso con il cloro , che rende polarizzato il legame Cl-Cl . Uno dei due atomi di cloro diventa quindi elettrofilo, e può subire un attacco nucleofilo dal ciclo aromatico, portando così alla formazione dell'intermedio di Wheland. L' anione formatosi contribuisce poi nella seconda fase all'eliminazione dell'atomo di idrogeno e al ripristino dell'aromaticità .
Il catalizzatore utilizzato è generalmente costituito dallo stesso elemento alogeno di quello che agisce nella sostituzione. Gli acidi di Lewis più comunemente utilizzati sono quindi il cloruro di zinco ZnCl 2 , il cloruro di alluminio AlCl 3 e il cloruro di ferro (III) FeCl 3 nel caso della clorazione e il bromuro di ferro (III) FeBr 3 nel caso della bromurazione . Nel caso dello iodio, il meccanismo di reazione è leggermente diverso. In effetti, il diodo I 2 è troppo poco reattivo. Deve prima reagire con un ossidante (ad esempio l'acido nitrico ) per formare il catione I + , elettrofilo , che interviene nella iodurazione .
Gli alogeni sono elementi debolmente disattivanti per il ciclo aromatico. Di conseguenza, se la reazione è catalizzata e l'alogeno è presente in eccesso , possono verificarsi polisostituzioni.
Reazioni di Friedel-Crafts
Le reazioni di Friedel-Crafts sono particolari sostituzioni aromatiche elettrofile in cui un anello aromatico è alchilato (sostituzione di un atomo di idrogeno con un gruppo alchile ) o acilato (sostituzione di un atomo di idrogeno con un gruppo acile ).
AlchilazioneL' alchilazione di Friedel-Crafts è una reazione per l' alchilazione di un composto aromatico. Questa reazione richiede la catalisi con un acido di Lewis .
AcilazioneIl Friedel-Crafts è una reazione di acilazione di un composto aromatico. Come l'alchilazione, richiede la catalisi da parte di un acido di Lewis . I principali catalizzatori utilizzati sono il cloruro di alluminio AlCl 3 e il bromuro di alluminio AlBr 3 . C'è generalmente più bisogno di catalizzatore rispetto alle quantità stechiometriche , perché si complessa con il prodotto formato, da qui la necessità di idrolisi dopo la reazione per distruggere il complesso.
Altre sostituzioni
Reazione di Kolbe-Schmitt
La reazione di Kolbe-Schmitt (o processo Kolbe ) è una reazione di carbossilazione sviluppata da A. Kolbe e R. Schmitt. Durante questa sostituzione elettrofila aromatica del fenolato di sodio ( sale del fenolo ) è stato riscaldato a 125 ° C in presenza di anidride carbonica sotto una pressione di 100 atm , e quindi trattato con l' acido solforico . I risultati della reazione sono i seguenti:
C 6 H 5 OH + CO 2+ NaOH + H 2 SO 4 → C 6 H 4 OHCOOH + HSO 4 - + H 2 O+ Na +Durante la prima fase (non in figura), i fenoli reagisce con l'idrossido di sodio per formare fenolato di sodio e HO - ioni . Il fenolato reagisce quindi con l' anidride carbonica mediante sostituzione elettrofila aromatica, il centro elettrofilo qui è l'atomo di carbonio di CO 2. Gli ioni HO - formati durante la prima fase assistono al ripristino dell'aromaticità. Il composto ottenuto è la base coniugata di acido carbossilico , l'ultimo passaggio consiste in una reazione acido-base con acido solforico.
Il prodotto ottenuto durante questa reazione è un acido β-idrossilato (en) aromatico [qui acido salicilico , precursore dell'aspirina ( acido acetilsalicilico )].
Reazioni con anelli aromatici già sostituiti: polisostituzioni
Il prodotto di una reazione di sostituzione elettrofila aromatica è esso stesso un composto aromatico : la rimozione di un atomo di idrogeno ripristina l' aromaticità dell'intermedio di Wheland (l' intermedio di carbocatione ). Non c'è quindi nulla che impedisca a questo prodotto, che è un anello aromatico sostituito, di subire nuovamente una sostituzione elettrofila aromatica, purché vi siano atomi di idrogeno legati ad atomi di carbonio. In realtà, tutti i composti aromatici sostituiti non potranno subire una nuova sostituzione aromatica elettrofila, e il prodotto risultante da una seconda reazione dipende dal prodotto di partenza: il gruppo presente sul composto sostituito di partenza influenza sia la reattività di questo composto (può o meno subire una seconda sostituzione), così come la regioselettività della reazione (non si formano tutti i prodotti possibili).
Reattività alla polisostituzione
Il gruppo presente sul composto sostituito di partenza influenza fortemente la sua reattività. Questi gruppi sono classificati in due categorie: gruppi di attivazione e gruppi di disattivazione . Un composto aromatico sostituito con un gruppo attivante è quindi più reattivo del composto aromatico non sostituito. Al contrario, un composto aromatico sostituito con un gruppo disattivante è meno reattivo . Queste regole furono stabilite dal chimico olandese Arnold F. Holleman nel 1910 , sono conosciute come regole Holleman .
Attivazione di gruppiUn gruppo attivante è un gruppo la cui presenza aumenta la reattività dell'anello aromatico rispetto alla sostituzione elettrofila aromatica rispetto all'anello per cui questo gruppo è assente. La sostituzione di un anello aromatico non sostituito con un gruppo attivante spesso si traduce in polisostituzione. La reattività dell'anello aromatico aumenta se è richiesta meno energia per passare dal composto di partenza all'intermedio di reazione (intermedio di Wheland), in altre parole se la differenza di energia tra il composto di partenza e l'intermedio di reazione è più debole. Questo è particolarmente vero per i composti donatori mesomerici , come il gruppo idrossile —OH . La figura seguente mostra la stabilizzazione mediante mesomeria del fenolo e del corrispondente intermedio di Wheland:

Sia il fenolo che l'intermedio di Wheland sono stabilizzati dal mesomerismo delocalizzando gli elettroni dall'anello aromatico. Inoltre, è possibile scrivere formule mesomeriche che coinvolgono un doppietto elettronico dell'atomo di ossigeno . Nel caso del fenolo, queste forme mesomeriche mostrano cariche formali sull'ossigeno e un atomo di carbonio, quindi inducono solo una debole stabilizzazione. Al contrario, nel caso dell'intermediario Wheland, non appare alcun carico aggiuntivo: la stabilizzazione è importante. L'intermedio di Wheland è quindi più stabilizzato del fenolo dalla presenza del gruppo -OH .
Questa situazione è riassunta nella figura a fianco, confrontata con il benzene ( anello aromatico non sostituito). Gli stati fittizi (linee tratteggiate) corrispondono ad una situazione in cui la presenza del gruppo -OH sarebbe neutra, cioè una situazione in cui non intervenirebbe tramite i doppietti trasportati dall'ossigeno. In questo caso, l'energia del fenolo e dell'intermedio di Wheland sarebbe la stessa del benzene. Le linee continue corrispondono alla situazione reale: l'intermedio di Wheland è più stabilizzato del fenolo (la sua energia è ridotta). Di conseguenza, la differenza di energia tra il fenolo e l'intermedio di Wheland Δ E 2 è minore di questa differenza nel caso del benzene Δ E 1 . Il fenolo è quindi più reattivo del benzene rispetto alla sostituzione elettrofila aromatica.
Complessivamente, tutti i gruppi che possono stabilizzare la carica positiva dell'intermedio di Wheland, sia per mesomerismo che per effetto induttivo , sono gruppi attivatori , e quindi i gruppi mesomerici donatori e donatori induttivi.
Disattivazione dei gruppiUn gruppo disattivante è un gruppo la cui presenza diminuisce la reattività dell'anello aromatico rispetto alla sostituzione elettrofila aromatica rispetto all'anello per cui questo gruppo è assente. La sostituzione di un anello aromatico non sostituito con un gruppo disattivante porta solo molto raramente alla polisostituzione. La reattività dell'anello aromatico diminuisce se è richiesta più energia per passare dal composto di partenza all'intermedio di reazione (intermedio di Wheland), in altre parole se la differenza di energia tra il composto di partenza e l'intermedio di reazione è più importante. Questo è particolarmente il caso dei composti di ritiro mesomerici , come il gruppo nitro -NO 2 . La figura seguente mostra la stabilizzazione mesomerica del nitrobenzene e del corrispondente intermedio di Wheland:
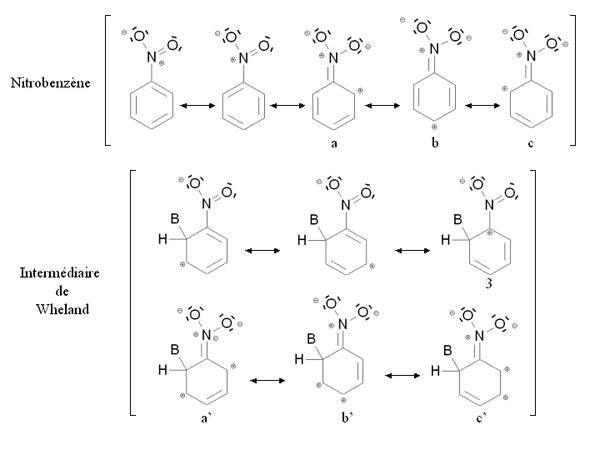
Sia il nitrobenzene che l'intermedio di Wheland sono stabilizzati mesomericamente dalla delocalizzazione degli elettroni dall'anello aromatico. Tuttavia, nel caso della forma mesomerica 3 dell'intermedio di Wheland, l'atomo di carbonio legato al gruppo nitro (altamente elettronegativo ) è caricato positivamente. Questa forma mesomerica è quindi molto poco stabilizzante: l'intermedio di Wheland è meno stabilizzato del nitrobenzene, e la presenza del gruppo nitro induce una destabilizzazione rispetto a una situazione in cui sarebbe assente. Inoltre, è possibile scrivere formule mesomeric coinvolgono un doppietto elettronico del azoto atomo ( un , b , c ed un ' b' , c ' ). Tuttavia, nel caso del b ' e c' mesomeric forme di Wheland intermedia, due cariche positive sono portate da atomi di carbonio comune, che corrisponde ad una configurazione molto instabile. Anche in questo caso, l'intermedio di Wheland è meno stabilizzato del nitrobenzene.
Questa situazione è riassunta nella figura a fianco, confrontata con il benzene ( anello aromatico non sostituito). Gli stati fittizi (linee tratteggiate) corrispondono a una situazione in cui il gruppo -NO 2 non interviene tramite i doppietti trasportati dall'azoto. Lo stato fittizio dell'intermedio di Wheland è destabilizzato rispetto al benzene (a causa di una carica positiva nella formula mesomerica 3 ). D'altra parte, il nitrobenzene non è destabilizzato rispetto al benzene. Le linee continue corrispondono alla situazione reale: l'intermedio di Wheland è meno stabilizzato del nitrobenzene (la sua energia si abbassa di meno) a causa delle cariche trasportate dagli atomi di carbonio congiunti nelle formule mesomeriche b ' e c' . Di conseguenza, la differenza di energia tra il nitrobenzene e l'intermedio di Wheland Δ E 2 è maggiore di questa differenza nel caso del benzene Δ E 1 . Il nitrobenzene è quindi meno reattivo del benzene rispetto alla sostituzione elettrofila aromatica.
A livello globale, vengono disattivati tutti i gruppi che possono destabilizzare la carica positiva dell'intermedio di Wheland, sia per mesomerismo che per effetto induttivo , quindi i gruppi attrattivi mesomerici e attrattori induttivi.
Valutazione: reattività relativa di alcuni composti sostituitiLa reattività di un composto aromatico sostituito rispetto ad una nuova sostituzione elettrofila aromatica dipende quindi fortemente dalla natura del sostituente già presente. La reattività è tanto maggiore quanto il sostituente porta gli elettroni nel sistema e stabilizza le cariche positive ( effetto mesomerico donatore ed effetto induttivo donatore). La tabella sottostante fornisce quindi alcuni ordini di grandezza di reattività (relativa a quella del benzene , fissata a 1) di alcuni benzeni sostituiti. Il fenolo è quindi 1000 volte più reattivo del benzene e il nitrobenzene 10.000 volte meno.
| Sostituto | -N (CH 3 ) 2 | -OH | -CH 3 | - H | -Cl | -COOH | -NO 2 |
| Reattività | 9.000.000 | 1000 | 25 | 1 | 0.3 | 4,10 × 10 −3 | 1,10 × 10 −4 |
Regioselettività
Quando un composto aromatico sostituito subisce una seconda sostituzione aromatica elettrofila, l'attacco può avvenire a priori da cinque posizioni. Tra queste posizioni, due sono posizioni orto , due sono meta posizioni e una posizione para (vedi figura a destra).
A prima vista, si potrebbe quindi pensare che il prodotto di reazione sia una miscela composta dal 40% di orto isomero , 40% di meta isomero e 20% di para isomero, secondo una distribuzione statistica ( 2 - 2 - 1 ). In realtà non è affatto così e la regioselettività della reazione (quindi la natura del prodotto finale) dipende fortemente dal gruppo già presente sull'anello aromatico sostituito. A seconda della natura di questo gruppo, la seconda sostituzione può essere eseguita quasi esclusivamente in meta , o secondo una miscela orto + para .
Gruppi di orientamento ortho-paraSperimentalmente, una sostituzione elettrofila aromatica utilizzando come prodotto di partenza un anello aromatico sostituito da un gruppo donatore ( mesomero donatore o donatore induttivo ) si traduce in una miscela di isomeri orto e para, con una quantità molto piccola di meta isomero. Questo risultato è spiegato da semplici considerazioni energetiche.
Per passare dal composto di partenza a un intermedio di reazione in una reazione chimica , è necessario fornire energia per attraversare una potenziale barriera . La velocità della reazione è tanto maggiore quanto questa barriera è debole, e quindi quanto l'intermedio di reazione è stabile. Nel caso della sostituzione elettrofila aromatica, si può considerare con buona approssimazione che il prodotto finale formato più velocemente è quello in cui si forma più velocemente l'intermedio di Wheland (reazione sotto controllo cinetico). Deve quindi corrispondere all'intermediario Wheland più stabile.
La figura a destra mostra gli intermedi di Wheland corrispondenti ai composti orto, meta e para nel caso in cui il prodotto di partenza sia il fenolo (mesomero donatore). In tutti e tre i casi, l'intermedio di Wheland viene stabilizzato dal mesomerismo riposizionando la carica positiva su tre atomi di carbonio . Nel caso dei composti orto e para, la carica è stabilizzata anche dal mesomerismo che coinvolge un doppietto elettronico dell'atomo di ossigeno . Questi due intermedi sono quindi notevolmente più stabili del meta intermedio e la reazione dà come risultato una miscela costituita principalmente dagli isomeri orto e para.
Nel complesso, un gruppo di donatori (mesomero donatore o donatore induttivo) è quindi orto-para-orientatore. Se questo gruppo è molto grande, il composto finale è prevalentemente para (le posizioni orto sono di difficile accesso). Al contrario, se è debolmente voluminoso, l'orto composto è statisticamente favorito (due posizioni orto per una singola posizione para). Così, ad esempio, la nitrazione del toluene (φ-CH 3 ) porta ad una miscela di isomeri orto (60%), para (37%) e meta (2%) (il sostituente è poco voluminoso), mentre la nitrazione di anisolo (φ-O-CH 3 ) porta a una miscela di isomeri orto (34%), para (65%) e meta (1%) (il sostituente è relativamente voluminoso).
Gruppi meta-referralSperimentalmente, una sostituzione elettrofila aromatica che utilizza come prodotto di partenza un anello aromatico sostituito da un gruppo ritirante ( ritiro mesomero o ritiro induttivo induttivo ) porta principalmente al meta isomero, con una piccola quantità di isomeri orto e para.
Come nel caso dei gruppi di orientamento orto-para, questo risultato è spiegato da semplici considerazioni energetiche ragionando sulla stabilità dell'intermedio di Wheland. La figura a destra mostra gli intermedi di Wheland corrispondenti ai composti orto, meta e para nel caso in cui il prodotto di partenza è nitrobenzene (mesomero ritirante). In tutti e tre i casi, l'intermedio di Wheland viene stabilizzato dal mesomerismo riposizionando la carica positiva su tre atomi di carbonio . Il gruppo nitro essendo un attrattore, non stabilizza mai la carica positiva dal mesomerismo. Per una delle forme mesomeriche di orto e para intermedi, l'atomo di carbonio legato al gruppo nitro trasporta una carica positiva. Essendo il gruppo nitro molto elettronegativo , questa situazione è molto instabile e questa forma mesomerica difficilmente si sta stabilizzando. Gli intermedi orto e para sono quindi meno stabili del meta intermedio, che si forma quindi più rapidamente.
Nel complesso, un gruppo attrattore (mesomero attrattore o attrattore induttivo) è quindi meta-orientatore. Così, ad esempio, una seconda nitrazione di nitrobenzene porta al 92% di meta isomero, al 7% di orto e all'1% di para.
Casi speciali di alogeniGli alogeni (specialmente cloro , bromo e iodio ) sono un caso speciale, essendo sia attrattori di donatori debolmente debolmente induttivi che mesomerici. Questi gruppi si disattivano debolmente (il clorobenzene è circa tre volte meno reattivo del benzene ) ma si orienta verso l'orto-para.
Tabella riassuntiva
In sintesi, i gruppi donatori si stanno attivando (la reattività è maggiore) e si orientano orto-para, mentre i gruppi in ritiro si stanno disattivando e meta-orientando. Come regola generale, l'effetto di attivazione o disattivazione è tanto più importante in quanto il gruppo è più donatore o attrattore. La tabella seguente elenca gli effetti sulla reattività e sulla regioselettività di alcuni gruppi di uso frequente.
| Attivazione | Disattivazione | |
|---|---|---|
| Potente | -O - , -OH ortho-para orienters |
-NO 2 , -NR 3 + (dove R = H o alchile ), -CCl 3 , -CF 3 meta orientatori |
| Si intende | -OR, -NH-CO-R (dove R = alchil ) orto-para-orientatori |
-CN, -SO 3 H, -COOR, -CO-R (dove R = H o alchile ) metaorientatori |
| Basso |
alchili , arili orto-para orientatori |
orto-para alogeni orientanti |
Sostituzioni che coinvolgono composti eterociclici
L' eterociclico aromatico , come il furano , il pirrolo o la piridina , può anche reagire per sostituzione aromatica elettrofila. Il loro comportamento rispetto alle polisostituzioni (reattività e regioselettività) è determinato dalle stesse considerazioni energetiche dell'esempio del benzene .
Riferimenti
- GW Wheland, A Quantum Mechanical Investigation of the Orientation of Substituents in Aromatic Molecules , J. Am. Chem. Soc. , 1942, 64 (4), p. 900-908 , DOI : 10.1021 / ja01256a047 .
- (de) H. Kolbe, Annalen der Chemie und Pharmacie , n . 113, 1860, p. 125 .
- (de) R. Schmitt, "Beitrag zu Kenntniss der Kolbe'schen Salicylsäure-Synthese". In Advanced Synthesis & Catalysis , n . 31, [2], 1885, p. 397 testo sulla Gallica .
- Peter Vollhardt, Trattato di chimica organica , cap. 15-8 .