Incontinentia pigmenti
| Incontinentia pigmenti | ||
 Incontinentia pigmenti sotto l'ascella di una bambina di tre anni. Le "macchie" adottano le linee di Blaschko . | ||
| Riferimento MIM | 308300 | |
|---|---|---|
| Trasmissione | Geneticamente | |
| Cromosoma | X | |
| Numero di casi | 700 | |
| Elenco delle malattie genetiche con gene identificato | ||
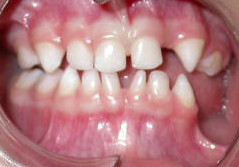 La dentatura rivela l'assenza dei denti 62, 74 e 75. I denti 71 e 82 hanno qui forme coniche.
La dentatura rivela l'assenza dei denti 62, 74 e 75. I denti 71 e 82 hanno qui forme coniche.
| Specialità | Genetica medica |
|---|
| CISP - 2 | S83 |
|---|---|
| ICD - 10 | Q82.3 |
| CIM - 9 | 757.33 |
| OMIM | 308300 |
| Malattie DB | 29600 |
| MedlinePlus | 001583 |
| eMedicine | 1176285 |
| eMedicine | articolo / 1114205 articolo / 1176285 |
| Maglia | D007184 |
| GeneReviews | [1] |
L' Incontinentia pigmenti (IP) o sindrome di Bloch-Sulzberger , è una malattia genetica raramente chiamata ereditaria di tipo "orfano" , che colpisce principalmente la pelle, i denti, gli occhi e il sistema nervoso centrale . Il suo nome deriva dalle anomalie osservate nella pelle all'esame microscopico (incontinenza da pigmento ).
Non deve essere confuso con Ito ipomelanosi (HI), precedentemente chiamata incontinentia pigmenti acromici i cui sintomi sono simili.
L' incontinenza pigmenti è causata da un deficit del gene nemo che codifica per la proteina NEMO (per NF-kappa B Essential Modulator) che è una subunità regolatrice della protein chinasi (IKK) coinvolta nei fattori di trascrizione della via del segnale ; questa proteina controlla quindi normalmente la moltiplicazione cellulare e la risposta immunitaria e infiammatoria limitando la mortalità cellulare ( apoptosi ) nei tessuti interessati; tuttavia la sua assenza provoca anche la degenerazione dei tessuti per apoptosi.
La malattia può manifestarsi per mutazione del gene nemo , nelle ragazze e raramente nei ragazzi.
Il nemo gene è dominante e legato al cromosoma X . La malattia viene ereditata solo dalle ragazze perché i feti maschi che l'hanno ereditata non sopravvivono.
Storico
La malattia è stata segnalata per la prima volta dal dermatologo svizzero Bruno Bloch nel 1926 e poi dal dermatologo americano Marion Suzberger nel 1928. Il gene nemo è stato scoperto nel 1998.
Epidemiologia
Una persona su 143.000 ne è colpita. Più del 50% dei casi segnalati è dovuto a mutazioni de novo .
Complessivamente (ereditarietà + caso de novo ), l' incontinenza pigmenti colpisce principalmente le femmine (95% dei casi) ma può colpire anche i maschi.
Nel 5% dei casi il feto maschio può essere affetto da mutazione (più o meno tessuto è interessato a seconda dello stadio di sviluppo in cui avviene la mutazione) e viene eliminato naturalmente. Esistono tuttavia delle eccezioni corrispondenti al cariotipo "47, XXY" o alla Sindrome di Klinefelter dove la gravidanza è portata a termine; questi ragazzi (individui “a mosaico”) non trasmettono la malattia ai loro ragazzi ma possono o meno trasmetterla alle loro figlie a seconda che i loro tessuti riproduttivi siano o meno colpiti. Per scoprirlo, devi fare un'analisi genetica dello sperma . I sintomi sperimentati dai ragazzi mutanti differiscono in modo significativo da quelli delle ragazze, con conseguente riconoscimento tardivo della prevalenza della malattia nei ragazzi.
Le figlie di madri surrogate hanno una possibilità su due di essere colpite dalla malattia; i feti maschi affetti (50% dei ragazzi) non sono vitali e vengono eliminati naturalmente. Per rilevare la malattia in queste ragazze, è possibile prelevare un campione in utero per determinare se il feto ha ereditato il gene o meno, a tre mesi ( diagnosi prenatale ).
Fisiopatologia
L'incontinentia pigmenti è causata da una mutazione nel gene NEMO (Xq28). Questo gene si trova sul cromosoma X , la trasmissione di questa malattia è dominante e chiamata "legata all'X". La mutazione, la cui entità è variabile (il gene è più o meno danneggiato) influisce sulla produzione della proteina Nemo coinvolta come regolatore del sistema NF-κB , il cui preciso funzionamento è scarsamente compreso. Inoltre, il fenomeno di inattivazione del cromosoma X o di lionizzazione nelle femmine provoca un interessamento casuale dei tessuti (danno a mosaico ). La diagnosi prenatale può rilevare la malattia ma non prevedere mai la gravità è molto variabile.
La malattia porta alla degenerazione di tessuti come la pelle e i vasi sanguigni nella parte posteriore dell'occhio e talvolta nel cervello, in questo caso con conseguenze potenzialmente gravi ( convulsioni , handicap mentale , ecc.).
È la causa di anomalie del sistema pilare (aree prive di pelo) e delle unghie .
La pelle è in gran parte autoriparante eliminando le cellule colpite dopo alcuni mesi se il soggetto viene mantenuto in buone condizioni igieniche (vedi Esame clinico ). La formula dentale viene spesso modificata: alcuni denti mancano e altri hanno una forma conica (vedi foto). Il danno causato ai denti può essere ridotto dall'ortodonzia . Quelli causati agli occhi e al cervello sono irreversibili. È necessario un follow-up oftalmologico , può aiutare a prevenire aggravamenti come il distacco di retina .
Si noti che il 41% dei pazienti non ha danni alla retina, il 7% ha una miopia elevata e il 43% ha strabismo .
Diagnostico
Oltre alla diagnosi prenatale, in alcuni paesi viene presa in considerazione la diagnosi preimpianto. Queste diagnosi si basano sull'identificazione del gene NEMO. La diagnosi dopo la nascita si basa sull'esame obiettivo e dovrebbe essere fatta alla nascita, se possibile
Segni funzionali
Esame fisico
L'esame della pelle alla nascita è essenziale perché le lesioni sono presenti alla nascita o nei primi 15 giorni nel 90% delle ragazze affette.
Lesioni cutanee presenti in quattro fasi:
- stadio vescicolobolloso: macchie rosse leggermente rialzate (aree di pelle più o meno ampie) pruriginose ricoperte da vescicole e bolle (vesciche) molto spesso presenti dalla nascita;
- stadio papuloverruquous: comparsa di lesioni simili a verruche (comparsa di verruche più o meno gravi) e licheni sulle mani e sui piedi all'età di 2-5 mesi; questo attacco cessa alla fine dei primi mesi e di solito lascia poco effetto collaterale
- fase pigmentata: questa pigmentazione assume l'aspetto di schizzi o getti d'acqua. Può essere osservato alla nascita nel 5-10% dei pazienti, ma il più delle volte si verifica solo tra i sei ei dodici mesi di vita;
- stadio atrofico: l'atrofia (assottigliamento della pelle) si verifica prima della regressione dell'iperpigmentazione. Assume l'aspetto negli adolescenti e negli adulti di band più leggere e non impilate. Sono più visibili sul cuoio capelluto o dietro i polpacci. Generalmente, in età adulta, il coinvolgimento cutaneo è quasi completamente scomparso e può persino passare del tutto inosservato se non indagato attentamente.
Si osservano anche manifestazioni extracutanee, soprattutto oftalmologiche (anomalie vascolari retiniche, distacco di retina, ecc. ) Dentali (anodonzia parziale, denti conici, allineamento anomalo), sulle unghie e neurologiche (ritardo mentale, convulsioni, ecc .).
L'esame della pelle consente la diagnosi. La prima comparsa di vescicole e pustole simili a quella della varicella si osserva sulla pelle delle femmine appena nate.
Test aggiuntivi
Ulteriori esami includono un follow-up oftalmico per valutare il danno retinico, se applicabile. Si raccomanda il follow-up: immediatamente dopo la nascita, mensilmente fino a quattro mesi, ogni tre mesi fino a un anno e due volte all'anno fino all'età di tre anni.
Si possono osservare diversi cambiamenti retinici, spesso asimmetrici. Iniziano nelle prime settimane dopo la nascita e progrediscono nel corso dei mesi:
- grado 1: cambiamento nell'epitelio pigmentato, pigmentato o meno con screziature;
- grado 2: vascolarizzazione o meno di una cresta temporale, con o senza trazione retinica o vitreale, gliosi o fibrosi, talvolta avascolare alla periferia della cresta;
- grado 3: distacco della retina e membrana retrocristallina.
Supportato
Non sono disponibili cure mediche. A seconda degli effetti sul corpo del paziente (denti, occhi, ecc. ) Ci sono solo trattamenti locali (ortodonzia, correzione laser, ecc. ); per i problemi della pelle come zone di alopecia o tracce di "schizzi" sui polpacci, al momento non esiste alcun trattamento.
Associazioni IP
L'organizzazione IPIF (International Incontinentia Pigmenti Foundation) è stata fondata nel 1995; il consorzio IP consente scambi tra scienziati o medici provenienti da Francia, Italia, Regno Unito, Germania, Stati Uniti.
Un'associazione francese "Incontinentia Pigmenti France" offre ai pazienti e alle famiglie di rompere l'isolamento, raggrupparsi e diffondere informazioni. Non esiste un'associazione simile in Belgio.
Evoluzione e complicazioni
Consulenza genetica
Note e riferimenti
- (it) Kitakawa D., Fontes PC, Magalhães FA, Almeida JD e Cabral LA, “ incontinentia pigmenti presenta come ipodonzia in una bambina di 3 anni: un caso clinico ” , J. Med. Case Rep. , n o 3,2009, p. 116 ( PMID 19946534 , DOI 10.1186 / 1752-1947-3-116 , leggi in linea ).
- Gilles Courtois, " Nuove funzioni di NEMO, la subunità regolatoria della chinasi attivazione di NF-kB " , su Med.Sci (Parigi) ,Novembre 2008(accesso 8 ottobre 2019 )
- (in) " Dermatosi del pigmento di Bloch-Sulzberger " su whonameit (accesso 8 ottobre 2019 )
- " incontinentia pigmenti " , su orpha.net ,settembre 2013(accesso 8 ottobre 2019 )
- (in) Gupta KD Padhiar BB Karia UK e Shah BJ, " Casi posticipati di Incontinentia Pigmenti nei maschi " , Indian J. Dermatol. , vol. 58, n o 4,2013, p. 328 ( PMID 23919034 , DOI 10.4103 / 0019-5154.113998 , leggi in linea ).
- (en) Vanessa Ngan, " Incontinentia pigmenti " , su Derm.net NZ ,2016(accesso 8 ottobre 2019 )
- " IPIF " da IPIF (accede 8 Ottobre 2019 ).
- " Incontinentia pigmenti France " , su incontinentia-pigmenti.fr .
Articoli Correlati
link esterno
- Incontinentia pigmenti , Orphanet