Bicarbonato
| Bicarbonato | |
 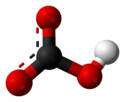 Struttura dello ione bicarbonato. |
|
| Identificazione | |
|---|---|
| Nome IUPAC | carbonato di idrogeno |
| N o CAS | |
| PubChem | 769 |
| ChEBI | 17544 |
| SORRISI |
C (= O) (O) [O-] , |
| InChI |
Std. InChI: InChI = 1S / CH2O3 / c2-1 (3) 4 / h (H2,2,3,4) / p-1 Std. InChIKey: BVKZGUZCCUSVTD-UHFFFAOYSA-M |
| Proprietà chimiche | |
| Formula bruta | HCO 3 |
| Massa molare | 61,0168 ± 0,0018 g / mol C 19,68%, H 1,65%, O 78,66%, |
| Unità di SI e STP se non diversamente specificato. | |
Il bicarbonato o idrogeno , è uno ione poliatomico la cui formula chimica è H C O 3 - . Il bicarbonato deve il suo prefisso (“bi-”) al suo doppio carattere acido-base (detto carattere anfotero ): è sia acido che base, appartenente a due differenti coppie acido-base. Questa è la forma intermedia nella doppia deprotonazione di acido carbonico : rimozione del primo protone ( H + ione ) di acido carbonico dà bicarbonato; la rimozione del secondo protone darà la forma di carbonato ionico.
La parola è scritta al plurale (bicarbonati) quando si parla di sali dello ione bicarbonato: ad esempio, bicarbonato di sodio (spesso chiamato "bicarbonato di sodio" per abuso di linguaggio, o "bicarbonato di sodio" e "mucca" in Canada ) con la formula NaHCO 3 , che è il sale più comune e ampiamente utilizzato dello ione bicarbonato. Contribuisce alla digestione del nostro corpo.
Proprietà
In acqua, anidride carbonica , acido carbonico , ione bicarbonato e ione carbonato sono in equilibrio , a seconda del pH :
CO 2+ H 2 O H 2 CO 3 H + + HCO 3 - 2 H + + CO 3 2–.L'aggiunta di un acido sposta gli equilibri a sinistra (con possibile rilascio di anidride carbonica), mentre l'aggiunta di una base li sposta a destra (con, facoltativamente, precipitazione di un sale carbonato.).
Applicazioni
La trasformazione parziale dei bicarbonati in contatto con acidi (come l' acido acetico dal aceto ) in anidride carbonica gas viene utilizzato in cottura per consentire pane a salire, e quando la propulsione di razzi giocattoli.
Biologia umana
Standard
Concentrazione di bicarbonato nel sangue è compresa tra 22 e 26 mmol / L .
Soluzione tampone
La natura anfotera del bicarbonato (il suo posto intermedio nell'equilibrio), gli fa svolgere un ruolo tampone . Questa funzione tampone bicarbonato esiste in particolare nel sangue , con un ruolo molto importante nel mantenimento del pH (cfr. Omeostasi ).
Molti organi sono coinvolti nella regolazione del livello dei bicarbonati, e quindi del pH: principalmente i polmoni (attraverso l'eliminazione dell'anidride carbonica ) ei reni . Interviene anche l'apparato digerente, attraverso la secrezione del succo gastrico acido (sotto il controllo della secretina ) e dei sali biliari prodotti dal fegato e secreti nella bile .
Attivazione degli enzimi digestivi
La funzione esocrina del pancreas produce, tramite anidrasi carboniche , ioni bicarbonato HCO 3 - che vengono scaricati nel duodeno per neutralizzare l'acidità del chimo e quindi attivare gli enzimi intestinali e gli enzimi pancreatici prodotti da questa stessa funzione.
Altre funzioni
Il bicarbonato è utilizzato nella sintesi dell'uracile monofosfato (UMP), un precursore delle basi pirimidiniche nel DNA .
È anche coinvolto nella capacità degli spermatozoi durante la fecondazione.
Note e riferimenti
- massa molecolare calcolata dal " peso atomico degli elementi 2007 " su www.chem.qmul.ac.uk .
- Webmaster Cuen, " Capitolo intero. Disturbi dell'equilibrio acido-base - [manuale di nefrologia n ° 7] ” , su cuen.fr (consultato il 2 dicembre 2018 ) .
