Miastenia grave
Miastenia grave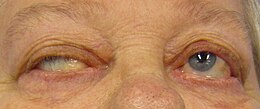 Ptosi in una persona con miastenia grave che cerca di aprire gli occhi.
Ptosi in una persona con miastenia grave che cerca di aprire gli occhi.
| Specialità | Neurologia |
|---|
| ICD - 10 | G70.0 |
|---|---|
| CIM - 9 | 358.0 |
| OMIM | 254200 |
| Malattie DB | 8460 |
| MedlinePlus | 000712 |
| eMedicine | 1171206, 793136, 261815 e 1216417 |
| eMedicine |
neuro / 232 emerg / 325 (emergenza), med / 3260 (gravidanza), oph / 263 (occhio) |
| Maglia | D009157 |
| Farmaco | Piridostigmina , neostigmina , ciclosporina , ciclofosfamide , prednisone , azatioprina , rituximab , eculizumab , micofenolato mofetile ( d ) , prednisolone , tacrolimus , distigmina ( d ) e piridostigmina |
| Paziente del Regno Unito | Miastenia-gravis-pro |
Il gravis (dal greco μύς "muscolo" e ἀσθένεια "debolezza"), in latino gravis è una malattia neuromuscolare autoimmune cronica , manifestata in varia misura dalla debolezza e dalla stanchezza eccessiva del muscolo scheletrico striato , cioè quelle che si attivano volontariamente. Deve il suo nome al neurologo tedesco Friedrich Jolly (1844-1904) e ha anche un nome omonimo : malattia di Erb - Goldflam , in onore dei due clinici che ne hanno fornito la descrizione più completa. E 'causata da anticorpi circolanti che, in più di tre o quattro casi, bersaglio recettori di acetilcolina a giunzione neuromuscolare , inibendo così l'effetto eccitatorio di questo neurotrasmettitore .
Storico
Probabilmente è stato Thomas Willis a descrivere per primo un paziente con miastenia grave. Jolly nomina la malattia coniando il termine “ miastenia grave pseudoparalitica ” e ne evidenzia il deterioramento elettrofisiologico. Mary Walker propose nel 1934 il trattamento con la fisostigmina . Anomalie del timo in relazione alla MG sono noti, e timectomia praticata fin dall'inizio del XX ° secolo , prima che la comprensione della fisiopatologia e l'identificazione della genesi autoimmune.
Epidemiologia
La sua prevalenza varia da 5 a 10 per 100.000 abitanti e la sua incidenza tra 2 e 20 all'anno e per milione di abitanti a seconda della serie. Può manifestarsi a qualsiasi età, il suo picco di incidenza riguarda la fascia di età dai 20 ai 30 anni. Il rapporto tra i sessi dei pazienti, 3 donne su 2 uomini, varia in base alla fascia di età (2 donne a 1 uomo per gli under 50, 1 donna a 1 uomo per gli over 50). Malattia essenzialmente sporadica, le forme familiari sono eccezionali.
Fisiopatologia
La presunta fisiopatologia della miastenia grave consiste nel danneggiamento delle proteine di membrana post-sinaptica della giunzione neuromuscolare da parte di autoanticorpi circolanti . Il primario anticorpo bersaglio corrispondente recettore dell'acetilcolina (un neurotrasmettitore ), che agisce come un inibitore competitivo di acetilcolina ed accelerare la degradazione del recettore dalla modulazione antigenica. Ciò si traduce in un aumento del numero di quanti di acetilcolina necessari per produrre la depolarizzazione della membrana postsinaptica, portando a un esaurimento più rapido e profondo delle riserve di acetilcolina presinaptica e clinicamente con conseguente affaticamento muscolare.
A medio termine, la presenza di questi anticorpi può indurre, tramite l'attivazione del sistema del complemento , alterazioni anatomiche della membrana postsinaptica, riducendone ulteriormente l'eccitabilità. In questa fase, nelle forme più gravi, possono insorgere deficit permanenti.
Ad eccezione della D-penicillamina e del trapianto di midollo allogenico, non è stato identificato alcun agente esogeno che promuova l'insorgenza della miastenia grave. Esiste una leggera predisposizione genetica, in particolare i gruppi HLA B8 (en) e DR3 (en) con DR1 (en) più specifico per la miastenia grave oculare. Molti altri autoanticorpi sono stati recentemente identificati come patogeni, tutti diretti a un componente della membrana postsinaptica: anticorpi anti-MuSK ( chinasi muscolare specifica ), anticorpi anti-agrina, anticorpi anti-LRP4. Viene dimostrato il ruolo del timo nella patogenesi. È la sede della maturazione dei linfociti T . Sotto la stimolazione di quest'ultimo, i linfociti B si trasformano in plasmacellule secernendo anticorpi.
Manifestazioni cliniche
Le caratteristiche cliniche possono essere descritte come segue:
il sintomo cardinale ed essenziale per la diagnosi è la stanchezza da sforzo. I sintomi sono quindi fluttuanti, intensificandosi con lo sforzo e migliorando a riposo. Spesso sono più marcati a fine giornata e possono peggiorare in situazioni di stress: infezione, intervento chirurgico, calore ... Infine, quindi, l'esame clinico può essere strettamente normale o poco disturbato, stress test che permettono poi di smascherare le anomalie .
La localizzazione muscolare e i sintomi che ne derivano sono variabili:
- nel 50% dei casi, il disturbo iniziale è ptosi , diplopia o entrambi. Questi sintomi sono spesso fluttuanti, di solito compaiono o peggiorano alla fine della giornata o durante la lettura o la guida di un veicolo. Questa è la denuncia più evocativa della diagnosi e consente l'unico esame diagnostico clinico specifico. È infatti caratteristica la comparsa di una ptosi con oftalmoparesi (abbassamento delle palpebre con difficoltà di convergenza) alla fissazione eccentrica dello sguardo prolungata di pochi minuti in un paziente precedentemente asintomatico. In un paziente sintomatico, il test del cubetto di ghiaccio (miglioramento della ptosi dopo aver posizionato del ghiaccio per alcuni minuti sulla palpebra sintomatica) è meno specifico ma molto suggestivo;
- nel 20% dei casi la lamentela iniziale riguarda un'affaticabilità degli arti, il più delle volte nelle sue parti prossimali, che può portare la diagnosi ad una miopatia. Ripetuti stress test possono smascherare l'affaticabilità segmentale ma non sono molto specifici;
- nel 10% dei casi, il disturbo iniziale consiste in astenia isolata (stanchezza generalizzata, spesso confusa con una vera debolezza muscolare), che non dovrebbe suggerire la diagnosi come trattamento di prima linea a meno che una reale debolezza muscolare non sia stata dimostrata da un medico e lasci affaticabilità essere in primo piano. Questa è la lamentela più aspecifica e i test clinici sono di scarsa utilità;
- molto raramente, i reclami iniziali consisteranno in disturbi fluttuanti di masticazione, deglutizione o debolezza degli estensori del collo;
- l'osservazione di un coinvolgimento oculo-cefalico globale che produce la "facies miastenica" è rara ma molto suggestiva (ptosi palpebrale asimmetrica, labbro inferiore cadente, cancellazione delle rughe sulla fronte, possibili disturbi oculomotori estrinseci e debolezza degli estensori del collo). La natura fluttuante di questa facies permette di distinguerla da molte altre cause di diplegia facciale e di confermare la diagnosi.
Per definizione, i sintomi sono solo motori e i disturbi sensoriali sono assenti. A causa di eccessivi sforzi compensativi, il paziente può tuttavia evidenziare disturbi sensibili e dolorosi (mialgia, artralgia, parestesia) che portano la diagnosi a patologia reumatica, miopatia, disturbo metabolico, polineuropatia o mielopatia.
All'esame, i riflessi miotatici sono normali e l'atrofia è osservata solo nelle forme avanzate gravi.
Si distingue tra forme generalizzate, forme bulbari e forme oculari pure. Si possono formare varie combinazioni (forme oculo-bulbari). Le forme oculari pure sono limitate alla compromissione dell'oculomotricità estrinseca e della ptosi. In questa fase rimarrà dal dieci al venti percento (dal 10 al 20%) delle forme oculari, forma disabilitante ma lieve della malattia, mentre le altre progrediranno verso la miastenia grave generalizzata.
Le forme bulbari iniziali (15%) includono una voce nasale con difficoltà di articolazione, debolezza masticatoria con tendenza a far cadere la mascella, difficoltà a deglutire (disfagia) con cibo falso o vie salivari.
Il decorso della malattia avviene tipicamente attraverso un susseguirsi di aggravamenti e remissioni, eventualmente intervallati da vere e proprie “crisi miasteniche” per le forme generalizzate. Queste crisi, vere e proprie emergenze mediche, sono definite da un peggioramento improvviso con insufficienza respiratoria acuta, dispnea con congestione, disturbi della deglutizione con rischio di aspirazione o grave debolezza generalizzata con impotenza che non lascia il posto al riposo.
Lo stadio di massima gravità viene raggiunto entro tre anni in più di tre quarti dei pazienti.
Nell'1-5% dei casi, la malattia è dichiarata da una crisi miastenica inaugurale. La diagnosi è quindi estremamente difficile e deve essere evocata in caso di sproporzione tra la presunta patologia causale e la gravità clinica o in caso di inspiegabili ripetuti fallimenti ai tentativi di svezzamento della ventilazione meccanica, altra diagnosi da evocare in tali situazioni. essendo una poliradicoloneurite acuta.
Classificazione clinica di Osserman o MGFA (Myasthenia Gravis Foundation of America)
Questa classificazione descrive diverse fasi:
- stadio I : debolezza di un muscolo oculare, possibile ptosi. Nessun'altra debolezza muscolare
- stadio II : debolezza dei muscoli oculari di qualsiasi gravità, lieve debolezza di altri muscoli
- stadio IIa : muscoli degli arti prevalentemente deboli o muscoli del tronco
- stadio II b: debolezza predominante nei muscoli respiratori o disturbi della deglutizione
- stadio III : debolezza dei muscoli oculari di qualsiasi gravità, moderata debolezza degli altri muscoli
- stadio IIIa : muscoli degli arti prevalentemente deboli o muscoli del tronco
- stadio III b: muscoli respiratori prevalentemente deboli o disturbi della deglutizione
- stadio IV : debolezza dei muscoli oculari di qualsiasi gravità, grave debolezza di altri muscoli
- stadio IV a: prevalentemente debolezza nei muscoli degli arti o dei muscoli del tronco
- stadio IV b: debolezza predominante nei muscoli respiratori o disturbi della deglutizione. Può anche includere la necessità di un sondino nasogastrico senza intubazione
- stadio V : intubazione necessaria per mantenere la respirazione
Forme speciali
Diverse forme di miastenia grave meritano di essere individuate dalla loro presentazione e dalla loro particolare gestione.
Miastenia grave autoimmune fetale e neonatale
La placenta è permeabile agli anticorpi. Dal dieci al venti percento (dal 10 al 20%) dei figli di madri con miastenia grave presenta miastenia grave neonatale che si manifesta entro i primi 3 giorni e di solito si risolve entro poche settimane (massimo 3 mesi). I sintomi che variano da bambino a bambino includono: ipotonia, pianto debole, suzione o deglutizione disturbata, ptosi, diplegia facciale e difficoltà respiratorie. Il trattamento si basa sulla gestione sintomatica in un'unità di terapia intensiva neonatale fino alla risoluzione e la somministrazione di farmaci anticolinesterasici. L'evoluzione è generalmente favorevole. Nelle forme più gravi può essere eseguita una trasfusione di dissanguamento.
Le forme fetali sono più rare e possono provocare un ritardo della crescita intrauterina. Eccezionalmente, si verificano manifestazioni cliniche gravi (idramnios, artrogriposi, morte in utero).
Miastenia grave autoimmune infantile e giovanile
Miastenia grave che inizia prima dei 15 anni, questa forma merita di essere individuata dalla difficile distinzione dalla miastenia grave congenita non autoimmune e dalla necessità, vista l'età, di limitare il più possibile l'uso di corticosteroidi e immunosoppressori.
Miastenia grave iatrogena autoimmune
Eccezionali, la loro diagnosi è generalmente evidente sulla base della storia clinica. Coinvolgono gli stessi autoanticorpi e rispondono agli stessi trattamenti della miastenia grave classica. Tuttavia, è probabile che rispondano a un trattamento specifico. Finora, sono stati dimostrati solo:
- Miastenia grave indotta da D-penicillamina. Riguarda l'1% dei pazienti trattati con D-penicillamina. Il recupero dopo l'interruzione della D-penicillamina entro 6 mesi è la regola;
- miastenia grave indotta da trapianto di midollo allogenico con malattia del trapianto contro l'ospite.
Patologie associate
Alcune patologie, dovute alla frequenza della loro associazione con la miastenia grave o alla gravità della loro intrinseca prognosi spontanea, dovrebbero essere sistematicamente studiate.
Tumori timici
Nel 10-15% dei casi di miastenia grave, con anticorpi anti-recettore dell'acetilcolina, si riscontra un timoma . I timomi sono tumori del mediastino anteriore, spesso benigni, associati in modo variabile a miastenia grave.
Un marker per l'esistenza di questi timomi per i pazienti di età inferiore ai 60 anni è l'antititina L'indicazione chirurgica è essenziale. Permette di specificare se il timoma è benigno (2/3 casi) o maligno a seconda del suo carattere invasivo oppure no.
Nel 50-70% della forma giovane di miastenia grave con anticorpo anti-recettore dell'acetilcolina si riscontra iperplasia timica. Questa anomalia è sempre da considerarsi benigna (il che non esclude l'ablazione del timo).
Tra il 15 e il 20% dei pazienti con timoma mostra anche segni clinici di miastenia grave e il 25% dei pazienti ha anticorpi anti-recettore dell'acetilcolina (anticorpi anti-ACh-R) senza mostrare sintomi. Qualsiasi paziente con un timoma con segni di miastenia grave ha anticorpi positivi e qualsiasi massa mediastinica asintomatica associata agli anticorpi anti-ACh-R è un timoma. Sebbene l'associazione statistica suggerisca una correlazione tra le due patologie, l'esatto meccanismo di causa-effetto rimane dibattuto e vengono prese in considerazione diverse ipotesi:
- selezione dei linfociti T difettosi all'interno del timoma, responsabili dell'ipersecrezione dell'autoanticorpo;
- presentazione difettosa degli autoantigeni alle cellule timiche, che porta alla non eliminazione dei linfociti T che li riconoscono;
- presenza di specifici centri germinali all'interno del parenchima timico che producono più prontamente autoanticorpi;
- negli anziani, presenza di autoimmunità aspecifica.
Non tutti i tipi istologici di timomi sono associati allo stesso modo con la miastenia grave, alcuni non sono nemmeno mai associati ad essa:
- tipo A: 0%
- tipo AB: 6,8%
- tipo B1: 40%
- tipo B2: 55,6%
- tipo B3: 10%
- carcinoma timico: 0%
Malattie autoimmuni
Nel 5-15% dei casi, a seconda della serie, nella miastenia viene identificata almeno un'altra malattia autoimmune. Si tratta di segnalazioni di associazioni significative, nessun legame fisiopatologico è stato dimostrato se non per l'ipotesi di un “terreno disimmune”. Queste patologie sono distiroidismo autoimmune, artrite reumatoide, lupus eritematoso sistemico, sindrome di Sjögren, polimiosite, malattia infiammatoria intestinale cronica, anemia di Biermer, anemia emolitica autoimmune, insufficienza surrenalica.
Test aggiuntivi
Gli esami complementari, oltre a quelli volti ad escludere eventuali diagnosi alternative, hanno lo scopo di confermare o escludere la diagnosi e, in caso di conferma diagnostica, di ricercare patologie associate. Questi esami sono:
Per scopi diagnostici
BiologiaNella pratica clinica vengono ricercati solo gli anticorpi anti-recettore dell'acetilcolina e, se sono assenti, gli anticorpi anti-MuSK. La loro specificità è del 99%. La loro sensibilità complessiva è superiore al 90%, meno del 10% della miastenia grave viene quindi definita “sieronegativa”. Più precisamente, la sensibilità degli anticorpi anti-recettore all'acetilcolina è del 90% per la miastenia grave generalizzata e del 50% per la miastenia grave oculare. A condizione che il test per gli anticorpi anti-recettore dell'acetilcolina sia negativo, la sensibilità degli anticorpi anti-MuSK è del 40% per la miastenia grave generalizzata e marginale per la miastenia grave oculare.
Le loro ottime specificità li rendono il miglior test per confermare la diagnosi in caso di forte sospetto clinico (valore predittivo positivo solo dell'1% per la popolazione generale).
Recentemente, in caso di miastenia grave doppia negativa, è possibile analizzare anche gli anticorpi LRP4.
Esami elettrofisiologiciSono necessari due esami elettrofisiologici:
- uno studio elettromiografico che include:
- un elettromiogramma di routine che di solito è normale. Le attività di reinnervazione possono tuttavia essere osservate nei casi avanzati gravi,
- uno studio elettromiografico con stimolazione sovra-massimale ripetitiva di un nervo motore. Il test è considerato positivo quando il decremento di ampiezza del potenziale dell'unità motoria (PUM) è maggiore del 10%. Questo test non è specifico e ha una sensibilità del 79% per la miastenia grave generalizzata e del 50% per la miastenia grave oculare,
- uno studio elettromiografico "singola fibra" con misurazione di un Jitter (variazione della latenza tra la stimolazione e il Potenziale dell'Unità Motoria per una data fibra durante la stimolazione ripetitiva di un nervo motore) significa sullo studio di molte fibre che richiedono un esaminatore esperto e specializzato attrezzature. Il test è considerato positivo quando si osserva un aumento di questo jitter al di sopra degli standard di laboratorio per il muscolo studiato. Questo test non è specifico e ha una sensibilità del 98% per la miastenia grave generalizzata e dell'80% per la miastenia grave oculare,
- uno studio delle velocità di conduzione nervosa. Questo esame deve essere normale affinché le anomalie dell'elettromiografia siano considerate rilevanti.
L'ottima sensibilità dell'elettromiografia lo rende il miglior test per escludere la diagnosi in caso di basso sospetto clinico (valore predittivo negativo indeterminabile se la percentuale di pazienti nel gruppo di studio è maggiore dell'1%).
Test farmacologicoLa prostigmina viene utilizzata sia come test terapeutico per os, sia in IM o soprattutto IV di fronte a un sintomo clinico che non ha parlato a livello elettrofisiologico o in urgenza (ptosi, diplopia, linguaggio o disturbi respiratori). considerato positivo se determina un miglioramento dei sintomi o dei segni elettrofisiologici. A volte è paragonato a un test placebo.
Alla ricerca di patologie associate
BiologiaSaranno sistematicamente misurati i marker di patologie autoimmuni potenzialmente associate alla miastenia grave. Ciò include marker di infiammazione, ormoni tiroidei e anticorpi anti-piroperossidasi, fattori anti-nucleari, anticorpi anti-nucleari, ematogramma, ionogramma, funzionalità epatica e renale, vitamina B12 e folato.
Scanner TC toracicoEseguito sistematicamente per cercare un timoma (sensibilità 99%, specificità 95%) e iperplasia timica (sensibilità 50%, specificità 95%).
Diagnosi differenziale
La diagnosi differenziale è ampia e dipende dalla presentazione clinica. Possiamo citare in particolare:
- altre sindromi miasteniche: congenita miastenia gravis , sindrome miastenica di Lambert-Eaton , botulismo , alcuni veleni di serpente , organofosforici o avvelenamento di magnesio;
- miopatie;
- neuropatie periferiche;
- patologie reumatiche;
- disturbi di liquidi ed elettroliti;
- endocrinopatie;
- anemia;
- ptosi acquisita, congenita e traumatica;
- strabismo scompensato;
- disturbi funzionali, disturbi psichiatrici e sindrome da stanchezza cronica.
Prognosi
La prognosi è specifica per ogni paziente. Tuttavia, possiamo descrivere alcune generalità:
La gravità della miastenia grave è legata al verificarsi di crisi miasteniche con distress respiratorio e pericolo di vita. Questo rischio è massimo all'inizio della malattia, con il 75% delle crisi che si verificano nei primi due anni di sviluppo.
Se non trattato, il decorso della miastenia grave generalizzata può essere fatale. La prognosi vitale delle forme che rimangono oculari non è coinvolta.
In casi molto rari si verificano remissioni spontanee della malattia, la cui durata è variabile.
Dal 10 al 20% risponderà poco o no al trattamento e svilupperà un'impotenza motoria variabile. I fattori di prognosi sfavorevole e di scarsa risposta terapeutica sono: la presenza di un timoma, la presenza di anticorpi anti-MuSK e le forme siero-negative.
Assistenza terapeutica
La gestione della miastenia grave può essere schematicamente suddivisa in trattamento sintomatico, trattamento di base e trattamento di crisi della malattia, trattamento delle patologie associate e misure generali. I principi generali sono:
Trattamenti sintomatici per la miastenia grave
Farmaci anticolinesterasiciGli inibitori dell'acetilcolinesterasi, un enzima che degrada l' acetilcolina , costituiscono il trattamento sintomatico di prima linea. I più usati sono la piridostigmina (Mestinon) e l'ambenonio cloruro (Mytelase). L'uso di altri farmaci anticolinesterasici (come la neostigmina ) è diventato marginale a parte la crisi miastenica. La loro efficacia nella miastenia grave sieronegativa o con gli anticorpi anti-MuSK non è stata dimostrata.
Trattamento a lungo termine per la miastenia grave
Corticosteroidi e immunosoppressoriI corticosteroidi - come un regime progressivo di prednisone (Cortancyl) o prednisolone (Solupred) - immunosoppressori - azatioprina (Imurel) che hanno dimostrato di essere più efficace - e il micofenolato mofetile (Cellcept) sono il secondo trattamento più importante. Intenzione. I corticosteroidi possono essere iniziati a dosi molto basse e con una stretta rivalutazione clinica, con un peggioramento clinico transitorio che è comune.
È stato ora dimostrato che l'aggiunta di un trattamento combinato con corticosteroidi e immunosoppressori per la miastenia grave generalizzata non sufficientemente controllata con farmaci anticolinesterasici migliora lo stato clinico a due anni rispetto all'aggiunta di corticosteroidi o immunosoppressori separatamente. Alcuni esperti ne consigliano l'uso come trattamento di prima linea per le forme sieronegative o con anticorpi anti-MuSK.
Gli immunosoppressori non sono molto efficaci per le forme oculari.
Marginalmente, trattamenti biologici come il rituximab (Mabthera), un anticorpo monoclonale chimerico mirato alla molecola CD20 espressamente espressa dai linfociti B , sono stati utilizzati con un certo successo nelle forme gravi.
Plasmaferesi endovenosa e immunoglobulineQuesti trattamenti hanno poco spazio a parte le crisi miasteniche ( vedi sotto ). Tuttavia, sono eccezionalmente utilizzati per le forme più gravi resistenti ad altri trattamenti o in caso di rapida degradazione clinica.
Trattamenti per patologie associate
Timectomia e trattamenti adiuvantiLa scoperta di un timoma è un'indicazione assoluta per la timectomia e richiede un follow-up radiologico prolungato alla ricerca di recidive neoplastiche. In caso di resezione incompleta, infiltrazione di tessuti vicini o scoperta di metastasi, deve essere offerto un trattamento adiuvante, consistente in radioterapia e / o chemioterapia, a seconda dei casi.
Il beneficio clinico della timectomia in assenza di timoma è ancora dibattuto. È comunque consigliato in caso di scoperta di iperplasia timica con presenza di anticorpi recettori anti-acetilcolina in pazienti sotto i 40 anni di età. Uno studio randomizzato del 2016 ha anche riscontrato un miglioramento clinico dei sintomi della miastenia grave dopo timectomia, anche in assenza di iperplasia timica.
È possibile un peggioramento sintomatico post-chirurgico transitorio. Nei primi mesi successivi alla timectomia, si può tentare la sospensione del farmaco se compare un miglioramento sintomatico o addirittura la remissione.
Altri trattamentiSono necessari trattamenti specifici in caso di scoperta di una patologia autoimmune associata.
Gestione delle crisi miasteniche
Terapia di supportoQualsiasi rapida insorgenza di insufficienza respiratoria, dispnea con congestione bronchiale, disturbi della deglutizione o debolezza generalizzata oggettivata da un medico giustifica un trasferimento medico in un istituto ospedaliero con un'unità di terapia intensiva. Al momento del ricovero, verrà eseguita una valutazione delle vie aeree, della respirazione, della circolazione e della neurologia, nonché una misurazione della capacità vitale (CV). Un disturbo della coscienza, una capacità vitale inferiore al 25% del valore teorico o l'esaurimento clinico respiratorio giustificano l'intubazione e il trasferimento in un reparto di terapia intensiva per la ventilazione meccanica e l'eventuale stabilizzazione emodinamica. In altri casi è sufficiente l'assistenza ordinaria con una valutazione regolare della capacità vitale.
Correzione di fattori scatenanti e promotori reversibiliQuesti fattori devono essere ricercati e corretti non appena vengono eseguite manovre vitali. Si tratta principalmente di cause iatrogene (vedi Controindicazioni ai farmaci), infezioni, scompenso di altre patologie croniche nel paziente e innalzamenti delle temperature, endogene o esogene.
Il caso di crisi epilettiche che si verificano durante la gravidanza è speciale e la possibilità che si verifichino deve essere stata preventivamente discussa con la paziente. Le crisi epilettiche gravi che non rispondono al trattamento sintomatico richiedono una gestione appropriata.
Escludere un'overdose di anticolinesterasiciLa principale diagnosi differenziale di crisi miastenica è il sovradosaggio di anticolinesterasi. È da sospettare sistematicamente in caso di assunzione giornaliera di più di 480 mg di piridostigmina o di sintomi muscarinici: bradicardia, miosi bilaterale, ipersecrezioni, disgregazione fecale, ecc. In caso di dubbio, il peggioramento clinico dopo la somministrazione di neostigmina confermerà la diagnosi di sovradosaggio. La gestione è quindi puramente di supporto, a parte la somministrazione di atropina per i suoi effetti antimuscarinici.
Trattamenti sintomaticiLa somministrazione di neostigmina è il trattamento sintomatico di prima linea. Se compaiono sintomi muscarinici, è necessario aggiungere atropina.
In caso di peggioramento clinico durante il trattamento, si deve prendere in considerazione un sovradosaggio di farmaci anticolinesterasici.
In caso di scarsa risposta terapeutica (fallimento della detubazione), il trattamento di seconda linea si basa sulla ripetizione di cure plasmaferesi e / o immunoglobuliniche endovenose.
Se questo fallisce, i corticosteroidi e gli immunosoppressori sono il trattamento di terza linea. Le loro indicazioni devono comunque essere richieste con attenzione, essendo comune un peggioramento clinico transitorio.
Misure generali e cure para-mediche
Controindicazioni ai farmaci Carta miastenicaIl Ministero della Salute francese ha pubblicato una scheda di cura e di emergenza per le persone con miastenia grave. Si raccomanda vivamente di portare con sé da parte del paziente questa scheda che menzioni la sua malattia, il suo trattamento, le sue ultime vaccinazioni e l'elenco dei farmaci controindicati nella miastenia grave. Possono ottenerlo dalle consultazioni di riferimento o contattando l'AFM-téléthon].
Stile di vitaCome per qualsiasi patologia cronica, la miastenia grave richiede che il paziente sia istruito sulla sua malattia e in particolare sui fattori che favoriscono le crisi miasteniche. La partecipazione a un esercizio fisico moderato, adattato allo stato del momento, dovrebbe essere incoraggiata con un riposo frequente.
Assistenza paramedicaNelle forme gravi o resistenti a cure approfondite, può risultare necessario il supporto sociale e da parte di specialisti in fisioterapia, logopedia, terapia occupazionale, riabilitazione o psicologia, così come il rinvio del paziente a una terapia combinata.
Preparati per gravidanze e interventi chirurgiciNel complesso, la gravidanza e la chirurgia sono una delle principali cause di convulsioni miasteniche, che si verificano nel 30% dei casi. Al fine di ridurre al minimo i rischi, alcuni autori raccomandano lo svolgimento pre-parto e pre-chirurgico di sessioni di plasmaferesi o cure immunoglobuliniche, nonché una valutazione che includa test respiratori funzionali. Il parto deve sempre avvenire in una struttura ospedaliera con unità di terapia intensiva e unità di rianimazione neonatale. La detubazione non deve mai essere eseguita fino a quando non viene confermata la capacità di partecipazione del paziente.
Durante la gravidanza, i corticosteroidi e gli immunosoppressori devono essere utilizzati in consultazione con un ginecologo.
Note e riferimenti
- (in) MB Walker , " Treatment of myasthenia gravis with physostigmine " , Lancet , Vol. 1,1934, p. 1200-1201 ( DOI 10.1016 / S0140-6736 (00) 94294-6 )
- (in) Phillips LH, "L'epidemiologia della miastenia grave " Ann NY Acad Sci. 2003; 998: 407-12
- College of Teachers of Neurology. Miastenia grave
- (in) Carr AS, Cardwell CR, PO McCarron, J McConville, "Una revisione sistematica degli studi epidemiologici basati sulla popolazione nella miastenia grave" BMC Neurol. 2010; 10:46.
- (en) Bradley et al. Neurology in clinic practice , 5 th ed., Butterworth-Heinemann, 2007
- Goulon-Goeau et al. "Miastenia grave e sindromi miasteniche" EMC-Neurologie , 17-172-B-10, 2002, Elsevier, riepilogo online
- B. Eymard “anticorpi in miastenia grave” recensione Neurological 2009; 165 (2): 125-205 DOI : 10.1016 / j.neurol.2008.11.020
- (a) Zhang B, C Shen, Bealmear B, Ragheb S, Xiong WC, Lewis RA, Lisak RP, Mei L. " Autoanticorpi agrina in miastenia grave pazienti ' PLoS One , 2014; 3: e91816 DOI : 10.1371 /journal.pone.0091816
- ( ) W. Allan. "Patogenesi della miastenia" Up-to-Date , 2012
- (in) Howard et al. "Correlazioni cliniche di anticorpi che legano, bloccano o modulano i recettori umani dell'acetilcolina nella miastenia grave " Ann NY Acas Sci. 1987
- (en) SJ Bird "Le manifestazioni cliniche della miastenia gravis " Up-to-Date 2013
- (en) Bershad et al. " Myasthenia gravis crisis" South Med J. 2008; 101 (1): 63-9. DOI : 10.1097 / SMJ.0b013e31815d4398
- Gaumond "Patologie dell'occhio della miastenia grave" EMC-Neurology 2005 DOI : 10.1016 / j.emcn.2005.08.002
- (in) Pelak e quando "oculare miastenia" Data Up-to- 2013
- (en) Spillane J, E Higham, Kullmann DM. " Miastenia gravis " BMJ 2012; 345: e8497
- (en) Jaretzki A, Barohn RJ, Ernstoff RM et al. , " Miastenia grave: raccomandazioni per gli standard di ricerca clinica. Task Force del Medical Scientific Advisory Board della Myasthenia Gravis Foundation of America " , Neurology , vol. 55, n o 1,2000, p. 16-23 ( PMID 10891897 , leggi in linea )
- (in) Finnis MF Jayawant S, " Juvenile miastenia grave: una prospettiva pediatrica " , Autoimmune Dis , vol. 2011,2011, p. 404101. ( PMID 22110902 , PMCID PMC3206364 , DOI 10.4061 / 2011/404101 , leggi online [html] )
- Anticorpo antititina nella miastenia grave a esordio precoce e tardivo. Szczudlik P, Szyluk B, Lipowska M, Ryniewicz B, Kubiszewska J, Dutkiewicz M, Gilhus NE, Kostera-Pruszczyk A. Acta Neurol Scand. 2014 (giugno). Doi: 10.1111 / ane.12271. [Epub prima della stampa]
- The thymus, timoma and myasthenia gravis Fujii Y, Surg Today 2013 May; 43 (5): 461-6. doi: 10.1007 / s00595-012-0318-2
- Significato clinico e funzionale della classificazione dell'OMS sulle neoplasie epiteliali timiche umane: uno studio su 146 tumori consecutivi. Okumura M, Miyoshi S, Fujii Y, Takeuchi Y, Shiono H, Inoue M, Fukuhara K, Kadota Y, Tateyama H, Eimoto T, Matsuda H, Am J Surg Pathol 2001 Jan; 25 (1): 103-10.
- (en) Mercelis et al. "Utilità diagnostica dell'elettromiografia stimolata a fibra singola del muscolo orbicolare dell'occhio in pazienti con sospetta miastenia oculare" Muscle Nerve 2011; 43 (2): 168-70.
- (en) Preston et al. Elettromiografia e disturbi neuromuscolari. Correlazioni clinico-elettrofisiologiche , 2 ° ed., Elsevier, 2005
- (en) Taraldsen Heldan. “Miastenia grave sieropositiva. Uno studio epidemiologico a livello nazionale » Neurology 2009
- (en) Trakas et al. "Sviluppo di un test diagnostico altamente sensibile per autoanticorpi tirosin chinasi muscolo-specifici (MuSK) nella miastenia grave" J Neuroimmunol . 2011; 240-241: 79-86.
- (en) Vincent et al. "Anticorpo recettore dell'acetilcolina come test diagnostico per la miastenia grave : risultati in 153 casi convalidati e 2967 saggi diagnostici" J Neurolo Neurosurg Psych. 1985; 48 (12): 1246-52.
- (en) Witoonpanich et al. “Studio elettrofisiologico e immunologico nella miastenia grave : sensibilità e correlazione diagnostica” Clin Neurophysiol. 2011; 122 (9): 1873-7.
- (en) Zambelis et al. "Stimolazione nervosa ripetitiva dei muscoli facciali e ipotenari: sensibilità relativa in diversi sottogruppi di miastenia grave" Eur Neurol. 2011; 65 (4): 203-7.
- (en) Lindstrom et al. "Anticorpo al recettore dell'acetilcolina nella miastenia grave. Prevalenza, correlati clinici e valore diagnostico » Neurology 1976.
- (in) Bird "Diagnosis in myasthenia gravis " Up-to-Date , 2013
- Autoanticorpi contro la proteina 4 correlata alle lipoproteine in pazienti con miastenia grave doppia sieronegativa. Zhang B1, Tzartos JS, Belimezi M, Ragheb S, Bealmear B, Lewis RA, Xiong WC, Lisak RP, Tzartos SJ, Mei L. Arch Neurol. 2012 aprile; 69 (4): 445-51. doi: 10.1001 / archneurol.2011.2393. Epub 2011 12 dicembre
- (in) Bird "Differential Diognosis of myasthenia gravis" Up-to-Date , 2012
- (in) Bird "Treatment of myasthenia" Up-to-Date , 2013
- (in) Howard et al. Miastenia grave. Un manuale per il fornitore di assistenza sanitaria , Myasthenia Gravis Foundation of America, 2008
- (it) oro R, Schneider-Gold C, “ gli standard attuali e futuri nel trattamento della miastenia grave ” , Neurotherapeutics , vol. 5, n o 4,2008, p. 535-41. ( PMID 19019304 , PMCID PMC4514693 , DOI 10.1016 / j.nurt.2008.08.011 , leggi online [html] )
- (en) Mandawat et al. "Analisi comparativa dell'opzione terapeutica utilizzata per la miastenia grave " Ann Neurol. 2010; 68 (6): 797-805.
- " ambenonio cloruro di " on www.vidal.fr (accessibile su 1 ° agosto 2015 )
- (en) Collongues N, O Casez, Lacour A. et al. "Rituximab nella miastenia refrattaria e non refrattaria: uno studio multicentrico retrospettivo " Muscle Nerve 2012; 46: 687-91
- (in) Gil I. Wolfe, Henry J. Kaminski, Inmaculada B. Aban et al., " Randomized Trial of Myasthenia Gravis in Thymectomy " , New England Journal of Medicine (NEJM \ / MMS), vol. 375, n o 6,11 agosto 2016, p. 511-522 ( ISSN 0028-4793 , DOI 10.1056 / nejmoa1602489 , leggi online ).
- (in) Goldenberg, WD and Shah, AK , " Myasthenia Gravis " , eMedicine (accesso 5 maggio 2012 )
- (fr) Questo articolo è parzialmente o interamente tratto dall'articolo di Wikipedia in inglese intitolato " Myasthenia gravis " ( vedere l'elenco degli autori ) .