Bromometano
| Bromometano | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identificazione | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Sinonimi |
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100.000.740 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CE | 200-813-2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 6323 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ChEBI | 39275 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SORRISI |
CBr , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1 / CH3Br / c1-2 / h1H3 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aspetto | gas compresso liquefatto, incolore e inodore. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietà chimiche | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Formula bruta |
C H 3 Br [Isomeri] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Massa molare | 94,939 ± 0,002 g / mol C 12,65%, H 3,19%, Br 84,16%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Momento dipolare | 1.8203 ± 0.0004 D | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietà fisiche | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fusione | −93,66 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° bollitura | 3,56 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solubilità | in acqua a 20 ° C : 1,5 ml / 100 ml | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Parametro di solubilità δ | 19,6 MPa 1/2 ( 25 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
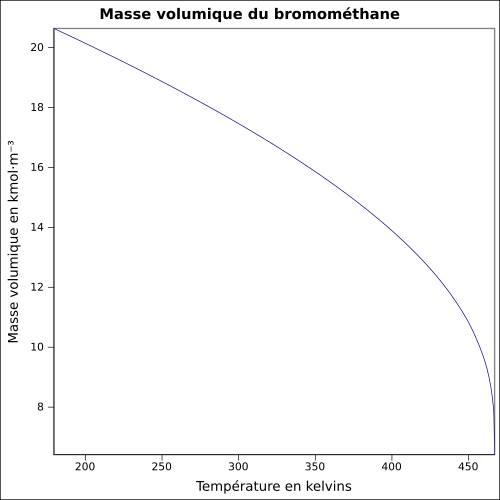
| Massa volumica |
3,9739 g · cm -3 ( 0 ° C , 1013 mbar )
equazione:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Temperatura di autoaccensione | 537 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| punto d'infiammabilità | < 194 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Limiti di esplosività in aria | 8,6 - 20 % vol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
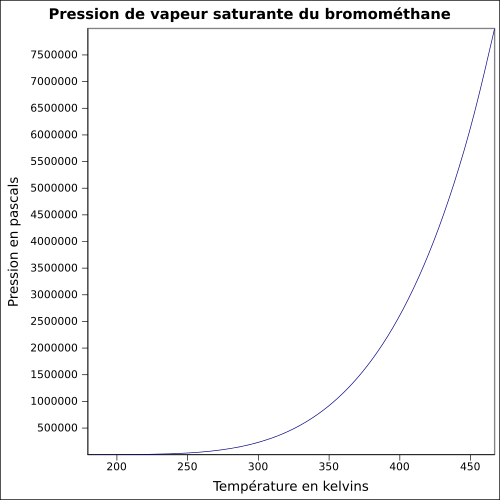
| Pressione del vapore saturo |
1,89 bar a 20 ° C 2,6 bar a 30 ° C 4,9 bar a 50 ° C equazione:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto critico | ( 194 ° C ), 52,3 bar , 0,577 kg · l -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto triplo | ( −93,7 ° C ), 0,002 bar | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termochimica | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 liquido, 1 bar | 155,14 J · K -1 · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 gas | -34,3 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 liquido | -60,6 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ fus H ° | 6,0 kJ · mol da -1 a -93,65 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ vap H ° | 23,24 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
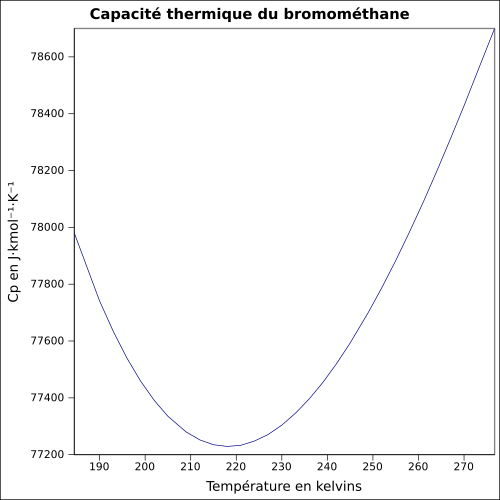
| C p |
114,6 J · K -1 · mol -1 (liquido, 9,85 ° C )
equazione:
equazione:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietà elettroniche | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 re energia di ionizzazione | 10,541 ± 0,003 eV (gas) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Precauzioni | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
    Pericolo H301, H315, H319, H331, H335, H341, H373, H400, EUH059, H301 : Tossico se ingerito H315 : Provoca irritazione cutanea H319 : Provoca grave irritazione oculare H331 : Tossico se inalato H335 : Può irritare le vie respiratorie H341 : Sospettato di provocare alterazioni genetiche (indicare la via di esposizione se è dimostrato in modo definitivo che nessun'altra via di esposizione provoca lo stesso pericolo) H373 : Sospetto rischio di gravi danni agli organi (elencare tutti gli organi interessati, se noti) a seguito di esposizione ripetuta o prolungata (indicare la via di esposizione se è dimostrato in modo conclusivo che nessun'altra via di esposizione causa il stesso pericolo) H400 : Molto tossico per gli organismi acquatici EUH059 : Pericoloso per lo strato di ozono |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
   A, D1A, D2B, E, A : Pressione assoluta di vapore del gas compresso a 50 ° C = 480 kPa D1A : Materiale molto tossico con gravi effetti immediati Trasporto di merci pericolose: classe 2.3 D2B : Materiale tossico con altri effetti tossici Tossicità cronica E : Materiale corrosivo necrosi della pelle umana Divulgazione a 1,0% secondo criteri di classificazione |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 3 0 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Trasporto | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
26 : gas velenoso Numero ONU : 1062 : BROMURO DI METILE Classe: 2.3 Etichetta: 2.3 : Gas tossici (corrisponde ai gruppi designati da una T maiuscola, cioè T, TF, TC, TO, TFC e Bam). Imballaggio: -  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Classificazione IARC | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gruppo 3: non classificabile quanto alla sua cancerogenicità per l'uomo | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ingestione | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Altro | depressione del sistema nervoso centrale . Danni al fegato e ai reni . Arresto respiratorio. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ecotossicologia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LogP | 1.19 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Soglia di odore | basso: 20 ppm alto: 1000 ppm |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Unità di SI e STP se non diversamente specificato. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Il bromuro di metile o bromuro di metile è un composto chimico organico alogenato la cui formula chimica è: C H 3 Br . Fa parte degli alogenuri metilici ( alocarburi ):
È un gas velenoso e altamente ecotossico , incolore e non infiammabile senza odore caratteristico. Le sue proprietà chimiche sono abbastanza simili a quelle del clorometano .
È un pesticida ( insetticida ), della famiglia dei biocidi . Fa parte dei gas refrigeranti. Il bromuro di metano è commercializzato con diversi nomi, i più noti dei quali sono Embafume e Terabol . È anche noto con il nome R40B1 .
Poiché è sia un gas a effetto serra (potente) che uno dei gas che distruggono lo strato di ozono che protegge la terra da un'eccessiva radiazione ultravioletta , si prevede di vietarlo a lungo, ma solo alcuni paesi lo hanno applicato, la Francia dal 2005 esenzioni per determinati usi) e dall'Unione Europea dal 2011.
Alla Trentesima Riunione delle Parti del Protocollo di Montreal sulle sostanze che impoveriscono lo strato di ozono, tenutasi a Quito , capitale dell'Ecuador, Canada , Australia , Argentina e Sud Africa, ha ottenuto anche esenzioni per l'uso del bromuro di metile per il 2019 e il 2020
Origine
Il bromuro di metano esiste in piccole quantità in natura dove si forma naturalmente nell'oceano , sintetizzato dal fitoplancton (e dalle alghe ?).
Quando è biogenico (di origine naturale, prodotto da organismi viventi), gioca in natura un ruolo che non è ancora stato compreso. Potrebbe essere coinvolto nel feedback climatico (perché se il suo tempo di permanenza nell'atmosfera è breve (circa 1 anno), è un potente gas serra e inibisce la produzione di ozono stratosferico .
Durante un recente esperimento di geoingegneria volto ad aumentare le capacità dei pozzi di carbonio marini fertilizzando l'oceano con ferro su scala media (superficie inferiore a 1000 km 2 ), è stato osservato un effetto negativo: aumento della produzione di bromometano oceanico.
Proviene anche da alcune piante terrestri, in particolare quelle della famiglia brassica .
Industrialmente, come biocida, viene prodotto facendo reagire metanolo con acido bromidrico .
Utilizza
Fino a quando la sua produzione e il suo utilizzo non furono ridotti o banditi dal Protocollo di Montreal (firmato nel 1987, ma ancora parzialmente rispettato), era ampiamente e ampiamente utilizzato come agente di sterilizzazione del suolo, principalmente per la produzione di semi ma anche per alcune colture orticole come le fragole .
Il bromuro di metano è stato anche utilizzato come fumigante generico per controllare un'ampia varietà di parassiti, dai ratti e insetti ai funghi microscopici. Viene ancora utilizzato per determinati usi (disinfezione del legno importato). Serve anche come precursore per la produzione di altri prodotti chimici, ed è stato utilizzato come solvente per l' estrazione degli oli dai semi e come sgrassante della lana .
Quando il Protocollo di Montreal ha severamente limitato l'uso del bromuro di metile a livello internazionale, alcuni paesi, inclusi gli Stati Uniti, hanno incoraggiato le esenzioni per l'uso del prodotto in uso controllato. Nel 2004, l'ultimo anno per il quale sono disponibili i dati, più di 3.000 tonnellate di bromuro di metile sono state spruzzate nei campi californiani.
Nel 2017, quasi 10.000 tonnellate di bromuro di metile erano state utilizzate per i trattamenti di quarantena e pre-spedizione e quel numero era in aumento. Negli ultimi dieci anni, la quantità di bromuro di metile utilizzata per i trattamenti di quarantena e pre-imbarco era più che raddoppiata in alcuni paesi, probabilmente a causa dell'aumento del commercio, dei pericoli posti dagli organismi nocivi da quarantena e / o dell'errata classificazione di alcuni usi come quarantena e pre-imbarco. usi della spedizione. Queste erano le componenti principali delle emissioni globali, pari a circa 7.500 tonnellate all'anno. Il bromuro di metile utilizzato per i trattamenti di quarantena e pre-spedizione era altamente volatile (fino al 95% del bromuro di metile così utilizzato poteva essere rilasciato direttamente nell'atmosfera dopo la fumigazione). Tuttavia, i progressi nelle tecniche di recupero e distruzione potrebbero ridurre notevolmente le emissioni.
Il bromuro di metano veniva utilizzato una volta negli estintori speciali, prima dell'avvento degli halon meno tossici, perché è elettricamente non conduttivo e non lascia residui. È stato utilizzato principalmente per sottostazioni elettriche, aerei militari e contro alcuni rischi industriali. Non è mai stato così popolare come altri agenti a causa del suo alto costo e della sua tossicità. Il bromuro di metano è stato utilizzato dagli anni '20 agli anni '60. In Francia, il decreto n. 59-449 del21 marzo 1959vietato 1 ° gennaio 1961, la fabbricazione, il possesso, il riempimento, la cessione a titolo oneroso o gratuito di estintori caricati con bromuro di metile o tetracloruro di carbonio .
Distruzione dello strato di ozono
Il bromuro di metano è nell'elenco delle sostanze vietate dal protocollo di Montreal a causa del rischio di distruzione dello strato di ozono . Poiché il bromo è 60 volte più dannoso del cloro , anche una piccola quantità di bromuro di metile è sufficiente per causare danni considerevoli allo strato di ozono . Nel 2005 e nel 2006, tuttavia, è stata concessa un'esenzione per uso controllato ai sensi del protocollo di Montreal.
Controversie
Il Protocollo di Montreal stabilisce che l'uso del bromometano deve essere vietato, ma questo prodotto ha molti vantaggi, in particolare per il trattamento del legno, del suolo, dei cereali e delle sementi, e per determinati usi non ci sono prodotti sostitutivi. conveniente. Il bromuro di metano viene utilizzato negli Stati Uniti per preparare campi da golf e superfici in erba utilizzate per varie competizioni atletiche, in particolare per la manutenzione del manto erboso Cynodon dactylon . L' amministrazione di George W. Bush ha adottato deroghe per evitare perturbazioni del mercato.
Una valutazione del rischio è stata aggiornata nel 2010 dall'EFSA
Effetti sulla salute
Se inalato ad alta concentrazione per breve tempo, provoca mal di testa, vertigini, nausea, vomito, malessere. Questi sintomi possono essere seguiti da segni di eccitazione nervosa, convulsioni e persino disturbi mentali acuti come l'agitazione maniacale . L'inalazione prolungata a concentrazioni inferiori può causare irritazione bronchiale e danni ai polmoni.
Il liquido brucia la pelle, provocando prurito ed eritema, quindi vesciche diverse ore dopo il contatto. Liquidi e gas provocano gravi ustioni agli occhi.
I livelli di esposizione che possono causare la morte variano da 1.600 a 60.000 ppm , a seconda della durata dell'esposizione.
Il danno respiratorio, renale e neurologico colpisce più persone. Non sono stati osservati casi di gravi effetti a lungo termine sul sistema nervoso nell'uomo a seguito di esposizione a bassi livelli, ma studi su conigli e scimmie hanno mostrato lesioni classificate da moderate a gravi.
Produzione e degrado
Le fonti di produzione di CH 3 Br includono la produzione oceanica, le emissioni da piante e paludi , combustione di biomasse , fumigazione del suolo e gas di scarico dei veicoli da carburante contenente piombo , nonché l'industria, la produzione di beni di consumo durevoli e beni deperibili. La sua produzione industriale è in declino, ma non si è fermata, anche in Francia
La degradazione dell'inquinante avviene per decomposizione fotochimica in atmosfera (reazione con il radicale chimico idrossile (OH)) e per ossidazione (che dà come prodotti secondari BrC (O) CH 3 e BrC (O) H), o per fotodecomposizione a altitudini più elevate.
A questi mezzi di eliminazione si devono aggiungere le perdite (adsorbimento, degradazione) nel suolo, degradazione chimica e biologica nell'oceano e un po 'di riciclaggio da piante verdi.
Alternative
Per molti usi (es: trattamento del legno, fumigazione del terreno prima della messa a dimora), non esiste alternativa così facile da attuare (oppure, con un maggior rischio tossico, se si utilizza ad esempio come alternativa la cloropicrina utilizzata durante la guerra mondiale Io come gas di guerra e come gas per uccidere gli animali nelle loro tane, o dazomet ...)
- I trattamenti termici possono essere utilizzati per disinfettare i pavimenti delle serre (eccetto contro le finestre) o del pollaio (con le stesse attrezzature del diserbo termico se necessario)
- Gestione integrata dei parassiti; ad esempio secondo ANSES, per l'agricoltura l'agricoltore può associarsi
- attento esame dei grafici di moltiplicazione,
- la coltivazione di varietà ad alto livello di resistenza,
- la produzione di semi su parcelle integre,
- campionamento e analisi di lotti di semi,
- l'eliminazione dei residui vegetali associati ai semi,
- pratiche culturali che limitano il rischio di insorgenza di un agente patogeno (rotazioni, ecc.).
Note e riferimenti
- BROMURO DI METILE , scheda / e di sicurezza del Programma internazionale sulla sicurezza chimica , consultato il 9 maggio 2009
- (a) David R. Lide, Manuale di chimica e fisica , Boca Raton, CRC,16 giugno 2008, 89 ° ed. , 2736 p. ( ISBN 978-1-4200-6679-1 e 1-4200-6679-X ) , p. 9-50
- massa molecolare calcolata dal " peso atomico degli elementi 2007 " su www.chem.qmul.ac.uk .
- Entry "Bromometano" nel database chimica GESTIS dell'IFA (ente tedesco responsabile della sicurezza e salute sul lavoro) ( tedesco , inglese ), si accede il 19 febbraio 2009 (È necessario JavaScript)
- (in) James E. Mark, Physical Properties of Polymer Handbook , Springer,2007, 2 ° ed. , 1076 p. ( ISBN 978-0-387-69002-5 e 0-387-69002-6 , presentazione online ) , p. 294
- (en) Robert H. Perry e Donald W. verde , di Perry Chemical Engineers' Handbook , Stati Uniti d'America, McGraw-Hill,1997, 7 ° ed. , 2400 p. ( ISBN 0-07-049841-5 ) , p. 2-50
- (en) "Methyl bromide " , su NIST / WebBook , accesso
- (in) Carl L. Yaws, Handbook of Thermodynamic Diagrams , Vol. 1, 2 e 3, Huston, Texas, Gulf Pub. Co.,1996( ISBN 0-88415-857-8 , 0-88415-858-6 e 0-88415-859-4 )
- (a) David R. Lide, Manuale di chimica e fisica , Boca Raton, CRC,2008, 89 ° ed. , 2736 p. ( ISBN 978-1-4200-6679-1 ) , p. 10-205
- Gruppo di lavoro IARC sulla valutazione dei rischi cancerogeni per gli esseri umani, " Valutazioni globali di cancerogenicità per gli esseri umani, Gruppo 3: Non classificabile per quanto riguarda la loro cancerogenicità per gli esseri umani " , su http://monographs.iarc.fr , IARC,16 gennaio 2009(visitato il 22 agosto 2009 )
- Numero indice nella tabella 3.1 dell'appendice VI del regolamento CE n. 1272/2008 (16 dicembre 2008)
- " Bromomethane " nella banca dati dei prodotti chimici Reptox del CSST (organizzazione del Quebec responsabile per la sicurezza e la salute sul lavoro), accesso 25 aprile 2009
- " Methyl bromide " su hazmap.nlm.nih.gov (visitato il 14 novembre 2009 )
- "bromomethane" , su ESIS , accesso 4 febbraio 2010
- Programma delle Nazioni Unite per l'ambiente, Rapporto della trentesima riunione delle parti del protocollo di Montreal sulle sostanze che riducono lo strato di ozono, decisione XXX / 9: esenzioni per uso critico per il bromuro di metile per il 2019 e il 2020.
- Concimazione oceanica: mitigazione degli impatti ambientali della ricerca scientifica ; Canadian Science Advisory Secretariat Science Advisory Report 2010/012 (versione pubblicata nell'aprile 2010 e aggiornata: giugno 2010, con consultazione 2013-09-17); vedere pagina 9/15 del PDF
- Rapporto della trentesima riunione delle parti del Protocollo di Montreal sulle sostanze che impoveriscono lo strato di ozono, UNEP / Ozl.Pro.30 / 11, Allegato VI, al paragrafo 74.
- " divieto di estintori caricati con bromuro di metile " , su legifrance (accesso 23 gennaio 2021 )
- EFSA 12/01/11 < Peer Review della valutazione del rischio dei pesticidi della sostanza attiva bromuro di metile
- | http://www.ifen.fr/uploads/media/couche_ozone_01.pdf Dati di produzione attuali e futuri per la Francia]
- Meccanismo di ossidazione atmosferica del bromoetano
- Duniway, JM (2002). Stato delle alternative chimiche al bromuro di metile per la fumigazione del terreno preimpianto . Fitopatologia, 92 (12), 1337-1343.
- ANSES (2013) Analisi del rischio di parassiti Ditylenchus dipsaci su erba medica Parere ANSES Rapporto di valutazione collettiva degli esperti , aprile 2013, PDF, 146 pagine
link esterno
- (en) Scheda di dati di sicurezza dell'INRS (versione 2007)
- (en) Scheda informativa canadese sulla rimozione del bromuro di metile per la gestione sostenibile e integrata dei parassiti (PDF, 41p)
- MSDS : Database di sostanze chimiche pericolose
- ChemSub Online (Bromometano) .