Etanolo
| Etanolo | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Molecola di etanolo |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identificazione | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nome IUPAC | Etanolo | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sinonimi |
alcool etilico |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100.000.526 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CE | 200-578-6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Codice ATC | D08 , V03 , V03 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| DrugBank | DB00898 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 702 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ChEBI | 16236 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o E | E1510 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| FEMA | 2419 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SORRISI |
CCO , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1 / C2H6O / c1-2-3 / h3H, 2H2,1H3 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aspetto | liquido incolore con un odore caratteristico. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietà chimiche | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Formula bruta |
C 2 H 6 O [Isomeri] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Massa molare | 46,0684 ± 0,0023 g / mol C 52,14%, H 13,13%, O 34,73%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Momento dipolare | 1.66 D | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Diametro molecolare | 0,469 nm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietà fisiche | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fusione | −114 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° bollitura | 79 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solubilità | in acqua: miscibile, Completo in solventi polari e non polari ( acetone , etere dietilico ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Parametro di solubilità δ |
26,0 MPa 1/2 ( 25 ° C ); 11.2 cal 1/2 · cm -3/2 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Massa volumica |
0.789
equazione:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Temperatura di autoaccensione |
Da 423 a 425 ° C ; 363 ° C (a seconda delle sorgenti) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| punto d'infiammabilità | vaso chiuso: 13 ° C puro 17 ° C 95 % vol . 21 ° C 70 % vol . 49 ° C 10 % vol . 62 ° C 5 % vol . |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Limiti di esplosività in aria | Inferiore: 3,3 % vol Superiore: 19 % vol |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pressione del vapore saturo | a 20 ° C : 5,8 kPa
equazione:
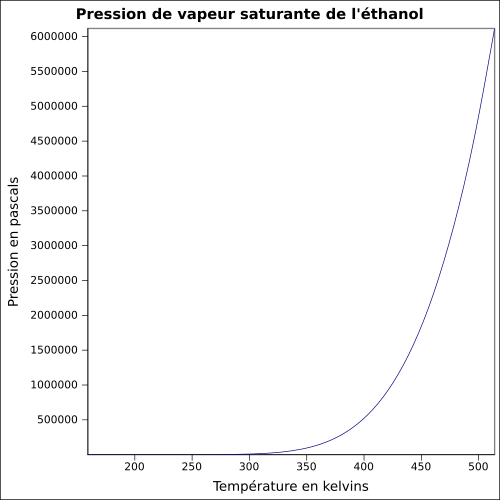
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Viscosità dinamica | 1,20 × 10 -3 Pa s a 20 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto critico | 240,85 ° C , 6,14 MPa , 0,168 l mol −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Velocità del suono | 1162 m s −1 a 20 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termochimica | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 liquido, 1 bar | 159,86 J · mol -1 · K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 gas | −235,3 kJ mol −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 liquido | −277,0 kJ mol −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C p |
111 J · K -1 · mol -1
equazione:
equazione:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PC | 1 366,8 kJ · mol -1 (liquido) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietà elettroniche | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 re energia di ionizzazione | 10,43 ± 0,05 eV (gas) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cristallografia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Classe di cristallo o gruppo spaziale | Pc | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Parametri della mesh |
a = 5,377 Å b = 6,882 Å |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volume | 298,57 Å 3 densità = 0,7893 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietà ottiche | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Indice di rifrazione | 1.3594. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Precauzioni | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Pericolo H225, P210, P305 + P351 + P338, P370 + P378, P403 + P235, H225 : Liquido e vapori facilmente infiammabili P210 : Tenere lontano da fonti di calore / scintille / fiamme libere / superfici riscaldate. - Vietato fumare. P305 + P351 + P338 : In caso di contatto con gli occhi: sciacquare accuratamente per parecchi minuti. Rimuovere le lenti a contatto se la vittima le indossa e possono essere rimosse facilmente. Continua a risciacquare. P370 + P378 : In caso di incendio: utilizzare ... per estinzione. P403 + P235 : conservare in un luogo ben ventilato. Stai calmo. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3 2 0 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Trasporto | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
33 : liquido altamente infiammabile (punto di infiammabilità inferiore a 21 ° C ) Numero ONU : 1170 : ALCOOL ETILICO contenente più del 24% di etanolo, in volume; SOLUZIONE DI ALCOL ETILICO contenente più del 24% di etanolo, in volume; ETANOLO contenente più del 24% di etanolo, in volume; o SOLUZIONE DI ETANOLO contenente più del 24% di etanolo, in volume Classe: 3 Etichetta: 3 : Liquidi infiammabili Confezione: Gruppo di imballaggio II : materiali mediamente pericolosi;  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Classificazione IARC | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gruppo 1: cancerogeno per l'uomo | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Inalazione | intossicazione, nausea, vomito | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pelle | nessun effetto | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Occhi | pericoloso | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ingestione | intossicazione, nausea, vomito, coma etilico (che può portare alla morte) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ecotossicologia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| DL 50 | Da 5 a 20 g kg −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CL 50 | Da 20.000 a 30.000 ppm per 4-6 ore | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LogP | -0.32 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Soglia di odore | basso: 49 ppm alto: 716 ppm |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dati farmacocinetici | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Metabolismo | nel fegato in etanale poi acido acetico , a ~ 100 mg kg -1 per ora | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Carattere psicotropo | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Categoria | Depressivo | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Modo di consumare |
Ingestione |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Altri nomi |
Alcol (vedi Bevande alcoliche ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rischio di dipendenza | Alunno | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Unità di SI e STP se non diversamente specificato. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
L' etanolo, o alcool etilico (o più semplicemente alcol ) è un alcol di formula strutturale CH 3 -CH 2 -OH. È un liquido incolore, volatile , infiammabile e miscibile con acqua in tutte le proporzioni. È una droga che altera la mente e una delle più antiche droghe ricreative , sotto forma di bevanda alcolica . L'etanolo è utilizzato dall'industria alimentare (per la produzione di alcolici in particolare), dalla profumeria e dai prodotti farmaceutici (come solvente ) nonché nei biocarburanti ( bioetanolo ). Viene anche utilizzato nei termometri ad alcool .
Formula
L'etanolo è un alcol primario a due atomi di carbonio della formula grezza C 2 H 6 Oe della formula semistrutturale CH 3 CH 2 OHo CH 3 -CH 2 -OH, indicando che il carbonio del gruppo metile (CH 3 -) è attaccato al gruppo metandiile (-CH 2 -) stesso attaccato al gruppo idrossile (-OH). È un isomero di costituzione dell'etere metilico . L'etanolo è solitamente designato dall'abbreviazione "EtOH", il gruppo etile (C 2 H 5 -) essendo comunemente abbreviato "E" in chimica organica .
Nome
L'etanolo è il nome sistematico definito dalla nomenclatura dei composti organici per una molecola con due atomi di carbonio (prefisso eth- ) aventi un unico legame tra loro (suffisso -ano ) e attaccati a un gruppo idrossile (suffisso -ol ).
Storia
La fermentazione degli zuccheri in etanolo è una delle più antiche biotecnologie utilizzate dall'uomo, soprattutto nell'industria degli alcolici ed è stata utilizzata fin dalla preistoria per ottenere bevande alcoliche . Analisi chimiche di composti organici assorbiti in vasi risalenti al periodo neolitico trovato in un villaggio nella provincia di Henan in Cina , ha rivelato che le miscele di bevande fermentate composto da riso, miele e frutta sono stati prodotti dal VII ° millennio aC. AD .
Anche se la distillazione è una tecnica nota alchimisti greco-egiziana (come Zosimo di Panopoli ), le prime testimonianze scritte di produzione di alcool da vino risale solo XII ° secolo con il lavoro degli alchimisti della scuola di Medicina di Salerno . La prima menzione della distinzione tra alcool assoluto miscele idroalcoliche e viene segnalato al XIII ° secolo da Raymond Lully . Si noti, tuttavia, che i persiani imparato Rhazes hanno isolato etanolo nella corrente X ° secolo.
Nel 1796 , Johann Tobias Lowitz ottenne etanolo puro filtrando etanolo distillato attraverso carbone attivo . Antoine Lavoisier determina che l'etanolo è composto da carbonio , ossigeno e idrogeno , e in 1808 , Nicolas Théodore de Saussure determina la sua formula grezza . Nel 1858 , Archibald Scott Couper pubblicato la struttura chimica di etanolo, che era una delle prime strutture determinate.
L'etanolo fu preparato sinteticamente per la prima volta nel 1826 dal lavoro indipendente di Georges Serullas in Francia e Henry Hennel nel Regno Unito . Nel 1828 , Michael Faraday sintetizzò l'etanolo mediante l' idratazione catalizzata dall'acido dell'etilene , una sintesi simile al processo industriale utilizzato oggi.
L'etanolo è stato utilizzato anche come carburante nelle lampade e come carburante per le automobili fino agli anni '30 . Ad esempio, la Ford T potrebbe funzionare fino al 1908 con etanolo puro.
Presenza naturale
L'etanolo è un sottoprodotto volatile del metabolismo del lievito . È quindi presente nell'habitat di questi organismi e nella nostra atmosfera. Si trova anche emesso dai frutti maturi, e in molte piante a causa di condizioni anaerobiche naturali durante la germinazione o quando piante prive di ossigeno (in caso di allagamento per esempio) traggono energia dalla fermentazione.
All'inizio degli anni 2000, il suo ciclo atmosferico era ancora poco conosciuto. Cerchiamo di quantificare l'etanolo emesso da piante e lieviti, i suoi livelli nell'atmosfera e il suo tasso di conversione tramite l'idrossile dell'aria (mediante titolazione del metilcloroformio ). Una prima stima approssimativa ha fornito un tasso di emissione di etanolo da parte degli impianti compreso tra 10 e 38 Tg / anno, ovvero un contributo importante alla stima di etanolo totale immesso in atmosfera annualmente (tra 25 e 56 Tg / anno). Poi un nuovo lavoro ha rivisto al rialzo le emissioni degli impianti: 70 Tg / anno (da 50 a 90 Tg / anno), circa il 75% dell'etanolo introdotto dall'aria essendo in realtà distrutto dalla reazione con i radicali idrossilici nell'aria secca o umida. Esistono anche depositi asciutti e umidi sulla terraferma.
L'etanolo è stato rilevato anche nello spazio , coprendo in forma solida granelli di polvere nelle nuvole interstellari .
Proprietà fisico-chimiche
L'etanolo è un liquido volatile , incolore che ha un odore. La sua combustione è priva di fumo e dà una fiamma bluastra. Le proprietà fisico-chimiche dell'etanolo derivano principalmente dalla presenza del gruppo idrossile e della corta catena di carbonio . Il gruppo idrossile può formare legami idrogeno , rendendo l'etanolo più viscoso e meno volatile rispetto ai solventi organici di peso molecolare equivalente. L' indice di rifrazione dell'etanolo è superiore a quello dell'acqua (1,3594 a 25,0 ° C ). Il punto triplo dell'etanolo si osserva a −123,15 ° C per una pressione di 4,3 × 10 −4 Pa .
Proprietà come solvente
L'etanolo è un solvente protico polare . È miscibile con molti solventi organici , come solventi clorurati ( tetracloruro di carbonio , cloroformio , tricloroetano , tetracloroetilene ), idrocarburi alifatici ( pentano , esano ), solventi aromatici ( benzene , toluene , piridina ), acido acetico , acetone , etere dietilico , il glicole etilenico o il nitrometano . Tuttavia, la miscibilità dell'etanolo con gli idrocarburi alifatici tende a diminuire con l'aumentare della lunghezza della catena di carbonio dell'alcano e la diminuzione della temperatura, il limite di miscibilità essendo ad esempio 13 ° C per il dodecano .
A causa della natura polare del gruppo idrossile , l'etanolo può anche sciogliere composti ionici , come idrossidi di sodio e di potassio , cloruri di magnesio , calcio e ammonio o bromuri di ammonio e sodio . I cloruri di sodio e di potassio sono solo leggermente solubili in etanolo.
La non polare parte di etanolo permette di dissolvere idrofobi sostanze , in particolare oli essenziali e molti odoroso, coloranti e composti medicinali.
L'etanolo può essere utilizzato come solvente in molte reazioni chimiche durante le sintesi , come nelle sostituzioni nucleofile di S N 1 , durante le idrogenazioni catalitiche , durante le reazioni aldoliche , durante le reazioni di Wittig , durante le reazioni di Diels. Ontano o durante le reazioni di diazotizzazione .
L'etanolo è inerte verso quasi tutte le superfici plastificate della vita quotidiana, le vernici (eccetto le vernici di cellulosa e quelle con gommalacca ), le pitture acriliche e gliceroftaliche pur essendo un ottimo solvente. Questo lo rende un solvente di pulizia ampiamente utilizzato da solo o in miscela con altri composti.
Miscibilità con l'acqua
Le miscele acqua-etanolo occupano un volume inferiore alla somma dei volumi dei due componenti presi singolarmente. La miscela di un volume di acqua e un volume di etanolo dà, ad esempio, un volume equivalente di 1,92. La reazione dell'acqua di miscelazione e dell'etanolo è esotermica e a 24,85 ° C possono essere rilasciati fino a 777 J mol −1 . La natura polare dell'etanolo lo rende igroscopico , tanto che, puro, assorbe l'umidità dall'aria.
Un azeotropo si forma con acqua all'89,47 moli% di etanolo e 10,53 moli% di acqua a pressione atmosferica . Il punto di ebollizione dell'etanolo è 78,4 ° C e 100 ° C per l'acqua, ma l'azeotropo bolle a 78,2 ° C , che è al di sotto dei punti di ebollizione di ciascun costituente. Le proporzioni della miscela azeotropica variano in funzione della pressione.
| Pressione | Punto di ebollizione | Frazione molare di etanolo |
|---|---|---|
| 0,1 MPa | 78,35 ° C | 0.894 |
| 0,344 MPa | 112,6 ° C | 0.882 |
| 0.689 MPa | 135,7 ° C | 0.874 |
| 1.378 MPa | 164,2 ° C | 0.862 |
| 2.068 MPa | 182,6 ° C | 0.852 |
L'aggiunta di una piccola percentuale di etanolo all'acqua riduce drasticamente la tensione superficiale dell'acqua. Questa proprietà aiuta a spiegare il fenomeno delle lacrime del vino . Quando si fa roteare il vino in un bicchiere, l'etanolo evapora più rapidamente nella pellicola sottile lungo i lati del bicchiere. La proporzione di etanolo diminuisce, quindi la tensione superficiale aumenta e il film si trasforma in goccioline. Questo fenomeno è chiamato effetto Marangoni , ed è stato descritto e spiegato nel 1855 da James Thomson.
La gradazione alcolica , chiamato anche gradazione alcolica è il rapporto tra il volume di alcole contenuto nella miscela e il volume totale della miscela a 20 ° C . Viene utilizzato per determinare la proporzione di alcol, cioè etanolo, in una bevanda alcolica . L'unità utilizzata per esprimere il titolo è la frazione di volume (% vol) o il grado (indicato con "°").
Le miscele acqua-etanolo contenenti più del 50% di etanolo sono infiammabili a temperatura ambiente , ma riscaldando una miscela contenente meno del 50% di etanolo può incendiarsi. La tecnica di cottura utilizza questa proprietà. L'alcol aggiunto in una padella calda brucia nelle fiamme e dà una reazione complessa. La temperatura dell'alcol che brucia può quindi superare i 240 ° C e porta alla caramellizzazione degli zuccheri presenti.
Produzione
L'etanolo può essere prodotto industrialmente da petrolchimica per idratazione di etilene , e da fermentazione alcolica di lieviti o cellulosa . Il processo più economico dipende principalmente dal mercato del petrolio .
Catalisi diretta
Questo processo, sviluppato negli anni '70, ha completamente soppiantato altri metodi di produzione. L'etanolo così prodotto viene utilizzato dall'industria come materia prima o come solvente . Esso è prodotto attraverso la petrolchimica , utilizzando idratazione da acido catalisi di etilene , dopo la reazione:
H 2 C = CH 2+ H 2 O↔ CH 3 CH 2 OHIl catalizzatore più comunemente usato è l'acido fosforico , adsorbito su un poroso di supporto quali il gel di silice o celite . Un aumento della pressione aiuta a spostare l' equilibrio verso la produzione di etanolo, seguendo il principio di Le Chatelier , ed è quindi utilizzare un catalizzatore ad alta pressione di vapore acqueo per avvicinarsi rapidamente all'equilibrio. Il prodotto finale è una miscela acqua-etanolo contenente tra il 10 % e il 25 % di etanolo.
Catalisi indiretta
Un processo in precedenza, ma ormai obsoleto, sviluppato negli anni 1930 da Union Carbide , e sarà utilizzato per gran parte del XX ° secolo . L' etilene viene esterificata da acido solforico per produrre solfato di etile , che viene poi idrolizzato per produrre etanolo ed acido solforico, che funge così da catalizzatore in questa reazione:
H 2 C = CH 2+ H 2 SO 4→ CH 3 CH 2 SO 4 H CH 3 CH 2 SO 4 H+ H 2 O→ CH 3 CH 2 OH+ H 2 SO 4Questo processo consuma grandi quantità di acido solforico e richiede una miscela di gas di buona qualità come input.
Fermentazione
L'etanolo utilizzato nelle bevande alcoliche è prodotto dalla fermentazione alcolica . Allo stesso modo, la maggior parte del bioetanolo proviene dal trattamento di fermentazione di piante da zucchero, come barbabietole e canna da zucchero , o cereali, come mais e frumento . Alcuni tipi di lievito , come il Saccharomyces cerevisiae , metabolizzano gli zuccheri in etanolo e anidride carbonica , seguendo queste reazioni:
C 6 H 12 O 6→ 2 CH 3 CH 2 OH+ 2 CO 2 C 12 H 22 O 11+ H 2 O→ 4 CH 3 CH 2 OH+ 4 CO 2La fermentazione è il lievito in coltura in condizioni favorevoli per produrre l'alcol, ad una temperatura di circa 35 per il 40 ° C . I ceppi di lievito più resistenti possono sopravvivere a una concentrazione di circa il 15 % in volume di etanolo. La tossicità dell'etanolo per il lievito limita la concentrazione di alcol che può essere ottenuta mediante fermentazione e concentrazioni più elevate possono essere ottenute mediante mutage o distillazione . Durante la fermentazione si formano prodotti secondari, come il glicerolo , dell'acido succinico , dell'acido acetico e dell'alcool amilico .
Per produrre etanolo dall'amido , ad esempio dai semi di cereali, deve prima essere convertito in zuccheri. Durante la preparazione della birra, un seme può germogliare ( maltaggio ), il che consente la produzione di alcuni enzimi, come citasi , amilasi , fosfatasi o peptidasi , necessari per la saccarificazione dell'amido. Per il bioetanolo , questo processo può essere accelerato utilizzando acido solforico o utilizzando un'amilasi prodotta da funghi.
Etanolo cellulosico
La fermentazione può essere ottenuta anche dalla cellulosa , ma fino a tempi recenti il costo della cellulasi , un enzima in grado di scomporre la cellulosa, non consentiva all'industria di svilupparsi industrialmente. Nel 2004 , la società canadese Iogen Corporation ha costruito il primo impianto basato sulla produzione di etanolo dalla cellulosa. Lo sviluppo di questa tecnologia potrebbe consentire di utilizzare e riciclare molti scarti vegetali provenienti dall'agricoltura contenenti cellulosa, come segatura o paglia . Altre aziende biotecnologiche stanno sviluppando funghi in grado di produrre grandi quantità di cellulasi e xilanasi per consentire di convertire altri residui agricoli in cellulosa, come il mais di scarto o la bagassa dalla canna da zucchero .
Purificazione
I vari processi di produzione di etanolo producono miscele acqua-etanolo. Per l'uso nell'industria o come combustibile, l'etanolo deve essere purificato. La distillazione frazionata può concentrarsi etanolo al 95,6 % in volume (89,5 mol% ), e forma una miscela azeotropica con acqua il cui punto di ebollizione è 78,2 ° C . I metodi usuali per ottenere etanolo assoluto includono l'uso di essiccanti , come amido , glicerolo o zeoliti , distillazione azeotropica e distillazione estrattiva .
Qualità dell'etanolo
Sono disponibili diversi gradi di etanolo per diversi usi:
- l' alcol denaturato è generalmente etanolo al quale viene aggiunto un denaturante per rendere la miscela inadatta al consumo alimentare. I denaturanti utilizzati possono essere alcool isopropilico , metanolo , dietilftalato , tiofene , etere dietilico oppure condensati di gas naturale . Viene utilizzato per le pulizie, la pulizia, la disinfezione e nelle stufe ad alcool . Solvente da ebanista per le sue vernici a gommalacca , è anche uno sgrassante nel settore, apprezzato per la sua bassa tossicità sulla pelle. Generalmente al 95 % vol ;
- l' alcol metilato è una miscela di etanolo e metanolo . Lo spirito metilato è altamente tossico a causa della presenza di metanolo (generalmente dal 5 al 10 % vol ). Si usa per pulire vetri e superfici in plastica;
- l' alcol rettificato è un distillato che misura dal 70 al 96% vol di etanolo utilizzando il metodo della distillazione frazionata . La concentrazione massima ottenibile per distillazione dell'alcool grezzo è del 96 % vol per la formazione di un azeotropo acqua-etanolo. È usato per fare liquori o vodka , ma anche per la manutenzione, la pulizia o la disinfezione della casa;
- l' etanolo assoluto è etanolo contenente al massimo l'1% di acqua, ma la maggior parte dei principali fornitori di prodotti chimici vende con il termine etanolo assoluto al 99,8%. Viene utilizzato come solvente per applicazioni industriali e di laboratorio e come combustibile;
- L' etanolo anidro è l'etanolo da cui l'acqua è stata rimossa il più possibile. Ad esempio, la reazione dell'etanolo assoluto con il magnesio metallico seguita dalla distillazione a pressione atmosferica produce etanolo a 50 ppm di acqua (0,005% di acqua in massa o 1 / 20.000). Questo grado di etanolo ne consente l'utilizzo in reazioni sensibili all'umidità.
Reattività e reazioni
L'etanolo è un alcol primario e un acido debole ( p K a = 15,5) la cui base coniugata è l' etanolato . È anche un buon nucleofilo , grazie alla reattività dei doppietti non leganti l' ossigeno. La sua reattività, dovuta principalmente alla presenza del gruppo idrossile , può comportare reazioni di disidratazione , deidrogenazione , ossidazione ed esterificazione .
Chimica acido-base
L'etanolo è una molecola neutra e il pH di una soluzione di etanolo in acqua è 7,00. L'etanolo può essere convertito quantitativamente nella sua base coniugata , lo ione etanolato , facendolo reagire con un metallo alcalino , come il sodio :
2 CH 3 CH 2 OH+ 2 Na→ 2 CH 3 CH 2 ONa+ H 2o con una base forte , come l'idruro di sodio :
CH 3 CH 2 OH+ NaH→ CH 3 CH 2 ONa+ H 2Esterificazione
L'etanolo reagisce con gli acidi carbossilici in presenza di un acido forte ( catalisi ) dando esteri etilici e acqua secondo la seguente reazione:
RCOOH+ CH 3 CH 2 OH→ RCOOCH 2 CH 3+ H 2 OQuesta reazione è reversibile e l' equilibrio viene raggiunto lentamente, richiedendo l'uso di catalizzatori acidi, come acido solforico , acido cloridrico , trifluoruro di boro o acido paratoluensolfonico . Per ottenere rese corrette, questa reazione, utilizzata nell'industria su larga scala, richiede la rimozione dell'acqua dalla miscela di reazione quando si forma. L'etanolo può anche formare esteri con acidi inorganici e consente di preparare composti ampiamente utilizzati nella sintesi organica , come il dietil solfato (C 2 H 5 ) 2 SO 4o trietilfosfato (C 2 H 5 ) 3 PO 4. Il nitrito etilico CH 3 CH 2 O-N = Opuò anche essere preparato da etanolo e nitrito di sodio , ed era comunemente usato come diuretico o rimedio per l' influenza o il comune raffreddore , prima di essere ritirato dal mercato all'inizio degli anni '80 .
La reazione di saponificazione , che consente di riformare l'etanolo da esteri etilici in presenza di un acido o una base per dare un carbossilato , viene utilizzata per la preparazione di saponi .
Disidratazione
L'uso di acidi forti può consentire la disidratazione dell'etanolo per formare etere dietilico e ogni anno vengono prodotte diverse tonnellate di etere dietilico utilizzando acido solforico come catalizzatore . La reazione può essere descritta come segue:
2 CH 3 CH 2 OH→ CH 3 CH 2 OCH 2 CH 3+ H 2 O(a 120 ° C )L' etilene è il prodotto principale quando la temperatura supera i 160 ° C :
CH 3 CH 2 OH→ H 2 C = CH 2+ H 2 OCombustione
La combustione dell'etanolo è fumo e dà una fiamma bluastra. La reazione di combustione forma anidride carbonica e vapore acqueo :
CH 3 CH 2 OH( l ) + 3 O 2( g ) → 2 CO 2( g ) + 3 H 2 O( g )Il potere calorifico (Δ c H °) della combustione dell'etanolo è 1366,8 kJ mol −1 a 25 ° C e la capacità termica specifica (C v ) è 2,438 kJ kg −1 K −1 .
Ossidazione
L' ossidazione (o deidrogenazione ) dell'etanolo in presenza di catalizzatori permette di ottenere etanale (o acetaldeide ), secondo la seguente reazione:
CH 3 CH 2 OH→ CH 3 CHO+ H 2Negli epatociti del fegato , l'enzima alcol deidrogenasi converte in modo simile l'etanolo in etanale. L'etanale è più tossico dell'etanolo e potrebbe essere responsabile di molti sintomi di sbornia , sebbene non sia presente nel sangue durante i sintomi. Nel cervello , l'alcol deidrogenasi ha un ruolo minore nella conversione dell'etanolo in etanale ed è l'enzima catalasi che catalizza principalmente questa reazione.
Le fasi finali della fermentazione alcolica comportano la conversione del piruvato in etanale da parte dell'enzima piruvato decarbossilasi , seguita dalla riduzione (o idrogenazione ) dell'etanale in etanolo da parte dell'enzima alcol deidrogenasi , catalizzando in questo caso la reazione opposta. Essendo un metabolita endogeno, l'etanale è tossico ed è un sospetto cancerogeno. Danneggia le cellule staminali ematopoietiche (responsabili del costante rinnovamento del sangue ); da un lato è la fonte delle rotture nel DNA a doppia elica di queste cellule (che ne favorisce il declino e crea riarrangiamenti cromosomici ), e dall'altro impedisce la corretta riparazione ( p. 53 ) di questo danno, che provoca tumori maligni.
Alogenazione
L'etanolo reagisce con gli acidi idroalici per produrre aloalcani , come il cloroetano e il bromoetano , tramite una reazione S N 2 :
CH 3 CH 2 OH+ HCl→ CH 3 CH 2 Cl+ H 2 OQuesta reazione richiede l'uso di un catalizzatore , come il cloruro di zinco . Gli alogenuri alchilici possono anche essere sintetizzati utilizzando agenti alogenanti come il cloruro di tionile o il tribromuro di fosforo :
CH 3 CH 2 OH+ SOCl 2→ CH 3 CH 2 Cl+ COSÌ 2+ HClReazione aloformica
La reazione aloformio è una reazione chimica che consiste nella sintesi di un trihalogenomethane , come il cloroformio (CHCl 3), bromoformio (CHBr 3) o iodoformio (CHI 3), ed è una delle più antiche reazioni organiche descritte come tali. Nel 1822 , Georges Serullas riferì la reazione dell'etanolo con diodio e idrossido di sodio in acqua, formando sodio formiato e iodoformio , allora chiamato "idroioduro di carbonio".
L'etanolo reagisce con l'ipoclorito di sodio per dare cloroformio, secondo la seguente sintesi:
CH 3 CH 2 OH+ NaClO→ CH 3 CHO+ NaCl+ H 2 O CH 3 CHO+ 3 NaOCl→ CCl 3 CHO+ 3 NaOH CCl 3 CHO+ NaOH→ CHCl 3+ HCO 2 NaAllo stesso modo, bromoformio e iodoformio si ottengono rispettivamente da ipobromito di sodio e ipoiodito di sodio. L'etanolo è l'unico alcol primario che consente questa reazione.
uso
Carburante
L'etanolo prodotto in tutto il mondo viene utilizzato principalmente come carburante . La quantità di etanolo può variare da una piccola percentuale di benzina nell'Europa occidentale al 95 % in volume di benzina in Brasile , dove il 90% dei nuovi veicoli utilizza la tecnica del carburante flessibile e può funzionare con questa miscela. Oltre il 66% dell'etanolo utilizzato come combustibile proviene dalla fermentazione alcolica .
Il carburante E85 distribuito in Francia contiene tra il 65% e l'85% di bioetanolo, il resto è benzina; il tasso varia tra il 65% e il 75% in inverno e raggiunge l'85% in estate.
Associato all'acqua, è stato il carburante per molti aeroplani ( motori a combustione interna ) e razzi durante la seconda guerra mondiale, per i paesi con poche risorse di petrolio.
In Francia, l'1% del territorio è destinato al bioetanolo. Dei diciotto milioni di ettolitri prodotti ogni anno in Francia, dodici milioni sono utilizzati per la fabbricazione di biocarburanti, di cui il 30% sono commercializzati al di fuori della Francia. Degli otto milioni di ettolitri di bioetanolo destinati ai biocarburanti in Francia, un milione (o il 12%) viene utilizzato nel carburante E85 . Una piccola quantità di etanolo viene anche utilizzata per produrre ED95 (95% di bioetanolo e 5% di additivo pro-cetano) per veicoli pesanti a motore specifico (compresi autobus e pullman).
Bevande alcoliche
Il contenuto di etanolo (o grado di alcol ) delle bevande alcoliche varia a seconda del modo di produzione e della materia prima. La maggior parte delle bevande alcoliche può essere classificata tra bevande fermentate e superalcolici . Le principali bevande fermentate sono le birre , prodotte da cereali o altre piante produttrici di amido , vini e sidri , prodotti da succo di frutta e idromele , prodotto dal miele . Gli spiriti sono prodotti distillando bevande fermentate . Siamo in grado di distinguere i diversi tipi di bevande spiritose , come il whisky , distillati da semi di cereali fermentato, eaux-de-vie , distillato dal succo fermentato di frutta, o il rum , distillato da melassa o succo di frutta. Di canna da zucchero . Molti eaux-de-vie e liquori sono preparati anche da infusione di frutta, erbe e spezie in bevande alcoliche , come il gin che viene creato infondendo ginepro bacche in alcole rettificato .
Altri metodi possono essere utilizzati per aumentare il livello di alcol , come la solidificazione frazionata , che viene utilizzata per preparare il jack di mela dal succo di mela. Il vino liquoroso viene preparato aggiungendolo all'acqua della vita o ad altri liquori al vino parzialmente fermentato, metodo che uccide i lieviti mantenendo parte degli zuccheri.
Le bevande alcoliche sono utilizzate in cucina per il loro profumo e perché l'alcol scioglie i composti odorosi idrofobici . L'etanolo di queste bevande viene utilizzato anche per produrre aceto , allo stesso modo in cui viene utilizzato l'etanolo industriale per la produzione di acido acetico .
Materiale grezzo
L'etanolo è un importante intermedio sintetico nell'industria chimica . Viene utilizzato in particolare durante la preparazione di alogenuri etilici, esteri etilici , ammine etiliche , etere dietilico , acido acetico e, in misura minore, butadiene .
Antisettico
L'etanolo è utilizzato in campo medico nelle compresse come antisettico . Viene utilizzato anche in soluzioni idroalcoliche ad una concentrazione di circa il 60 % vol . L'etanolo uccide gli organismi denaturando le loro proteine e dissolvendo i loro lipidi. È efficace contro la maggior parte dei batteri e funghi , molti virus , ma è inefficace contro le spore .
Solvente
L'etanolo è miscibile con l'acqua ed è un buon solvente . Può essere trovato in pitture , tinte industriali, vernici tradizionali, bevande alcoliche , pennarelli e nei cosmetici come profumi e deodoranti .
Uso medico
L' etanolo assoluto è talvolta iniettato in tumori al fine di provocare la necrosi . Tuttavia, non ha un'attività mirata poiché provoca indiscriminatamente la necrosi dei tessuti sani e cancerosi.
L'etanolo è anche usato per trattare l' avvelenamento da metanolo o glicole etilenico . In questi casi, l'etanolo compete con altri alcoli per essere metabolizzato dall'enzima alcol deidrogenasi , riducendo così i derivati tossici che derivano dalla loro metabolizzazione in aldeidi e acidi carbossilici , e riducendo gli effetti tossici dovuti alla cristallizzazione dell'ossalato di calcio (da glicole etilenico ) nei reni .
Usi storici
Prima dello sviluppo dei farmaci moderni, l'etanolo veniva utilizzato per vari scopi medici, incluso il trattamento della depressione e come anestetico . È anche noto per essere in grado di servire come siero della verità .
Come carburante , è stato utilizzato nei motori a razzo combinato con ossigeno liquido . Durante la seconda guerra mondiale , il missile tedesco " V2 " utilizzava etanolo miscelato con il 25 % in volume di acqua per abbassare la temperatura della camera di combustione . Il missile balistico americano " PGM-11 Redstone ", ispirato al design del V2 tedesco, utilizzava anche etanolo miscelato con ossigeno liquido . I combustibili a base di alcol per razzi e missili sono successivamente caduti in disuso con lo sviluppo di nuovi combustibili.
Farmacologia
Le due principali vie del metabolismo dell'etanolo nel fegato sono l' alcol deidrogenasi e il sistema di ossidazione dell'etanolo microsomiale (in) . A basse concentrazioni di etanolo, l' alcol deidrogenasi ossida l'etanolo in acetaldeide , ma a concentrazioni più elevate, o con dosi ripetute di etanolo, predomina il sistema di ossidazione dell'etanolo microsomiale.
Nella farmacopea europea , "etanolo" designa etanolo anidro, vale a dire puro al 100%, in contrasto con il 95 % vol o il 70 % vol di etanolo che si trova nelle farmacie . A questo si aggiunge la qualità “alcool Ph. Eur. "(For European Pharmacopoeia ), che designa una qualità di etanolo per la quale sono state quantificate numerose tracce e impurità.
Proprietà fisiologiche
Ci sono diversi effetti delle bevande alcoliche , con l' alcolismo che è il consumo eccessivo di bevande contenenti etanolo che porta alla dipendenza, che classifica l'etanolo come droga. Questa sarebbe la droga più dannosa per le società.
| Livello di alcol nel sangue ( g · l –1 ) |
Grado alcolico ( % vol ) |
Sintomi |
|---|---|---|
| 0,5 | 0,05 | Euforia, rilassamento |
| 1.0 | 0.1 | Depressione, nausea, vomito, diminuzione delle capacità sensoriali e motorie, rallentamento della cognizione |
| > 1.4 | > 0,14 | Diminuzione del flusso sanguigno al cervello |
| 3.0 | 0.3 | Perdita di conoscenza |
| 4.0 | 0.4 | Possibile morte |
| 5.5 | 0,55 | Morte |
Alcol nel sangue
Il BAC è la quantità di etanolo nel sangue; è generalmente espresso in grammi per litro di sangue. Livelli di alcol nel sangue superiori a 4,0 g L −1 possono essere fatali e il livello diventa letale oltre 5,5 g L −1 . Basse dosi di etanolo, inferiori a 0,5 g L -1 , provocano una sensazione di euforia , con le persone che diventano più loquaci, meno inibite e mostrano ridotte capacità analitiche. A dosi maggiori, sopra 1.0 g L -1 , etanolo agisce come un sedativo sul sistema nervoso centrale , sintomi coinvolgono rallentato cognizione , diminuita sensoriali e motorie funzione, perdita di coscienza , fino alla morte.
Effetti sul sistema nervoso centrale
L'etanolo è un depressivo del sistema nervoso centrale ed è considerato un farmaco psicotropo . Agisce sul sistema nervoso centrale interagendo principalmente con i recettori GABA A , aumentando l'effetto inibitorio del neurotrasmettitore acido γ-aminobutirrico (o GABA). GABA rallenta l'attività dei neuroni (a differenza del glutammato che è un acceleratore di informazioni); quindi, legandosi ai recettori GABA, l'etanolo esagera il rallentamento del cervello . Agisce quindi come un modulatore allosterico positivo . L'etanolo agisce anche sui recettori della serotonina , glutammato , acetilcolina e dopamina . I suoi effetti negativi possono essere esacerbati dal piombo che aumenta lo stress ossidativo . Il piombo potenzia l'effetto dell'alcol sul sistema nervoso centrale (SNC).
Il consumo prolungato di etanolo può quindi causare danni permanenti al cervello e ad altri organi. L' astinenza da alcol può causare vari sintomi quali disturbo da deficit di attenzione , aumento della sudorazione, tachicardia , tremori di (tremore delle estremità), talvolta nausea o vomito, disidratazione, malessere , ipertensione . A volte è accompagnato da convulsioni , allucinazioni visive, tattili o uditive, è delirium tremens nella sua forma più grave. Alla fine, e in rari casi, può comparire dolore dalla mascella al cranio. È stato anche dimostrato che l'etanolo causa cambiamenti nelle dimensioni della materia grigia visibile ad occhio nudo .
Effetti sul metabolismo
In quanto tale, l'etanolo è un nutriente . Nel corpo umano, viene metabolizzato in acetaldeide dall'enzima alcol deidrogenasi . L'acetaldeide viene successivamente convertita dall'acetaldeide deidrogenasi in acetil-coenzima A , che è il prodotto finale del metabolismo dei carboidrati e dei lipidi . Tuttavia, l'acetaldeide stessa è molto più tossica dell'etanolo ed è in parte responsabile della maggior parte degli effetti clinici dell'alcol, come i postumi di una sbornia . In particolare, è stato dimostrato di aumentare il rischio di cirrosi del fegato ed è collegata a molte forme di cancro .
Effetti a lungo termine
L'etanolo è classificato come un teratogeno agente , e può indurre la sindrome alcolica fetale , che è l'alcol avvelenamento del dell'embrione o del feto a causa di consumo di alcol della madre durante la gravidanza , e che interrompe organi di sviluppo.
Il consumo regolare di alcol è anche un fattore che contribuisce all'aumento dei trigliceridi nel sangue che favorisce la comparsa di malattie cardiovascolari .
L'etanolo nelle bevande alcoliche è considerato un cancerogeno definito ed è quindi uno degli agenti cancerogeni del gruppo 1 IARC .
Interazioni farmacologiche
L'etanolo può aumentare il fenomeno di sedazione causato da farmaci depressivi che agiscono sul sistema nervoso centrale , come i barbiturici , le benzodiazepine , gli oppioidi , le fenotiazine e gli antidepressivi .
Note e riferimenti
- (fr) Questo articolo è parzialmente o interamente tratto dall'articolo di Wikipedia in inglese intitolato " Ethanol " ( vedere l'elenco degli autori ) .
- ETANOLO (ANHYDRO) , scheda / e di sicurezza del Programma internazionale sulla sicurezza chimica , consultato il 9 maggio 2009
- (a) Y. Marcus , The Properties of Solvents , Chichester, England, John Wiley & Sons , al. "Solution Chemistry" ( n o 4),1998, 254 p. ( ISBN 978-0-471-98369-9 e 0471983691 , LCCN 98018212 , presentazione in linea ) , p. 95
- Marcus, 1998 , p. 88.
- massa molecolare calcolata dal " peso atomico degli elementi 2007 " su www.chem.qmul.ac.uk .
- (in) James E. Mark, Physical Properties of Polymer Handbook , Springer,2007, 2 ° ed. , 1076 p. ( ISBN 978-0-387-69002-5 e 0-387-69002-6 , leggi online ) , p. 294
- (in) Serban Moldoveanu, Preparazione del campione in cromatografia , Amsterdam / Boston, Elsevier ,2002, 930 p. ( ISBN 0-444-50394-3 ) , p. 258
- " Scheda tossicologica FT 48 - Etanolo " , sul sito web dell'Istituto Nazionale di Ricerca e Sicurezza per la prevenzione degli infortuni sul lavoro e delle malattie professionali ,2011(visitato il 14 maggio 2012 ) .
- (in) RH Perry e DW Verde , Chemical Engineers' Handbook di Perry , McGraw-Hill ,1997, 7 ° ed. , 2640 p. ( ISBN 978-0-07-049841-9 , LCCN 96051648 ) , p. 2-50.
- (in) CA Faúndez e OJ Valderrama , " Activity Coefficient Models to Describe Vapor-Liquid Equilibrium in Ternary Hydro-Alcoholic Solutions " , Chin. J. Chem. Eng. , vol. 17, n o 2aprile 2009, p. 259-267 ( ISSN 1004-9541 , DOI 10.1016 / S1004-9541 (08) 60203-7 )
- (a) William M. Haynes , CRC Handbook of Chemistry and Physics , Boca Raton, CRC Press / Taylor e Francis,1 ° luglio 2010, 91 ° ed. , 2610 p. ( ISBN 9781439820773 , presentazione online ) , p. 14-40
- (a) O. Haida , H. Suga et al. , “ Studio calorimetrico dello stato vetroso XII. Fenomeni di transizione vetrosa plurale dell'etanolo " , J. Chem. Termodinamica. , vol. 9, n o 12,Dicembre 1977, p. 1133–1148 ( ISSN 0021-9614 , DOI 10.1016 / 0021-9614 (77) 90115-X ).
- (in) J. Chao e FD Rossini , " Calori di combustione, addestramento e isomerizzazione degli alcanoli diciannove " , J. Chem. Eng. Dati , vol. 10, n o 4,1965, p. 374–379 ( ISSN 0021-9568 , DOI 10.1021 / je60027a022 ).
- (in) Carl L. Yaws, Handbook of Thermodynamic Diagrams: Organic Compounds C8 to C28 , vol. 1, Huston, Texas, Gulf Pub. Co.,1996, 396 p. ( ISBN 978-0-88415-857-8 , LCCN 96036328 )
- (a) David R. Lide , CRC Handbook of Chemistry and Physics , Boca Raton, CRC Press,18 giugno 2002, 83 ° ed. , 2664 p. ( ISBN 0849304830 , presentazione online ) , p. 5-89
- (a) David R. Lide , CRC Handbook of Chemistry and Physics , Boca Raton, CRC Press / Taylor e Francis,17 giugno 2008, 89 ° ed. , 2736 p. ( ISBN 9781420066791 , presentazione online ) , p. 10-205
- " Ethanol " , su reciprocalnet.org (visitato il 12 dicembre 2009 )
- [1]
- Gruppo di lavoro IARC sulla valutazione dei rischi cancerogeni per l'uomo, " Valutazioni globali di cancerogenicità per l'uomo, Gruppo 1: Cancerogeno per l'uomo " , su http://monographs.iarc.fr , IARC,16 gennaio 2009(visitato il 22 agosto 2009 )
- Scheda dati di sicurezza fornita da Sigma-Aldrich, consultata il 28/09/2019
- " Ethyl alcohol " , su hazmap.nlm.nih.gov (visitato il 14 novembre 2009 )
- " ESIS " (visitato il 6 dicembre 2008 )
- (in) GP Moss (a cura di ), " Terminologia di base della stereochimica " , Pure Appl. Chem. , IUPAC , vol. 68, n o 12,1996, p. 2193-2222 ( ISSN 0033-4545 e 1365-3075 , DOI 10.1351 / pac199668122193 ).
- (en) PE McGovern , J. Zhang et al. , " Bevande fermentate della Cina pre- e protostorica " , Proc. Natl. Acad. Sci. USA , vol. 101, n o 51,21 dicembre 2004, p. 17593-17598 ( ISSN 0027-8424 , PMID 15590771 , PMCID PMC539767 , DOI 10.1073 / pnas.0407921102 , leggi online ).
- (it) RJ Forbes , Breve storia del l'arte della distillazione: dalle origini fino alla morte di Cellier Blumenthal , Leiden, Paesi Bassi, Brill ,1970, 2 ° ed. ( 1 ° ed. 1948), 405 p. ( ISBN 978-90-04-00617-1 , presentazione online , leggi online ) , p. 89.
- " Mohammad Ibn Zakariâ Râzi (865-925), Il più eminente medico della civiltà islamica - La Revue de Téhéran | Iran " , su www.teheran.ir (consultato il 9 luglio 2016 )
- (in) " Alcohol " , sul sito dell'Encyclopaedia Britannica ,1911(visitato il 12 maggio 2012 ) .
- (in) AS Cut , " era New Chemical Theory " , Philos. Mag. , 4 th serie, vol. 16,1858, p. 104-116 ( ISSN 1478-6435 , leggi in linea ).
- (in) H. Hennell , " Sull'azione reciproca dell'acido solforico e dell'alcol, con osservazioni sulla composizione e le proprietà del composto risultante " , Philos. Trans. R. Soc. , vol. 116,9 marzo 1826, p. 240-249 ( DOI 10.1098 / rstl.1826.0021 , leggi online ).
- (in) Joseph DiPardo, " Outlook for Biomass Ethanol Production and Demand " , su Energy Information Administration (visitato il 14 maggio 2012 )
- (in) VD Hunt , The gasohol handbook , New York Industrial Press,diciannove ottantuno, 580 p. ( ISBN 978-0-8311-1137-3 , presentazione online ).
- (in) R. Dudley , " Ethanol Fruit Matening, and the Historical Origins of Human Primate Alcoholism in Frugivory " , Integr. Comp. Biol. , vol. 44, n o 4,2004, p. 315-323 ( ISSN 1540-7063 , DOI 10.1093 / icb / 44.4.315 ).
- Kreuzwieser J, Papadopoulou E & Rennenberg H (2004) Interaction of flooding with carbon metabolism of forest trees , Plant Biol., 6, 299-306, 2004
- Kimmerer TW e MacDonald RC (1987) Biosintesi di acetaldeide ed etanolo nelle foglie delle piante , Plant Physiol., 84, 1204–1209
- (in) S. Leblová E. Sineckáet et al. , " Metabolismo del piruvato nella germinazione dei semi durante l'anaerobiosi naturale " , Biol. Plantarum , vol. 16, n o 6,1974, p. 406-411 ( ISSN 0006-3134 , DOI 10.1007 / BF02922229 ).
- Kirstine WV & Galbally IE (2011) L'etanolo del bilancio atmosferico globale rivisitato ; Chimica e fisica dell'atmosfera 11 (1): 25909-25936 | Settembre | DOI: 10.5194 / acpd-11-25909-2011
- (in) A. Schriver , L. Schriver-Mazzuoli et al. , " Una possibile origine dell'etanolo nel mezzo interstellare: fotochimica di pellicole CO 2 –C 2 H 6 miste a 11 K. Uno studio FTIR " , Chem. Phys. , vol. 334, n osso 1-3,2007, p. 128-137 ( DOI 10.1016 / j.chemphys.2007.02.018 ).
- (en) M. Windholz (a cura di ), The Merck Index: An Encyclopedia of Chemicals and Drugs , vol. 9, Merck ,1976, 9 ° ed. , 1835 p. ( ISBN 978-0-911910-26-1 ).
- (en) U. Dahlmann e GM Schneider , " (Liquido + liquido) equilibri di fase e curve critiche di (etanolo + dodecano o tetradecano o esadecano o 2,2,4,4,6,8,8-eptametilnonano) da 0 , Da 1 MPa a 120,0 MPa " , J. Chem. Termodinamica. , vol. 21, n o 9,Settembre 1989, p. 997-1004 ( ISSN 0021-9614 , DOI 10.1016 / 0021-9614 (89) 90160-2 ).
- (in) C. Reichardt e T. Welton , Solvents and solvent effects in organic chemistry , Weinheim, Wiley-VCH ,2010, 4 ° ed. , 692 p. ( ISBN 978-3-527-32473-6 , DOI 10.1002 / 9783527632220 , presentazione in linea ) , "Appendice" , p. 568.
- (en) JE Logsdon , Kirk-Othmer Encyclopedia of Chemical Technology , John Wiley & Sons ,2004( ISBN 978-0-471-23896-6 , DOI 10.1002 / 0471238961.0520080112150719.a01.pub2 , leggi online ) , "Etanolo".
- (en) MJ Costigan , LJ Hodges et al. , " Il calorimetro a spostamento isotermico: modifiche progettuali per la misurazione delle entalpie esotermiche di miscelazione " , Aust. J. Chem. , vol. 33, n o 10,1980, p. 2103-2119 ( ISSN 0004-9425 , DOI 10.1071 / CH9802103 ).
- (in) RW Rousseau , Handbook of Separation Process Technology , John Wiley & Sons ,1987, 1010 p. ( ISBN 978-0-471-89558-9 , leggi online ) , p. 261–262.
- J. Vidal , Termodinamica: applicazione di ingegneria chimica e l'industria del petrolio , Paris, Éditions Technip ,1997, 500 p. ( ISBN 978-2-7108-0715-5 , LCCN 97194455 , leggi online ) , p. 181.
- (in) J. Thomson , " sono alcuni movimenti curiosi osservabili sulle superfici del vino e di altri liquori alcolici " , Philos. Mag. , vol. 10,1855, p. 330-333 ( leggi in linea ).
- (en) GA Mills e EE Ecklund , " Alcohols as Components of Transportation Fuels " , Annu. Rev. Energia circa. , vol. 12,Novembre 1987, p. 47-80 ( DOI 10.1146 / annurev.eg.12.110187.000403 ).
- (en) PB Morais , CA Rosa et al. , " Produzione di alcool combustibile da ceppi di Saccharomyces da habitat tropicali " , Biotechnol. Lett , vol. 18, n o 11,1996, p. 1351-1356 ( ISSN 0141-5492 , DOI 10.1007 / BF00129969 ).
- (in) PC Badger , J. Janick (a cura di ) e A. Whipkey (a cura di ), Trends in new crop and new uses , Alexandria, VA, ASHS Press,2002, 599 p. ( ISBN 978-0-09-707565-5 , letto online ) , "Etanolo dalla cellulosa: una revisione generale" , p. 17–21.
- (in) MJ Taherzadeh e K. Karimi , " Processi di idrolisi a base di acido per etanolo da materiali lignocellulosici: una revisione " , BioRes. , vol. 2 n o 3,2007, p. 472-499 ( ISSN 1930-2126 , leggi in linea ).
- (in) MJ Taherzadeh e K. Karimi , " Processi di idrolisi basati su enzimi per etanolo da materiali lignocellulosici: una revisione " , BioRes. , vol. 2, n o 4,2007, p. 707-738 ( ISSN 1930-2126 , leggi in linea ).
- (in) SK Ritter , " Esplosione d'oro da biomassa: la tecnologia per utilizzare zuccheri di origine vegetale per produrre materie prime chimiche è pronta e in attesa ... " , Chem. Eng. Notizie , vol. 82, n o 22,Maggio 2004, p. 31-34 ( ISSN 0009-2347 , leggi in linea ).
- (in) " Brew Better Ethanol " su Popular Science Online ,2006(visitato il 18 maggio 2012 ) .
- (in) DR Lide (a cura di ), CRC Handbook of Chemistry and Physics , Boca Raton, FL, CRC Press ,2007, 88 ° ed. , 2640 p. ( ISBN 978-0-8493-0488-0 ) , cap. 8 ("Analytical Chemistry") , p. 42.
- (in) HD Hinton e JA Nieuwland , " Organic Reactions with Boron Fluoride. I. La preparazione degli esteri " , J. Am. Chem. Soc. , vol. 54, n o 5,1932, p. 2017-2018 ( ISSN 0002-7863 , DOI 10.1021 / ja01344a046 ).
- (in) " Rulemaking History for OTC Sweet Spirits of Nitre Drug Products " su Food and Drug Administration (visitato il 22 maggio 2012 ) .
- (in) K. Schumann e K. Siekmann , Ullmann Encyclopedia of Industrial Chemistry , Wiley-VCH Verlag ,2000( ISBN 978-3-527-30673-2 , presentazione online ) , "Saponi".
- Lide, 2007 , cap. 5 ("Termochimica, elettrochimica e cinetica"), p. 70.
- Lide, 2007 , cap. 15 ("Dati pratici di laboratorio"), p. 17 .
- (a) R. Swift e D. Davidson , " Alcohol Hangover: Mechanisms and Mediators ' , Alcohol Health Res. W. , vol. 22, n o 1,1998, p. 54-60 ( leggi in linea ).
- (in) L. Hipolito , J. Sanchez et al. , " Metabolismo cerebrale di etanolo e alcolismo: un aggiornamento " , Curr. Drug Metab , vol. 8, n o 7,ottobre 2007, p. 716-727 ( ISSN 1389-2002 , PMID 17979660 , DOI 10.2174 / 138920007782109797 ).
- (pdf) Scheda tossicologica N ° 120 dell'INRS, consultata il 24 giugno 2017
- Juan I. Garaycoechea e al. (2018) L'alcol e le aldeidi endogene danneggiano i cromosomi e mutano le cellule staminali | Nature | doi: 10.1038 / nature25154 | pubblicato online il 3 gennaio 2018 | riassunto
- (a) L. Kurti e B. Czako , Strategic Applications of Named Reactions in Organic Synthesis , Academic Press ,2005, 864 p. ( ISBN 978-0-12-369483-6 , presentazione online ) , p. 264-265.
- GS Serullas , " Carbon idrioduro. Circostanze particolari in cui si è verificata questa tripla combinazione; mezzi per produrlo all'istante ”, Annal. Chim. Phys. , vol. 20,Maggio 1822, p. 17-37 ( leggi in linea ).
- " L'ultimo cambio di superetanolo E85..N645843 " , su usinenouvelle.com .
- (in) G. McDonnell e AD Russell , " Antisettici e disinfettanti: attività, azione e resistenza " , Clin. Microbiol. Rev. , vol. 12, n o 1,1999, p. 147–179 ( ISSN 0893-8512 , PMCID PMC88911 , leggi online [PDF] ).
- (en) DG Barceloux , GR Bond et al. , " Linee guida di pratica dell'American Academy of Clinical Toxicology sul trattamento dell'avvelenamento da metanolo " , Clin. Toxicol. , vol. 40, n o 4,2002, p. 415-446 ( DOI 10.1081 / CLT-120006745 ).
- (a) YB Shvets , stazione di Washington: My Life as a KGB spy in America , New York, Simon & Schuster ,1995, 298 p. ( ISBN 978-0-671-88397-3 ).
- (in) " V2 " su Rocket and Space Technology (visitato il 27 maggio 2012 ) .
- (a) " propellenti per razzi " , su Internet Encyclopedia of Science (accessibile 27 maggio 2012 ) .
- (in) " A Brief History of Rocketry " sul Kennedy Space Center (visitato il 27 maggio 2012 ) .
- (a) LA Pohorecky e J. Mattone , " Farmacologia di etanolo " , Pharmacol. Ther. , vol. 36, n osso 2-3,1988, p. 335-427 ( ISSN 0163-7258 , PMID 3279433 , DOI 10.1016 / 0163-7258 (88) 90109-X ).
- (in) " Ethanolum anhydricum " su European Directorate for the Quality of Medicines (visitato il 28 maggio 2012 ) .
- (in) DJ Nutt , THE King et al. , " Drug harms in the UK: a multicriteria decision analysis " , Lancet , vol. 376, n o 9752,6 novembre 2010, p. 1558-1565 ( ISSN 0140-6736 , DOI 10.1016 / S0140-6736 (10) 61462-6 ).
- (it) DA Yost , “ cure acute per intossicazione da alcool. Preparati a considerare i dilemmi clinici ” , Postgrad Med. , vol. 112, n o 6,2002, p. 14-26 ( ISSN 0032-5481 , PMID 12510444 , DOI 10.3810 / pgm.2002.12.1361 ).
- (a) V. Santhakumar , Mr. Wallner et al. , " L'etanolo agisce direttamente sui sottotipi extrasinaptici dei recettori GABA A per aumentare l'inibizione tonica " , Alcohol , vol. 41, n ° 3,Maggio 2007, p. 211–221 ( ISSN 0741-8329 , PMID 17591544 , PMCID PMC2040048 , DOI 10.1016 / j.alcohol.2007.04.011 , leggi online ).
- Virgolini, MB, Mattalloni, MS, Deza-Ponzio, R., Albrecht, PA, & Cancela, LM (2019). Esposizione al piombo e assunzione di etanolo: stress ossidativo come meccanismo d'azione convergente . In Neuroscience of Alcohol (pp. 515-525). Academic Press ( abstract ).
- (en) Fein G, D Greenstein, Cardenas VA, Cuzen NL, Stein DJ et al. , " Volumi corticali e subcorticali negli adolescenti con dipendenza da alcol ma senza sostanze o comorbidità psichiatriche " , Psychiatry Res , vol. 214, n o 1,2013, p. 1-8. ( PMID 23916536 , PMCID PMC4203651 , DOI 10.1016 / j.pscychresns.2013.06.001 , leggi online [html] )
- (in) Little G, P Maurage, Kornreich C Verbanck P, S Campanella, " Binge drinking in adolescents: a review of neurophysiological and neuroimaging research " , Alcohol Alcohol , vol. 49, n o 22014, p. 198-206. ( PMID 24302160 , DOI 10.1093 / alcalc / agt172 , leggi online [html] )
- (en) K. Nakamura , K. Iwahashi et al. , “ Addotti dell'acetaldeide nel cervello degli alcolisti ” , Arch. Toxicol. , vol. 77, n o 10,2003, p. 591-593 ( ISSN 0340-5761 , DOI 10.1007 / s00204-003-0465-8 ).
Vedi anche
Bibliografia
- (en) JE Logsdon , Kirk-Othmer Encyclopedia of Chemical Technology , John Wiley & Sons ,2004( ISBN 978-0-471-23896-6 , DOI 10.1002 / 0471238961.0520080112150719.a01.pub2 , leggi online ) , "Etanolo".
- (en) LA Pohorecky e J. Brick , " Pharmacology of ethanol " , Pharmacol. Ther. , vol. 36, n osso 2-3,1988, p. 335-427 ( ISSN 0163-7258 , PMID 3279433 , DOI 10.1016 / 0163-7258 (88) 90109-X ).
Articoli Correlati
- Altri alcoli: alcool , alcool primario , metanolo , propanolo e butanolo
- Qualità: alcool assoluto , alcool denaturato , alcool denaturato e alcool rettificati
- Produzione: fermentazione alcolica , etanolo di cellulosa
- Uso: alcool , bioetanolo , bevanda alcolica , bevanda spiritosa , industria degli alcolici
- Storia: Storia della birra , Storia della vite e del vino
- Proprietà fisiologiche: alcool deidrogenasi , alcolemia , Alcolismo , Una notte da leoni , intossicazione da alcool , sindrome alcolica fetale
- Varie: Calcolo dei titoli di alcol e volumi , Grado di alcol , Tears di vino , macerazione alcolica










