Reazione di disidratazione
In chimica, una reazione di disidratazione è una reazione chimica in cui il reagente di partenza perde un atomo di idrogeno e un gruppo idrossile , o una molecola d'acqua , il contrario della reazione di idratazione . Le reazioni di disidratazione sono una sottocategoria delle reazioni di eliminazione .
Poiché il gruppo idrossile (–OH) è un cattivo gruppo uscente , avere un acido di Brønsted come catalizzatore promuove la protonazione del gruppo, trasformandolo in –OH 2 + , il migliore gruppo uscente. Gli agenti disidratanti comunemente usati nella sintesi organica sono acido solforico concentrato , acido fosforico concentrato , ossido di alluminio caldo e ceramica calda.
Una reazione di condensazione a volte può rilasciare una molecola d'acqua come prodotto. Questo a volte è indicato come sintesi per disidratazione. Questo è ad esempio il caso di due monosaccaridi , come il glucosio o il fruttosio , che possono condensarsi in un disaccaride ( saccarosio ) per sintesi per disidratazione. La reazione inversa è quindi idrolisi , l'acqua si ricombina con i due gruppi idrossilici, il disaccaride viene riconvertito in due monosaccaridi.
Esempi
Nella sintesi organica, ci sono molti esempi di reazione di disidratazione, ad esempio la disidratazione di alcoli o zuccheri.
| Reazioni di disidratazione | ||
| Reazione | Equazione | Esempi |
|---|---|---|
| Conversione di alcoli in eteri | 2 R-OH → ROR + H 2 O | |
| Conversione di alcoli in alcheni | R-CH 2- CHOH-R → R-CH = CH-R + H 2 O | ad esempio, conversione del glicerolo in acroleina :
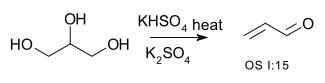 o disidratazione del 2-metil-1-cicloesanolo a (principalmente) 1-metilcicloesene :  |
| Conversione degli acidi carbossilici in anidridi acide | 2 RCOOH → (RCO) 2 O + H 2 O | |
| Conversione delle ammidi in nitrili | RCONH 2 → R-CN + H 2 O | |
| Riarrangiamento dienolo-benzene | 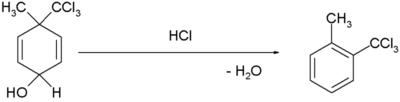 |
|
Note e riferimenti
- Sintesi organiche OS I: 15 Link
- Disidratazione del 2-metil-1-cicloesanolo: nuovi risultati da un popolare esperimento di laboratorio universitario J. Brent Friesen e Robert Schretzman J. Chem. Educ., 2011, 88 (8), pagg. 1141–1147 DOI : 10.1021 / ed900049b
- H. Plieninger e Gunda Keilich, " Die Dienol-Benzol-Umlagerung ", Angew. Chem. , vol. 68, n o 19,1956, p. 618–618 ( DOI 10.1002 / angel.19560681914 )
- Margaret Jevnik Gentles, Jane B. Moss, Hershel L. Herzog e EB Hershberg, “ The Dienol-Benzene Rearrangement. Some Chemistry of 1,4-Androstadiene-3,17-dione ", J. Am. Chem. Soc. , vol. 80, n o 14,1958, p. 3702–3705 ( DOI 10.1021 / ja01547a058 )
- ( fr ) Questo articolo è parzialmente o interamente tratto dall'articolo di Wikipedia in inglese intitolato " Reazione alla disidratazione " ( vedere l'elenco degli autori ) .