Reazione di Kulinkovich
La reazione kulinkovich è una ciclopropanazione di esteri carbossilici che portano diastereoselettivamente ai ciclopropanoli .

Versione stechiometrica
I primi esempi di reazioni di Kulinkovich , descritti nel 1989, impiegavano una quantità stechiometrica di tetraisopropilossititanio. Tre equivalenti del reagente di Grignard erano necessari per ottenere buone rese.
Versione catalitica
È stato nel 1991 che Kulinkovich ha dimostrato che una quantità catalitica di tetraisopropilossitanio era sufficiente per ottenere buone rese. È stato persino possibile, in queste condizioni, ridurre la quantità impegnata di reagente di Grignard a due equivalenti.
Versione asimmetrica della reazione di Kulinkovich
Poiché la reazione di Kulinkovich era catalitica in titanio, Corey e il suo team ne hanno rilasciato una versione asimmetrica. Hanno ottenuto eccessi enantiomerici fino al 78% utilizzando un ligando di tipo Taddol.
Meccanismo
Il meccanismo comunemente invocato coinvolge la prima di due fasi successive di transmetallazione del reagente di Grignard impegnato, portando a un complesso intermediario dialchildiisopropilossitanico. Questo subisce una sproporzione per dare una molecola di alcano e un titanaciclopropano 1 . L'inserimento dell'estere carbonile nel più chiaro legame carbonio - titanio di questa specie si traduce in un ossatitanaciclopentano 2 che si riorganizza in chetone 3 . Infine, l'inserimento del gruppo carbonile 3 nel legame residuo carbonio-titanio chiude il ciclopropano. Nello stato di transizione di questa fase elementare, che è la fase limitante della reazione, è stata invocata un'interazione agostica stabilizzante tra l' idrogeno in α del gruppo R² e l'atomo di titanio per spiegare la diastereoselettività osservata. Il Complesso 4 ottenuto è un tetraalchilossititanio in grado di svolgere un ruolo analogo a quello del tetraisopropilossititanio di partenza, che chiude il ciclo catalitico . Al termine della reazione, il prodotto si trova principalmente sotto forma di magnesio alcolato 5 , dando ciclopropanolo al momento dell'idrolisi del mezzo di reazione .

Il meccanismo della reazione di Kulinkovich è stato oggetto di ampi calcoli pubblicati nel 2001. Alcuni punti restano tuttavia poco chiari e, con ogni probabilità, il meccanismo di questa reazione in realtà non è così semplice. Complessi intermedi di titanio del tipo " mangiato " sono stati recentemente proposti da Kulinkovich.
Reazioni di scambio di leganti con olefine
Già nel 1993, il team di Kulinkovich ha dimostrato la capacità dei titanaciclopropani di subire scambi di leganti con olefine . Questa scoperta è stata importante, perché ha dato accesso a ciclopropanoli più funzionalizzati evitando la preparazione del corrispondente magnesio, di cui avrebbero dovuto essere utilizzati almeno due equivalenti per ottenere buone rese. Cha e il suo team hanno introdotto l'uso di reagenti ciclici di Grignard, particolarmente adatti per queste reazioni di scambio di leganti.
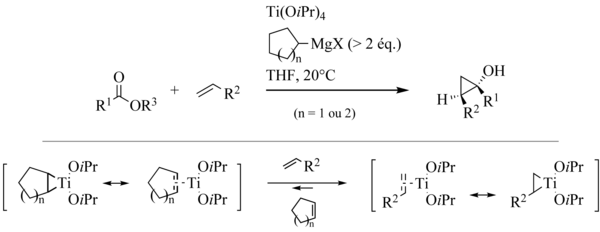
Reazioni di Kulinkovich intramolecolari
Un'interessante applicazione delle reazioni di scambio ligando consiste nell'effettuare reazioni intramolecolari a partire da esteri con funzione olefinica.
Reazioni correlate
Sono state sviluppate diverse estensioni della reazione Kulinkovich :
- la reazione di Kulinkovich-de Meijere , che porta agli amminociclopropani dalle ammidi.
- la reazione Kulinkovich-Szymoniak , che porta agli aminociclopropani dai nitrili.
- Vedi anche: F. Sato, H. Urabe e S. Okamoto, Pure Appl. Chem. , 1999 , 71 , 1511-1519.
Fonti di ulteriori informazioni
Sono apparsi diversi articoli di approfondimento sull'argomento:
- OG Kulinkovich e A. de Meijere, Chem. Rev. , 2000 , 100 , 2789–2834.
- F. Sato et al., Synlett , 2000 , 753–775.
- A. de Meijere, SI Kozhushkov e AI Savchenko in Titanium and Zirconium in Organic Synthesis (Ed.: I. Marek), Wiley-VCH, Weinheim, 2002 , p. 390–434.
- OG Kulinkovich, Chem. Rev. , 2003 , 103 , 2597-2632.
- OG Kulinkovich, Russ. Chem. Bull., Int. Ed. , 2004 , 53 , 1065-1086.
- OG Kulinkovich, Eur. J. Org. Chem. , 2004 , 4517–4529.
- A. Wolan e Y. Six, Tetrahedron , 2010 , 66 , 15–61.
- A. Wolan e Y. Six, Tetrahedron , 2010 , 66 , 3097–3133.
Per una modalità operativa con discussione, vedere:
Note e riferimenti
- OG Kulinkovich, SV Sviridov, DA Vasilevsky e TS Prityckaja, Zh. Org. Khim. , 1989 , 25 , 2244-2245.
- OG Kulinkovich, SV Sviridov e DA Vasilevski, Synthesis , 1991 , 234.
- EJ Corey, S. Achyutha Rao e Mark C. Noe, J. Am. Chem. Soc. , 1994 , 116 , 9345-9346.
- Y.–D. Wu e Z.-X. Yu, J. Am. Chem. Soc. , 2001 , 123 , 5777-5786.
- OG Kulinkovich e DG Kananovich, Eur. J. Org. Chem. , 2007 , 2121-2132.O.
- OG Kulinkovich, AI Savchenko, SV Sviridov e DA Vasilevski, Mendeleev Common. , 1993 , 230-231.
- J. Lee, H. Kim e JK Cha, J. Am. Chem. Soc. , 1996 , 118 , 4198-4199.
- A. Kasatkin e F. Sato, Tetrahedron Lett. , 1995 , 36 , 6079-6082.