Mutasi di bifosfoglicerato
| Mutasi di bifosfoglicerato
|

Dimero mutasi di bisfosfoglicerato umano ( PDB 2H4Z )
|
| Caratteristiche principali |
|---|
| Simbolo
|
BPGM
|
|---|
|
|
CE n.
|
5.4.2.4
|
|---|
| Homo sapiens |
|---|
|
|
Locus
|
7 q 33
|
|---|
|
Peso molecolare
|
30 005 Da
|
|---|
| Numero di residui
|
259 amminoacidi
|
|---|
|
|
Collegamenti accessibili da GeneCards e HUGO .
|
|
Entra
|
669
|
|---|
|
HUGO
|
1093
|
|---|
|
OMIM
|
613896
|
|---|
|
UniProt
|
P07738
|
|---|
|
RefSeq ( mRNA )
|
NM_001293085.1 , NM_001724.4 , NM_199186.2 , XM_011516527.1
|
|---|
|
RefSeq ( proteina )
|
NP_001280014.1 , NP_001715.1 , NP_954655.1 , XP_011514829.1
|
|---|
|
|
Insieme
|
ENSG00000172331
|
|---|
|
PDB
|
1T8P , 2A9J , 2F90 , 2H4X , 2H4Z , 2H52 , 2HHJ , 3NFY
|
|---|
|
|
GENATLAS • GeneTests • GoPubmed • HCOP • H-InvDB • Treefam • Vega
|
|
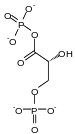
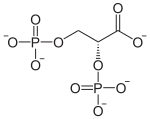
Il mutasi bisphosphoglycerate (BPGM) è un enzima specifico per eritrociti e cellule della placenta catalizzando l'isomerizzazione di 1,3-bisphospho- D -glycérate (1,3-BPG) prodotta durante glicolisi in 2,3-bisphospho - D -glycerate , che ha la proprietà di stabilizzare il desossi forma di emoglobina e quindi di rendere più efficace il trasporto di ossigeno nel sangue sotto bassa pressione parziale di O 2 adattando di conseguenza la curva di affinità.
Questa reazione è fisiologicamente utile solo in presenza di emoglobina , dove il 2,3-BPG ha l'effetto di provocare il rilascio di ossigeno legato all'ossiemoglobina stabilizzando la deossiemoglobina. Per questo la BPGM si trova solo negli eritrociti e nella placenta : in quest'ultima, permette di fornire maggiori quantità di ossigeno al feto .
Mutasi di bifosfoglicerato
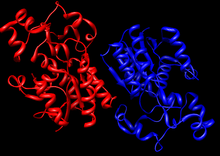
Struttura cristallina di un
dimero di mutasi di bisfosfoglicerato umano (
PDB 1T8P ).
Riferimenti
-
I valori per la massa e il numero dei residui indicato qui quelli della proteina precursore risultante dalla traduzione del gene , prima modificazioni post-traduzionali , e possono differire significativamente dai valori corrispondenti per il proteina funzionale.
-
(en) Wang Y, Wei Z, Bian Q, Cheng Z, Wan M, Liu L, Gong W, " Crystal structure of human Bisphosphoglycerate mutase " , J. Biol. Chem. , vol. 279, n . 37,
Settembre 2004, p. 39132–8 ( PMID 15258155 , DOI 10.1074 / jbc.M405982200 )

 Struttura cristallina di un dimero di mutasi di bisfosfoglicerato umano ( PDB 1T8P ).
Struttura cristallina di un dimero di mutasi di bisfosfoglicerato umano ( PDB 1T8P ).
