Acido selenio
| Acido selenio | |||
| |||
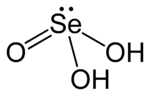
| Struttura dell'acido selenio | |||
| Identificazione | |||
|---|---|---|---|
| Nome IUPAC | acido selenio | ||
| N o CAS | |||
| N o ECHA | 100.029.067 | ||
| N o CE | 231-974-7 | ||
| N o RTECS | VS7175000 | ||
| PubChem | 1091 | ||
| ChEBI | 26642 | ||
| SORRISI |
O [Se] (O) = O , |
||
| InChI |
Std. InChI: InChI = 1S / H2O3Se / c1-4 (2) 3 / h (H2,1,2,3) Std. InChIKey: MCAHWIHFGHIESP-UHFFFAOYSA-N |
||
| Aspetto | solido bianco igroscopico | ||
| Proprietà chimiche | |||
| Formula bruta | H 2 SeO 3 | ||
| Massa molare | 128,97 ± 0,03 g / mol H 1,56%, O 37,22%, Se 61,22%, |
||
| Proprietà fisiche | |||
| T ° fusione | 70 ° C ( decomposizione ) | ||
| Solubilità | 1670 g · L -1 | ||
| Massa volumica | 3,004 g · cm da -3 a 15 ° C | ||
| Precauzioni | |||
| SGH | |||
   Pericolo H301, H331, H373, H410, P261, P273, P311, P301 + P310, P501, H301 : Tossico se ingerito H331 : Tossico se inalato H373 : Può provocare danni agli organi (elencare tutti gli organi interessati, se noti) in caso di esposizione ripetuta o prolungata (Indicare la via di esposizione se è definitivamente dimostrato che nessun'altra via di esposizione causa il pericolo) H410 : Molto tossico per gli organismi acquatici con effetti di lunga durata P261 : Evitare di respirare la polvere / i fumi / i gas / le nebbie / i vapori / gli aerosol. P273 : evitare il rilascio nell'ambiente. P311 : Contattare un CENTRO ANTIVELENI o un medico. P301 + P310 : In caso di ingestione: contattare immediatamente un CENTRO ANTIVELENI o un medico. P501 : Smaltire il contenuto / contenitore in ... |
|||
| Trasporto | |||
60 : materiale tossico o che presenta un grado di tossicità minore Numero UN : 3283 : COMPOSTO DI SELENIO, Classe NSA : 6.1 Etichetta: 6.1 : Materie tossiche Confezione: Gruppo di imballaggio II : sostanze moderatamente pericolose;  |
|||
| Unità di SI e STP se non diversamente specificato. | |||
L' acido selenio è un composto chimico di formula H 2 SeO 3. È il principale ossoacido del selenio , l'altro è l'acido selenico H 2 SeO 4. È un analogo di acido solforoso H 2 SO 3, ma è più facile isolare. Si ottiene facilmente aggiungendo biossido di selenio SeO 2e acqua H 2 O. Allo stato solido cristallizzato, le sue molecole sono piramidali, unite da legami idrogeno . In soluzione acquosa , è un diacido diprotico.
H 2 SeO 3 H + + HSeO 3- (p K a = 2,62) HSeO 3- H + + SeO 32– (p K a = 8,32)È debolmente ossidante, con cinetica abbastanza lenta. A 1 mol · L -1 di H + :
H 2 SeO 3+ 4 H + + 4 e - Se + 3 H 2 O ( E o = + 0,74 V ).A 1 mol · L -1 di ioni OH - :
SeO 32– + 4 e - + 3 H 2 O Se + 6 OH - ( E o = −0,37 V ).Viene utilizzato nella sintesi organica per produrre 1,2-dialdeidi , come gliossale O = CH - CH = O.
L'uso principale dell'acido selenio è nelle superfici metalliche azzurrate , in particolare negli acciai delle armi da fuoco . Pertanto, viene utilizzato l'acido selenio H 2 SeO 3con nitrato di rame (II) Cu (NO 3 ) 2e acido nitrico HNO 3per cambiare il colore dell'acciaio da grigio argento a grigio-blu o nero. Altri processi invece coinvolgono il solfato di rame CuSO 4e acido fosforico H 3 PO 4. Si forma in tutti i casi uno strato di passivazione in seleniuro di rame (I) Cu 2-δ If, che differenzia questi processi da altri azzurramento, che si traduce nella formazione di ossido di ferro (II, III) FeO · Fe 2 O 3.
Viene anche utilizzato in alcuni test per l'uso di stupefacenti.
Note e riferimenti
- massa molecolare calcolata dal " peso atomico degli elementi 2007 " su www.chem.qmul.ac.uk .
- Voce "Selenious acid" nel database delle sostanze chimiche GESTIS dell'IFA (ente tedesco responsabile per la sicurezza e la salute sul lavoro) ( tedesco , inglese ), accesso 22 maggio 2017 (JavaScript richiesto)
- (in) Anthony R. Ronzio e TD Waugh , " Glyoxal bisulfite " , Organic Syntheses , vol. 24, 1944, p. 61 ( DOI 10.15227 / orgsyn.024.0061 , leggi in linea )
- (in) " Kit / reagenti per test del colore per l'identificazione preliminare di droghe d'abuso " , norme per l'applicazione della legge e correzioni e programma di test presso il Dipartimento di giustizia degli Stati Uniti, programmi dell'Ufficio di giustizia, Istituto nazionale di giustizia , luglio 2000(visitato il 22 maggio 2017 ) .
