Reazione di Diels-Alder
La reazione Diels-Alder è una reazione chimica utilizzata in chimica organica , in cui un alchene (dienofilo) si aggiunge a un diene coniugato per formare un derivato del cicloesene . Otto Diels e Kurt Alder hanno ricevuto il Premio Nobel per la chimica nel 1950 per il lavoro relativo a questa reazione.
Nel campo dei materiali avanzati e della robotica flessibile si parla di “Diels-Alder polymers” ( “Diels-Alder polymers” ) per descrivere i polimeri costituiti da reti covalenti termoreversibili. Tale materiale è stato recentemente (2016-2017) testato con successo per tre attuatori pneumatici di robotica flessibile (un morsetto flessibile, una mano e muscoli artificiali) autoriparanti dopo lesioni mediante perforazione, lacerazione o colpi sul polimero in questione.
Ciclo-aggiunte
La reazione di Diels-Alder è un caso speciale di una classe più generale di reazioni: reazioni di cicloaddizione tra sistemi π. Nella reazione Diels-Alder, gli elettroni 4 π del diene reagiscono con il doppio legame dell'alchene contenente 2 elettroni π. Per questo motivo, questa reazione è chiamata cicloaddizione [4 + 2].
L'esecuzione di queste reazioni generalmente richiede il riscaldamento.
Regola dell'ontano
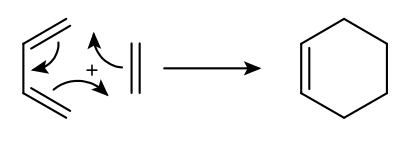
La facilità della reazione Diels-Alder dipende fortemente dalla natura dei sostituenti dieni e dienofili. La reazione prototipo di seguito, tra etene e but-1,3-diene, avviene con difficoltà e dà una resa piuttosto bassa di cicloesene.
La regola dell'ontano permette di specificare le condizioni che facilitano la produzione di queste cicloaddizioni: la reazione avviene più facilmente tra un diene ricco di elettroni e un dienofilo povero di elettroni. In altre parole, un diene "buono" è sostituito da atomi o gruppi di atomi che donano elettroni, un dienofilo "buono" da atomi o gruppi di atomi che attraggono (accettano) elettroni.
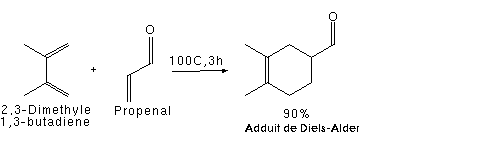
Questi caratteri, attrattori o donatori, possono essere effetti induttivi , mesomerici o di iperconiugazione . Di seguito, la reazione tra 2,3-dimetilbuta-1,3-diene (2 gruppi metilici donatori di elettroni) e propenale (gruppo aldeidico ritirante gli elettroni) avviene con una buona resa.
Gli alchino sostituiti dai gruppi attrattori sono buoni dienofili e sono soggetti a una reazione di Diels-Alders. Infatti, la reazione di un etino sostituito con 2 gruppi ritiranti (ad esempio, CH 3 OOC) -C≡C- (COOCH 3 ) con buta-1,3-diene dà una possibile reazione. D'altra parte, un composto comprendente due legami π coniugati di cui almeno uno è un alchino è un cattivo diene, perché non può essere posizionato nella conformazione s-cis. La reazione richiede una temperatura elevata.
Stereochimica della reazione
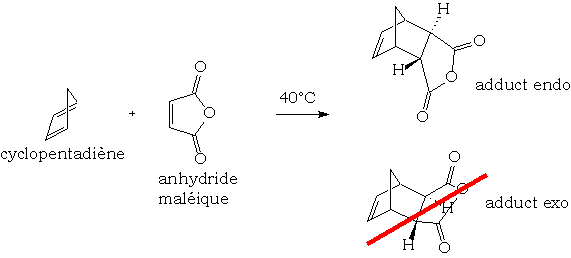
Questa reazione di cicloaddizione [4 + 2] è sotto controllo orbitale, che generalmente si traduce nella formazione di un endo stereoisomero quando il diene è ciclico. Questa selettività è spesso giustificata da considerazioni di confine secondarie che stabilizzano l'approccio endo:
La reazione è reversibile. Il composto endo è generalmente il più termodinamicamente stabile. Se si lascia che la reazione continui per un tempo molto lungo, l'equilibrio sarà quindi a favore del prodotto eso.
Carattere reversibile
Questa reazione è reversibile. Le reazioni inverse, chiamate retro-Diels-Alder , possono essere utilizzate per preparare composti. Ad esempio, il cracking termico del cicloesene consente di ottenere butadiene ed etene .
Alcuni autori usano erroneamente il termine "reversibile" invece di "reversibile" mentre qualsiasi trasformazione chimica crea entropia.
In pratica
La reazione Diels-Alder può essere problematica, ad esempio nel contesto dello stoccaggio del ciclopentadiene che dimerizza lentamente a temperatura ambiente per formare un composto triciclico, mediante reazione di Diels-Alder su se stesso. Il composto ottenuto, stabile a temperatura ambiente (T eb = 140 ° C ), deve essere distillato lentamente per recuperare il ciclopentadiene (T eb = 41 ° C ) per reazione retro-Diels-Alder .
Note e riferimenti
- (de) O. Diels e K. Alder , “ Synthesen in der hydroaromatischen Reihe. I. Mitteilung: Anlagerungen von Di-en kohlenwasserstoffen " , Liebigs Ann. Chem , vol. 460, n o 1,1928, p. 98–122 ( ISSN 0075-4617 , DOI 10.1002 / jlac.19284600106 ).
- (de) O. Diels e K. Alder , “ Synthesen in der hydroaromatischen Reihe. III. Mitteilung: Synthese von Terpenen, Camphern, hydroaromatischen und heterocyclischen Systemen " , Liebigs Ann. Chem , vol. 470, n o 1,1929, p. 62-103 ( ISSN 0075-4617 , DOI 10.1002 / jlac.19294700106 ).
- (de) O. Diels e K. Alder , “ Synthesen in der hydroaromatischen Reihe. IV. Mitteilung: Über die Anlagerung von Maleinsäure-anhydrid an arylierte Diene, Triene und Fulvene " , Ber. Dtsch. Chem. Ges. , vol. 62, n o 8,1929, p. 2081–2087 ( ISSN 0365-947X , DOI 10.1002 / cber.19290620829 ).
- (de) O. Diels e K. Alder , “ Synthesen in der hydroaromatischen Reihe. V. Mitteilung: Über Δ 4 -Tetrahydro-o-phthalsäure " , Ber. Dtsch. Chem. Ges. , vol. 62, n o 8,1929, p. 2087-2090 ( ISSN 0365-947X , DOI 10.1002 / cber.19290620830 ).
- Seppe Terryn, Joost Brancart, Dirk Lefeber, Guy Van Assche e Bram Vanderborght (2017), Robot pneumatici morbidi autoriparanti | Scienza robotica | 16 agosto 2017: Vol. 2, edizione 9, eaan4268 | DOI: 10.1126 / scirobotics.aan4268 | riassunto