Acido carbossilico
Il termine acido carbossilico si riferisce a una molecola comprendente un gruppo carbossilico (-C (O) OH). Sono acidi e le loro basi coniugate sono chiamate ioni carbossilato .
In chimica organica , un gruppo carbossilico è un gruppo funzionale composto da un atomo di carbonio , legato da un doppio legame a un atomo di ossigeno e legato da un singolo legame a un gruppo idrossile -OH.
Generale
In chimica , gli acidi carbossilici R-COOH costituiscono con gli acidi solfonici R-SO 3 H i due tipi di acidi della chimica organica . Si trovano abbondantemente in natura come acidi grassi ( lipidi ) e sono molto importanti nella chimica industriale . Ad esempio, l'acido acetico non è solo un elemento fondamentale per le complesse molecole presenti in biologia , ma è anche una molecola prodotta industrialmente che si trova nell'aceto . Uno dei più noti è l'acido acetilsalicilico o l'aspirina. I mattoni delle proteine , gli amminoacidi sono gli acidi carbossilici.
Il gruppo funzionale caratteristico è il gruppo carbossilico, dove R è l'idrogeno o un gruppo organico:

Gli acidi carbossilici hanno la formula grezza C n H 2 n O 2 quando R è un gruppo alchilico . Il calcolo del numero di insaturazione dà: . Questa insaturazione riflette il doppio legame carbonio-ossigeno .
I gruppi carbossilici sono spesso scritti nella forma ridotta: -COOH (forma non ionizzata del gruppo). La forma ionizzata del gruppo è: -COO - .
Si trova sempre alla fine della catena del carbonio . L'aggiunta di un gruppo carbossilico a un composto organico è una carbossilazione , la rimozione di questo stesso gruppo è una decarbossilazione .
Ioni carbossilato
Queste sono le basi coniugate R-COO - acidi carbossilici. Queste basi sono generalmente piuttosto deboli . La carica negativa sulla molecola è delocalizzata sui due atomi di ossigeno del gruppo carbossilico dal mesomerismo, il che spiega la relativa stabilità di questo tipo di molecole.

Lo ione carbossilato è un tensioattivo anfifilico , è la specie detergente del sapone . Infatti, il gruppo _COO- carbossilato è idrofilo perché molto polare . D'altra parte, la catena di carbonio R è apolare e quindi idrofobica e lipofila .
Nomenclatura
- Sistematico: se l'atomo di carbonio del gruppo carbossilico COOH è compreso nella catena principale del corrispondente idrocarburo (avente lo stesso numero di atomi di carbonio, con CH 3 invece di COOH), il nome di questo è seguito. Idrocarburo con il suffisso " -oic "(dioico per un diacido), e precedendolo con la parola" acido ". Altrimenti (in serie cicliche ad esempio), la parola “ acido ” è seguita dal nome dell'idrocarburo a cui è aggiunto il suffisso “-carbossilico”.
| Classe | Formula * del gruppo caratteristico |
Suffisso |
|---|---|---|
| Acidi carbossilici | - (C) OOH -COOH |
acido- ... acido oico ... -carbossilico |
- l'acido eptanoico CH 3 (CH 2 ) 5 -COOH può in alternativa essere chiamato acido esano-1-carbossilico se l'atomo di carbonio di -COOH non è incluso nella numerazione della catena;
- L'acido eptandioico HOOC- (CH 2 ) 5 -COOH è un acido bicarbossilico . Il suffisso -oic è preceduto dal prefisso moltiplicativo di- ;
- acido ciclopentancarbossilico: -COOH .
- Normale: come molti composti organici, gli acidi carbossilici hanno nomi comuni usati frequentemente in letteratura e che richiamano la fonte da cui sono stati isolati per la prima volta. Tuttavia, un elenco definito dalla IUPAC regola l'uso di nomi banali accettati accanto a nomi sistematici.
| genere | Struttura | Nome IUPAC | nome comune | fonte |
|---|---|---|---|---|
| Monoacidi alifatici | H-COOH | acido metanoico | acido formico | secreto da alcune formiche (latino: formica , formiche) |
| CH 3 -COOH | acido etanoico | acido acetico | Latino: acetum , aceto | |
| CH 3 CH 2 -COOH | acido propanoico | acido propionico | Greco: pedone , grasso | |
| CH 3 (CH 2 ) 2 -COOH | acido butanoico | acido butirrico | Greco: bouturos , burro | |
| CH 3 (CH 2 ) 3 -COOH | acido pentanoico | acido valerico | valeriana | |
| CH 3 (CH 2 ) 4 -COOH | acido esanoico | acido caproico | ||
| CH 3 (CH 2 ) 5 -COOH | acido eptanoico | acido enantico | ||
| CH 3 (CH 2 ) 6 -COOH | acido ottanoico | acido caprilico | cocco , latte materno | |
| CH 3 (CH 2 ) 7 -COOH | acido nonanoico | acido pelargonico | ||
| CH 3 (CH 2 ) 8 -COOH | acido decanoico | acido caprico | ||
| CH 3 (CH 2 ) 9 -COOH | acido undecanoico | acido undecilico | ||
| CH 3 (CH 2 ) 10 -COOH | acido dodecanoico | acido laurico | olio di cocco | |
| CH 3 (CH 2 ) 11 -COOH | acido tridecanoico | acido tridecilico | ||
| CH 3 (CH 2 ) 12 -COOH | acido tetradecanoico | acido miristico | Noce moscata | |
| CH 3 (CH 2 ) 13 -COOH | acido pentadecanoico | acido pentadecilico | ||
| CH 3 (CH 2 ) 14 -COOH | acido esadecanoico | acido palmitico | olio di palma | |
| CH 3 (CH 2 ) 15 -COOH | acido eptadecanoico | acido margarico | ||
| CH 3 (CH 2 ) 16 -COOH | acido ottodecanoico | acido stearico | grassi animali | |
| CH 3 (CH 2 ) 17 -COOH | acido nonadecanoico | acido non adecilico | ||
| CH 3 (CH 2 ) 18 -COOH | acido eicosanoico | acido arachidico | olio di arachidi , oli di pesce e oli vegetali | |
| CH 3 (CH 2 ) 20 -COOH | acido docosanoico | acido fenico | ||
| Monoacidi aromatici | C 6 H 5 -COOH | acido benzoico | benzene | |
| HO-C 6 H 4 -COOH | Acido 2-idrossibenzoico | acido salicilico | frutta (come salicilato di metile ) | |
| Acidi tiolici | CH 3 CH (SH) -COOH | Acido 2-mercaptopropanoico | acido tiolattico |
NB: un espediente mnemonico per ricordare i nomi degli acidi lineari, in ordine crescente del numero di atomi di carbonio, è la seguente frase: " O n M angel S aucisse G rillée A P anointed " ( O xalique, M alonique, S uccinic , G lutarico, A dipico, P imelico). I diacidi sono utilizzati per la sintesi di poliammidi e poliesteri .
Si possono citare altri tipi di acidi carbossilici: gli acidi dicarbossilici , gli acidi tricarbossilici , gli acidi alfa- idrossilati , i chetoacidi , gli amminoacidi e gli acidi grassi .
Proprietà fisiche e strutturali
stato
Gli acidi carbossilici sono liquidi in condizioni normali fintanto che la loro catena di carbonio ha meno di otto atomi di carbonio. Sono solidi oltre a questo.
Gli acidi a basso peso molecolare hanno un forte odore; per esempio l'acido butanoico è responsabile dell'odore del burro rancido.
Polarità, solubilità
La funzione dell'acido carbossilico è fortemente polare ed è sia donatore che accettore di legami idrogeno . Ciò consente la creazione di legami idrogeno, ad esempio con un solvente polare come acqua, alcol e altri acidi carbossilici.

A causa di questa proprietà, i piccoli acidi carbossilici (fino all'acido butanoico) sono completamente solubili in acqua. Le molecole di acido sono anche in grado di formare dimeri stabili mediante legami idrogeno, il che spiega perché il loro punto di ebollizione è superiore a quello degli alcoli corrispondenti.
Acidità
In soluzione in acqua, l'acido si dissocia parzialmente nello ione carbossilato, secondo l' equazione di equilibrio :
Questi sono acidi deboli in acqua ( p K A tra 4 e 5).
Come gli alcoli, gli acidi carbossilici mostrano un carattere acido e basico: la deprotonazione in ioni carbossilati è facile, ma la protonazione è più difficile. Hanno quindi un p K A inferiore a quello degli alcoli. Infatti l'acidità degli acidi carbossilici è spiegata dall'effetto induttivo nel gruppo carbossilico: il legame C = O è molto polarizzato ( elettronegatività dell'ossigeno maggiore di quella del carbonio) che rende il carbonio elettrofilo. , E quindi attrae elettroni dal altro ossigeno. Ora quest'altro ossigeno è esso stesso legato a un idrogeno, e anche questo legame è polarizzato , quindi l'elettrone dell'idrogeno che si è avvicinato all'ossigeno è a sua volta attratto dal carbonio elettrofilo. Questo idrogeno diventa quindi molto facilmente mobile, da qui l'acidità del gruppo carbossilico.
La solubilità dell'acido carbossilico aumenta con il pH .
Spettroscopia
Nell'infrarosso (IR), l'acido carbossilico ha due bande di valenza:
| Vibrazione | C = O | OH |
|---|---|---|
| Numero d'onda (cm −1 ) | 1.680-1.710 | 2.500-3.200 |
| Intensità | (forte) | grande, da medio a forte |
Struttura

Secondo la teoria VSEPR :
- la geometria attorno all'atomo di carbonio (legami) è di tipo trigonale;
- anche la geometria attorno all'atomo di ossigeno della funzione carbonilica (doppio legame + doppietti liberi) è di tipo trigonale;
- la geometria attorno all'atomo di ossigeno della funzione ossidrile (legami + doppietti liberi) è di tipo tetraedrico (AX 2 E 2 ).
L'acido carbossilico ha diverse forme mesomeriche .
Reattività
Come mostrato, tra le altre, le diverse formule mesomeriche dell'acido carbossilico:
- gli atomi di ossigeno sono siti nucleofili così come basi di Lewis;
- il carbonio centrale è elettrofilo;
- l'atomo di idrogeno elettrofilo è acido.
Derivati
Gli acidi carbossilici hanno molti derivati:
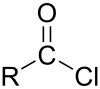
-
Anidride acida
- gli esteri
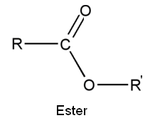
- le ammidi

- il nitrile
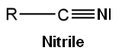
In termini di gruppo uscente (nucleofuge), l'ordine di facilità è:
Cl - (cloruro acilico), RCOO - (anidride), RO - (estere), - NH 2 e - NR 1 R 2 (ammidi).
Riduzione
Ossidazione
- Anidride carbonica (CO 2)
Sintesi
Sintesi per ossidazione
alcoli o aldeidi Gli acidi carbossilici possono essere ottenuti per ossidazione di aldeidi , quindi appunto per doppia ossidazione di alcoli primari .di alcheni esempio: sintesi dell'acido acetico per ossidazione del propene
Sintesi da un derivato acido
È semplicemente l'idrolisi dei vari derivati acidi.
estere- idrolisi in mezzo acido: retroesterificazione
- idrolisi in mezzo basico: saponificazione dell'estere
Sintesi per reazione di un reagente di Grignard su anidride carbonica
ReazioneLa sintesi avviene a bassa temperatura ( −40 ° C ). L'anidride carbonica è quindi in forma solida, chiamata ghiaccio secco . Viene messo in eccesso. Dopo la reazione, l'idrolisi viene eseguita in un mezzo acido per ottenere l'acido carbossilico.
MeccanismoPrimo passaggio : aggiunta del reagente di Grignard alla CO 2

Seconda fase : idrolisi in un mezzo acido
Sintesi malonica
La sintesi malonica è un insieme di reazioni che consentono la sintesi di molti acidi carbossilici primari o secondari dal dietil malonato .
È composta:
- una reazione acido-base tra dietil malonato ed etanoato ( sodio , potassio, ecc. );
- una sostituzione nucleofila , in cui il gruppo desiderato (primario o secondario) viene inserito per l'acido carbossilico finale;
- una doppia saponificazione delle due funzioni estere del dietil malonato sostituito, seguita da acidificazione del terreno;
- decarbossilazione (rilascio di anidride carbonica per riscaldamento);
- riorganizzazione del prodotto finale in acido carbossilico mediante tautomeria .
Questa sintesi è tanto più interessante in quanto a priori , che permette di sintetizzare qualsiasi acido carbossilico, dal momento che, a parte un gruppo terziario, sembra che possiamo mettere quello che vogliamo al posto di R .
Note e riferimenti
- R. Panico e J.-C. Richer, nomenclatura IUPAC dei composti organici , Masson, 1994, p. 70, 118- ( ISBN 978-2-225-84479-9 ) . Una matrice di suffissi (e prefissi) utilizzati per descrivere alcuni importanti gruppi di caratteristiche nella nomenclatura sostitutiva è disponibile in un riferimento IUPAC online (in inglese): suffissi e prefissi per le caratteristiche principali Alcuni gruppi nella nomenclatura sostitutiva .
- Robert Panico, Jean-Claude Richer e Jean Rigaudy , Nomenclature and terminology in organic chemistry - Functional classes. Stereochimica , tecniche ingegneristiche , 1996, p. 20 ( ISBN 2 85 059-001-0 ) .
- http://www.acdlabs.com/iupac/nomenclature/93/r93_705.htm











