Reazione di eliminazione
In chimica organica , l' eliminazione (o β-eliminazione ) è una reazione organica che trasforma un alcano sostituito ( aloalcani , alcoli, ecc.) In un derivato dell'etilene, o anche in un alchene , se la molecola di partenza, in aggiunta al gruppo uscente , n 'è solo una catena di carbonio di tipo alcano.
Le condizioni sono, oltre che dure, quelle di una sostituzione nucleofila , una reazione simile per molti aspetti e concorrente: l'eliminazione avviene in presenza di una base forte e riscaldando la miscela di reazione.
Equazione generale
Uno dei principali esempi di eliminazione è la conversione di un aloalcano in un alchene ; si parla quindi di deidroalogenazione :
Le basi più comunemente utilizzate sono la soda (Na + , HO - ), la potassa (K + , HO - ) o anche gli ioni alcolati (RO - ) (ottenuti facendo reagire il sodio in un alcol ROH, anidro ).
Proprio come per la sostituzione nucleofila c'è un'eliminazione monomolecolare e un'eliminazione bimolecolare che è comunemente indicata rispettivamente come E1 ed E2.
Nel resto di questo articolo, gli esempi sono forniti con un derivato alogenato come reagente.
Eliminazione monomolecolare
Cinetica E1
La reazione di eliminazione monomolecolare si svolge in due fasi: una fase monomolecolare che coinvolge solo la molecola del derivato alogenato sul lato reagente, che è la fase cineticamente limitante, seguita da una fase bimolecolare. Di conseguenza la cinetica della reazione, nell'approssimazione dello stadio cineticamente determinante (o limitante ), dipende solo dalla concentrazione della specie RX.
La reazione è quindi caratterizzata da una cinetica di ordine complessivo 1, di ordini parziali 1 rispetto al derivato alogenato e 0 rispetto alla base B | : v = k. [RX] , dove:
- [RX] rappresenta la concentrazione del derivato alogenato in mol.L −1
- v rappresenta la velocità della reazione di eliminazione. È espresso in mol.s −1 .
- k è la costante di velocità: è infatti quella del passo cineticamente limitante (k 1 ). La sua unità, Ls −1 , è dedotta da quelle degli altri due termini.
Meccanismo di E1
La reazione avviene in due fasi.
- Primo passo: partenza del nucleofugo, formazione di un carbocatione. questa fase di formazione del carbocatione è una fase lenta, reversibile e impone la sua velocità all'intera reazione.
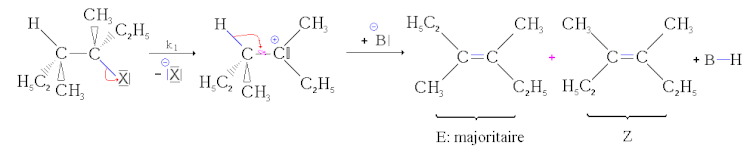
- Seconda fase: reazione acido-base. La base strappa il protone. Il doppietto quindi "si piega" sul legame carbonio-carbonio per formare un doppio legame . Poiché il legame singolo carbonio-carbonio può ruotare, si possono formare due stereoisomeri. Poiché questa reazione è molto più veloce della precedente, la sua velocità non influenza la velocità complessiva.

Stereoselettività e regioselettività
StereochimicaCome mostrato dal meccanismo, il passaggio attraverso un carbocatione, che è una struttura planare, rimuove qualsiasi elemento di stereospecificità a differenza (vedi sotto) del meccanismo di eliminazione bimolecolare.
Ma, se si possono formare due stereoiseomeri geometrici, non si formano nelle stesse proporzioni. L'isomero più stabile, cioè quello con l'energia più bassa, è formato prevalentemente (questa è la regola di Zaitsev). È quindi l'isomero E che si forma principalmente in assenza di mesomeria. D'altra parte, se il doppio legame di uno solo dei due prodotti può essere delocalizzato dalla mesomeria, allora è questo che si formerà principalmente. Questa è chiamata stereoselettività parziale.
 Regiochimica
Regiochimica
Quando si possono formare diversi isomeri costituzionali, si forma preferenzialmente l'alchene termodinamicamente più stabile. Se ci sono solo gruppi alchilici, questo è l'alchene più sostituito. Se può intervenire la mesomeria, è l'alchene più coniugato che è in maggioranza. Questo è indicato come regioselettività o regola di Zaïtsev .
Tuttavia, a volte si forma preferenzialmente l'alchene meno termodinamicamente stabile, questo viene indicato come eliminazione di Hofmann . Ciò è particolarmente vero quando la base utilizzata è congestionata (es. KtBuO) o quando c'è uno ione ammonio che viene eliminato, per esempio. (Molecola portante un'ammina in presenza di MeI in un numero di equivalenti sufficiente a formare il sale di ammonio, quindi posta in presenza di ossido d'argento umido e riscaldato. Formazione dell'alchene per eliminazione di Hofmann e quindi allontanamento. Di N (Me ) 3.)
Fattori che influenzano la risposta
I parametri che influenzano l'eliminazione di E1 sono:
- l'effetto di R-: lo stadio cineticamente determinante è la formazione del carbocatione (e non la sua reattività), quindi più è stabile più si favorisce la reazione.
- il nucleofuge: essendo la scissione del legame del gruppo C uscente il passaggio chiave nel meccanismo, la reazione dipende fortemente dalla natura di questo nucleofuge. Migliore è il gruppo di partenza, più veloce è la reazione. Ad esempio per la disidratazione degli alcoli, il primo passo è la protonazione dell'alcool per formare un ossonio, e quindi un miglior gruppo uscente (H 2 O⇒ HO - ). Una rapida classifica dei gruppi di partenza potrebbe essere:
(il segno ">" significa: "miglior gruppo iniziale di")
Si noti che la base non influenza questo tipo di reazione di ordine 1 e ciò in quanto non interviene durante la prima fase che determina la velocità complessiva della reazione.
Gruppo alchilico del derivato alogenatoIl meccanismo passa attraverso un intermedio di reazione del tipo carbocatione. Quest'ultimo è tanto più stabile quanto più viene sostituito. Quindi, la velocità di reazione (quindi di formazione del carbocatione) progredisce dai derivati primari, ai secondari e quindi a quelli terziari. In pratica, solo questi ultimi e pochi derivati secondari reagiscono con questo meccanismo.
NucleofugePiù polarizzabile è il collegamento RX, più facile è rompere. Questo legame è quindi di labilità decrescente ("fragilità") da fluoro a iodio: F> Cl> Br> I.
(il simbolo ">" significa: "più veloce di")
Solvente- Polarità: un solvente polare stabilizza il carbocatione; rende così più facile la prima reazione. La velocità quindi aumenta con la polarità del solvente.
- Proticità: un solvente protico è più un handicap: rischia infatti di competere con il carbocatione durante la (forte) reazione acido-base.
concorrenza
Questa reazione non solo compete con l'altra eliminazione, ma anche con le reazioni di sostituzioni nucleofile, in particolare con S N 1 . Quest'ultimo si verifica infatti in condizioni simili (oltre al riscaldamento).
Eliminazione bimolecolare
Cinetico
La reazione di eliminazione bimolecolare ha una cinetica di ordine globale 2 e di ordine parziale 1 rispetto alla derivata alogenata RX e alla base B: - . La reazione avviene in un unico passaggio bimolecolare, la velocità di reazione segue quindi una legge di tipo: v = k. [RX]. [B: - ] .
o :
- [RX] rappresenta la concentrazione del derivato alogenato (espressa in mol.L -1)
- [B: - ] rappresenta la concentrazione di base (espressa in mol.L −1 )
- v rappresenta la velocità della reazione di eliminazione. È espresso in mol.s −1 .
- k è la costante di velocità. La sua unità, Ls −1 .mol −1 , è dedotta da quelle degli altri due termini.
Meccanismo di E2
L'eliminazione bimolecolare è una reazione bimolecolare monofase.
Durante la stessa fase elementare si verifica lo strappo del protone da parte della base, la formazione del doppio legame e la partenza dell'atomo di alogeno (nucleofuga) sotto forma di ione alogenuro. Parliamo di un meccanismo sincrono o concertato.
Stereochimica
E2 è una reazione stereospecifica .
La reazione avviene solo quando l'idrogeno e il gruppo uscente sono in posizione anti-pleurplanare .
Fattori che influenzano la risposta
- La velocità di reazione di un E2 varia solo leggermente a seconda della classe (primaria: I, secondaria: II, terziaria: III) dell'alogenuro considerato. Tuttavia, più alta è la classe, più veloce è la reazione (III> II> I) per ragioni steriche (l'eliminazione permette di rimuovere sostituenti voluminosi, e quindi "voluminosi", nel prodotto finale, presente nel prodotto iniziale, il reagente , poiché in questo andiamo da un angolo di valenza di 109 ° 28 ', a livello del carbonio "sp 3 ", portando il protone H, ad un angolo di valenza di 120 °, nel prodotto finale dove questo stesso carbonio è ora "ibridizzato sp 2 "). Un aloalcano primario è generalmente preferito in questo caso, ma quando si è in presenza di un alogeno secondario, le reazioni di tipo E1 ed E2 si distinguono per i potenziali effetti mesomerici ( effetto "mesomero": termine generale che definisce un effetto elettronico corrispondente ad una delocalizzazione della carica, qui positiva, su un gruppo Arile, ad esempio, un vicino immediato, quindi "in α", del legame CH spezzato, si parla di "deprotonazione", dalla base forte). Qualsiasi sostituente sulla catena di carbonio in grado di stabilizzare lo ione carbenio (C + carbocatione ) attraverso questo tipo di effetto elettronico promuoverà il meccanismo E1.
- La velocità di reazione aumenta con la forza della base, quindi è necessaria una base forte.
- Anche il carattere nucleofugo del gruppo uscente ha un'influenza sulla reazione, ma questa influenza non è il parametro primario a differenza del meccanismo di eliminazione unimolecolare (E1).
- Per promuovere un meccanismo di reazione di eliminazione bimolecolare di E2, è opportuno utilizzare un solvente aprotico (DMSO, THF, toluene, n-esano, ecc.)
concorrenza
Questa reazione compete non solo con E1, ma anche con reazioni di sostituzione nucleofila, in particolare con S N 2 , che si verifica in condizioni simili. Si noti che una reazione di eliminazione richiederà più energia di una corrispondente reazione di sostituzione, solitamente mediante riscaldamento.
Osservazioni
La base utilizzata è anche un nucleofilo . Questo spiega la competizione con le reazioni delle sostituzioni. Alla fine della reazione si possono trovare, miscelati, prodotti di eliminazione e prodotti sostitutivi.