Aria
| Aria | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identificazione | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Codice ATC | V03 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietà chimiche | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Massa molare | 28,965 g / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietà fisiche | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fusione | −216,2 ° C ( 1 atm ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° bollitura | −194,3 ° C ( 1 atm , 874,0 kg / m 3 ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solubilità | 0,0292 vol / vol (acqua, 0 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
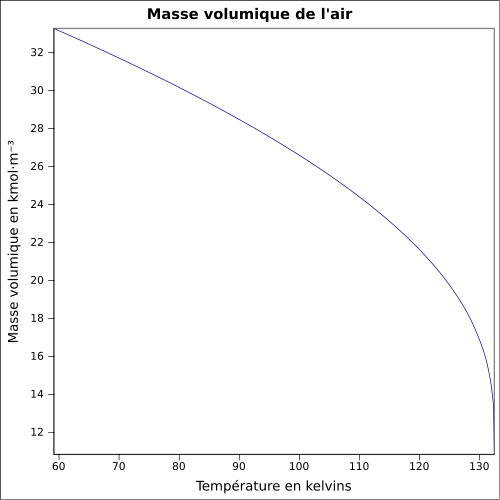
| Massa volumica |
1,2 kg / m 3 ( 21,1 ° C , 1 atm )
equazione:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pressione del vapore saturo |
equazione:
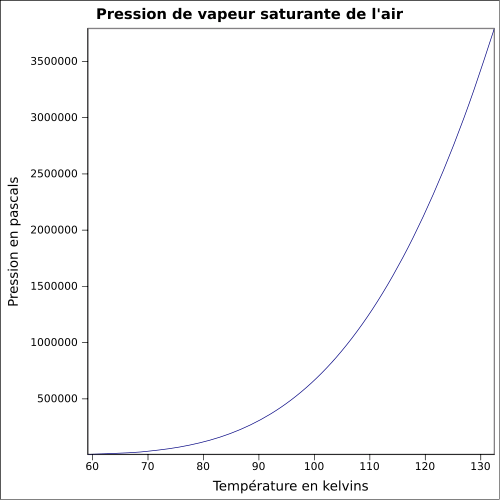
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto critico | −140,6 ° C , 3.771 kPa , 351 kg / m 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conduttività termica | 0,023 4 W m −1 K −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termochimica | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
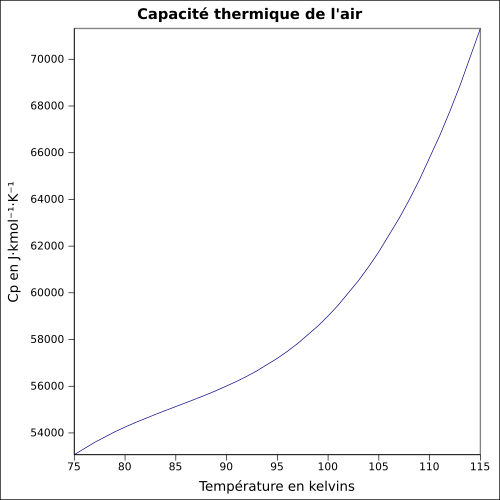
| C p |
equazione:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proprietà ottiche | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Indice di rifrazione | 1,00026825 ( 100 kPa , aria secca con 450 ppm di CO 2) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Unità di SI e STP se non diversamente specificato. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
L' aria è una miscela di gas che costituiscono l' atmosfera della Terra . Normalmente è incolore, invisibile e inodore.
Composizione
L'aria secca vicino al suolo è una miscela di gas omogenea. È composto approssimativamente dalla frazione molare o dal volume di:
Contiene anche tracce dello 0,000072% di diidrogeno (0,72 ppmv ), ma anche ozono , oltre a una minima presenza di radon . Può anche contenere anidride solforosa , ossidi di azoto , sostanze sospese fini in forma aerosol , polvere e microrganismi.
Il più delle volte, l'aria nell'ambiente terrestre è umida perché contiene vapore acqueo . In prossimità del suolo, la quantità di vapore acqueo è molto variabile. Dipende dalle condizioni climatiche, e in particolare dalla temperatura. La pressione parziale del vapore acqueo nell'aria è limitata dalla sua pressione del vapore saturo che varia notevolmente con la temperatura:
| Temperatura dell'aria | −10 ° C | 0 ° C | 10 ° C | 20 ° C | 30 ° C | 40 ° C |
| % vapore acqueo
per una pressione dell'aria di 1013 hPa |
Da 0 a 0,2% | Da 0 a 0,6% | Da 0 a 1,2% | Da 0 a 2,4% | Da 0 a 4,2% | Da 0 a 7,6% |
La percentuale di vapore acqueo presente nell'aria si misura dal tasso di umidità , è un elemento importante per le previsioni meteorologiche. Esistono diverse quantità per descrivere l'idrometria: umidità assoluta , che corrisponde alla massa di vapore acqueo per volume d'aria; e umidità relativa , che è la percentuale della pressione parziale del vapore acqueo rispetto alla pressione del vapore saturo .
Il livello di anidride carbonica varia nel tempo. Da un lato, esso subisce una variazione annua di circa 6,5 ppmv ( p ezione p ar m ilioni in v olume) ampiezza. D'altra parte, il tasso medio annuo aumenta da 1,2 a 1,4 ppmv all'anno. Circa 384 ppmv (0,0384%) a metà 2008, erano 278 ppmv prima della rivoluzione industriale , 315 ppmv nel 1958, 330 ppmv nel 1974 e 353 ppmv nel 1990. Questa serra a gas serra svolge un ruolo importante nel riscaldamento globale del pianeta .
Il metano è un'altra importante serra di gas il cui tasso aumenta nel tempo: 800 mm 3 / m 3 (0,8 ppmv ) nell'era preindustriale, 1585 mm 3 / m 3 nel 1985, 1663 mm 3 / m 3 nel 1992 e 1.676 mm 3 / m 3 nel 1996.
Fino a circa 80 km di altitudine, la composizione dell'aria secca è molto omogenea, l'unica variazione significativa nella composizione dell'aria è quella del contenuto di vapore acqueo.
Composizione dell'aria
|
|
||||||||||||||||||||||||||||||||||||||||||||
Le proporzioni di massa possono essere valutate moltiplicando le proporzioni di volume per il rapporto tra la massa molare del gas considerata divisa per la massa molare dell'aria, ovvero 28,976 g mol −1 , ad esempio nel caso di CO 2. Questo rapporto non è trascurabile poiché è pari a 44 / 28,976 = 1,5185 da qui il contenuto in massa di CO 2in aria pari a 415 × 1.5185 = 630 ppmm .
Massa volumica
Poiché l'aria è un gas comprimibile, la sua densità (in kg / m 3 ) è una funzione della pressione, della temperatura e dell'umidità.
Per aria secca a pressione atmosferica normale ( 1013,25 hPa ):
Generalmente prende 1.293 kg / m 3 a 0 ° C e 1.204 kg / m 3 a 20 ° C .
Questo è generalizzato ( formula del gas ideale ) in: (con T in kelvin e P in pascal secondo le convenzioni SI). Per una temperatura θ in gradi Celsius, la temperatura T in kelvin si ottiene aggiungendo 273,15 a θ : T (K) = θ (° C) + 273,15 .
Potenziale di riscaldamento globale
Il potenziale di riscaldamento globale (GWP in inglese : GWP: Global Warming Potential ) o CO 2 equivalentepermette di misurare la “nocività” di ogni gas serra .
La tabella seguente riporta il valore del GWP per i principali gas serra presenti nell'aria:
| PRG | 1 (riferimento) | 8 | 23 | 310 | da 1.300 a 1.400 | da 6.200 a 7.100 | 6500 | 22.800 |
| gas | diossido di carbonio | vapore acqueo | metano | protossido di azoto (N 2 O) | clorodifluorometano (HCFC) | diclorodifluorometano (CFC) | tetrafluoruro di carbonio (CF 4 ) | esafluoruro di zolfo (SF 6 ). |
Indice di rifrazione
L'espressione per l' indice di rifrazione dell'aria "in condizioni standard" è:
con dove è la lunghezza d'onda espressa in nanometri (nm), dove è il reciproco della lunghezza d'onda in micrometri.È per aria secca con 0,03% di anidride carbonica , a una pressione di 101.325 Pa (760 millimetri di mercurio) e una temperatura di 288,15 Kelvin ( 15 ° C ).
Possiamo ottenere n per una temperatura o pressione diversa, utilizzando una delle due espressioni seguenti:
con:
- T , temperatura espressa in kelvin ;
- p , pressione in pascal;
- T s , 288,15 K ;
- p s , 101.325 Pa ;
- n s , indice di rifrazione dell'aria dato sopra,
o :
con:
- T , temperatura in gradi Celsius ;
- T s , 15 ° C ;
- p , pressione in mmHg ;
- p s , 760 mmHg ;
- , 0,00366 K −1 ;
- , (1,049 - 0,015 T ) × 10-6 mmHg -1 ;
- , 8,13 × 10-7 mmHg -1 ;
- n s , indice di rifrazione dell'aria dato sopra.
Proprietà termofisiche
Dalle tabelle pubblicate da Frank M. White, Heat and Mass transfer , Addison-Wesley, 1988.
con:
- T , temperatura in Kelvin ;
- ρ , densità ;
- μ , viscosità dinamica ;
- ν , viscosità cinematica ;
- C p , calore specifico a pressione costante ;
- λ , conducibilità termica ;
- a , diffusività termica ;
- Pr , numero Prandtl .
| T | ρ | μ | ν | C p | λ | a | Pr |
|---|---|---|---|---|---|---|---|
| K | kg m −3 | kg m −1 s −1 | m 2 s −1 | J kg −1 K −1 | W m −1 K −1 | m 2 s −1 | - |
| 250 | 1.413 | 1,60 × 10 −5 | 0,949 × 10 −5 | 1.005 | 0.0223 | 1,32 × 10 −5 | 0.722 |
| 300 | 1.177 | 1,85 × 10 −5 | 1,57 × 10 −5 | 1.006 | 0.0262 | 2,22 × 10 −5 | 0.708 |
| 350 | 0.998 | 2,08 × 10 −5 | 2,08 × 10 −5 | 1.009 | 0.0300 | 2,98 × 10 −5 | 0.697 |
| 400 | 0.883 | 2,29 × 10 −5 | 2,59 × 10 −5 | 1.014 | 0.0337 | 3,76 × 10 −5 | 0.689 |
| 450 | 0.783 | 2,48 × 10 −5 | 2,89 × 10 −5 | 1.021 | 0.0371 | 4,22 × 10 −5 | 0.683 |
| 500 | 0.705 | 2,67 × 10 −5 | 3,69 × 10 −5 | 1.030 | 0.0404 | 5,57 × 10 −5 | 0.680 |
| 550 | 0.642 | 2,85 × 10 −5 | 4,43 × 10 −5 | 1.039 | 0.0436 | 6,53 × 10 −5 | 0.680 |
| 600 | 0.588 | 3,02 × 10 −5 | 5,13 × 10 −5 | 1.055 | 0.0466 | 7,51 × 10 −5 | 0.680 |
| 650 | 0.543 | 3,18 × 10 −5 | 5,85 × 10 −5 | 1.063 | 0.0495 | 8,58 × 10 −5 | 0.682 |
| 700 | 0.503 | 3,33 × 10 −5 | 6,63 × 10 −5 | 1.075 | 0.0523 | 9,67 × 10 −5 | 0.684 |
| 750 | 0.471 | 3,48 × 10 −5 | 7,39 × 10 −5 | 1.086 | 0.0551 | 10,8 × 10 −5 | 0.686 |
| 800 | 0.441 | 3,63 × 10 −5 | 8,23 × 10 −5 | 1.098 | 0.0578 | 12,0 × 10 −5 | 0.689 |
| 850 | 0.415 | 3,77 × 10 −5 | 9,07 × 10 −5 | 1 110 | 0.0603 | 13,1 × 10 −5 | 0.692 |
| 900 | 0.392 | 3,90 × 10 −5 | 9,93 × 10 −5 | 1.121 | 0.0628 | 14,3 × 10 −5 | 0.696 |
| 950 | 0.372 | 4,02 × 10 −5 | 10,8 × 10 −5 | 1.132 | 0.0653 | 15,5 × 10 −5 | 0.699 |
| 1000 | 0.352 | 4,15 × 10 −5 | 11,8 × 10 −5 | 1.142 | 0.0675 | 16,8 × 10 −5 | 0.702 |
| 1.100 | 0.320 | 4,40 × 10 −5 | 13,7 × 10 −5 | 1.161 | 0.0723 | 19,5 × 10 −5 | 0.706 |
| 1.200 | 0.295 | 4,63 × 10 −5 | 15,7 × 10 −5 | 1.179 | 0.0763 | 22,0 × 10 −5 | 0.714 |
| 1.300 | 0.271 | 4,85 × 10 −5 | 17,9 × 10 −5 | 1.197 | 0.0803 | 24,8 × 10 −5 | 0.722 |
Il rapporto tra temperatura e conducibilità termica dell'aria, valido per una temperatura compresa tra 100 K e 1600 K è il seguente:
o :
- : temperatura espressa in K
- : conducibilità termica in W m −1 K −1
La relazione tra viscosità dinamica dell'aria e temperatura è:
o :
- : temperatura in K
- : viscosità dinamica in kg m −1 s −1
La relazione tra viscosità cinematica dell'aria e temperatura è:
o :
- : temperatura in K
- : viscosità cinematica in m 2 / s
Secondo le informazioni WPI (en) , la relazione tra il calore specifico dell'aria e la temperatura è:
o :
- : temperatura in K
- : calore specifico in J kg −1 K −1
Pressione
A causa della diminuzione della pressione atmosferica con l' altitudine , è necessario pressurizzare le cabine di aeroplani e altri aeromobili . In pratica, la pressione imposta nelle cabine è maggiore della pressione esterna, sebbene inferiore alla pressione a livello del suolo.
L' aria compressa viene utilizzata anche nelle immersioni subacquee .
Liquefazione
L'aria è composta da diversi gas che, se sufficientemente raffreddati, alla fine passano allo stato liquido e quindi allo stato solido . Ad esempio, l' ossigeno diventa solido ad una temperatura di -218 ° C , i azoto liquefa a -195 ° C . Ad una temperatura di −270 ° C (circa 3 K ), tutti i gas tranne l' elio sono quindi solidi e si ottiene "aria congelata".
L'aria non può essere liquefatta prima che siano note le pressioni critiche e le temperature che segnano i limiti teorici oltre i quali un composto può esistere solo allo stato gassoso. Essendo l'aria una miscela, questi valori non hanno un significato stretto, ma, infatti, ad una temperatura superiore a -140 ° C l'aria non è più liquefacibile.
Temperatura di ebollizione dei componenti dell'aria
| Nome | Formula | Temperatura |
|---|---|---|
| Dinitrogen | No. 2 | −195,79 ° C , azoto liquido |
| Dioxygen | O 2 | −183 ° C , ossigeno liquido |
| Argon | Ar | −185,85 ° C |
| Diossido di carbonio | CO 2 | −56,6 ° C a 5,12 atm |
| Neon | Nato | −246,053 ° C |
| Elio | Hey | −268,93 ° C , elio liquido |
| Monossido di azoto | NO | −151,8 ° C |
| Krypton | Kr | −154,34 ° C |
| Metano | CH 4 | −161,52 ° C |
| Diidrogeno | H 2 | −252,76 ° C , idrogeno liquido |
| Ossido nitroso | N 2 O | −88,5 ° C |
| Xeno | Xe | −108,09 ° C |
| Diossido di azoto | NO 2 | 21,2 ° C |
| Ozono | O 3 | −111,9 ° C |
| Radon | Rn | −61,7 ° C |
Le prime gocce di aria liquida furono ottenute quasi contemporaneamente da Louis Paul Cailletet e Raoul-Pierre Pictet nel 1877 , per improvvisa espansione tra 300 e 1 atmosfera.
Nel 1894 , il fisico olandese Heike Kamerlingh Onnes sviluppò la prima installazione di aria liquida. Nei successivi 40 anni, i ricercatori in Francia, Gran Bretagna, Germania e Russia hanno apportato molti miglioramenti al processo.
Sir James Dewar ha liquefatto per la prima volta l' idrogeno nel 1898 e l' elio Heike Kamerlingh Onnes , il gas più difficile da liquefare, nel 1908 .
Indipendentemente da Carl von Linde , Georges Claude sviluppò nel 1902 un processo industriale per la liquefazione dell'aria.
Simbolico
- In un dominio non scientifico, l'aria è uno dei quattro elementi (insieme al fuoco , all'acqua e alla terra ) che una volta erano considerati (e ancora considerati in alcune culture) le sostanze su cui si sarebbero basati per tutta la vita. È il simbolo dello Spirito.
- L'aria è spesso associata a vari altri concetti come la famiglia delle spade nei mazzi dei tarocchi .
Note e riferimenti
Appunti
- Questa è la massa molare dell'aria secca.
Riferimenti
- " Air " , su olivier.fournet.free.fr (consultato il 4 marzo 2010 )
- (en) Compressed Gas Association, Handbook of compressed gases , Springer,1999, 4 ° ed. , 702 p. ( ISBN 0-412-78230-8 , leggi online ) , p. 234
- (en) Robert H. Perry e Donald W. verde , di Perry Chemical Engineers' Handbook , Stati Uniti d'America, McGraw-Hill,1997, 7 ° ed. , 2400 p. ( ISBN 0-07-049841-5 ) , p. 2-50
- (in) Philip E. Ciddor, " Indice di rifrazione dell'aria: nuove equazioni per il visibile e il vicino infrarosso " , Applied Optics , Vol. 35, n o 9,1996, p. 1566-1573 ( DOI 10.1364 / AO.35.001566 )
- (a) Recenti globale di CO2 su noaa.gov, accessibile 21 aprile, 2021.
- (in) The Keeling Curve , the keelingcurve.ucsd.edu website, consultato il 23 aprile 2015
- Concentrazione di CO 2 nell'atmosfera terrestre
- Concentrazione di CO 2 misurata a Mauna Loa (Hawaii), NOAA.
- Concentrazione di metano misurata a Mauna Loa (Hawaii), NOAA.
- In pratica, l'aria fortemente essiccata contiene ancora tracce di vapore acqueo.
- Fonte dati: anidride carbonica: (en) NASA - Earth Fact Sheet , gennaio 2007. Metano: IPCC TAR; tabella 6.1, 1998 (en) Terzo rapporto di valutazione IPCC "Climate Change 2001" di GRID-Arendal nel 2003. Il totale della NASA era di 17 ppmv su 100%, e la CO 2aumentato qui di 15 ppmv . Per normalizzare, N 2 dovrebbe essere ridotto di 25 ppmv e O 2 di 7 ppmv .
- " Indice di rifrazione dell'aria " , su olivier.fournet.free.fr (consultato il 4 marzo 2010 )
- Professionisti chimici
- Chemical Professionals , non trovato l'11 agosto 2013
- Questo documento dal sito Web WPI , sul sito wpi.edu
Vedi anche
Articoli Correlati
- Densità dell'aria
- Massa d'aria
- Psicrometria
- Aria umida
- Inquinamento atmosferico e articoli della categoria: Inquinamento atmosferico
- Qualità dell'aria